Bài ập CHọn Lọc Hóa Học 10
PGS.TS NGUYỄN XUÂN TRƯỜNG - TS.TRẦN TRUNG NINH
BÀI TẬP CHỌN LỌC
HÓA HỌC 10
(Chương trình chuẩn và nâng cao)
NHÀ XUẤT BẢN ĐẠI HỌC QUỐC GIA
THÀNH PHỐ HỒ CHÍ MINH - 2006
LỜI NÓI ĐẦU
Hóa học là một khoa học lý thuyết và thực nghiệm. Hóa học đòi hỏi sự chính xác của toán học đồng thời với sự linh hoạt trong tư duy và óc tưởng tượng phong phú, sinh động và sự khéo léo trong các thao tác thí nghiệm.
Chúng tôi giới thiệu cùng bạn đọc quyển "Bài tập chọn lọc Hóa học 10" chương trình chuẩn và nâng cao. Sách gồm các bài tập Hóa học chọn lọc trong chương trình Hóa học 10 có mở rộng và nâng cao, có thể sử dụng để phát triển năng lực tư duy Hóa học cho học sinh lớp 10 và phục vụ ôn tập các kì thi tú tài, thi tuyển sinh đại học, cao đẳng và thi học sinh giỏi. Quyển sách được biên soạn theo chương trình mới của Bộ Giáo dục và đào tạo. Sách được chia thành 7 chương, tương ứng với từng chương của sách giáo khoa Hóa học 10. Mỗi chương bao gồm các nội dung chính sau:
A- Tóm tắt lí thuyết.
B- Bài tập có hướng dẫn.
C- Hướng dẫn giải
D- Bài tập tự luyện
E- Bài tập trắc nghiệm
F- Thông tin bổ sung,
Sách có thể được sử dụng làm tài liệu tham khảo cho các thầy, cô giáo, cho các em học sinh mong có được một nền tảng vững chắc các kiến thức, tư duy và kĩ năng môn Hóa học lớp 10.
Mặc dù chúng tôi đã có nhiều cố gắng, nhưng do trình độ và thời gian biên soạn còn hạn chế nên không tránh khỏi các sai sót. Chúng tôi xin chân thành cảm ơn mọi ý kiến đóng góp của các bạn đọc, nhất là các thầy, cô giáo và các em học sinh để sách được hoàn chỉnh hơn trong lần tái bản sau.
Các tác giả
Chương 1
 NGUYÊN TỬ
NGUYÊN TỬ
A. TÓM TẮT LÍ THUYẾT
I. Thành phần nguyên tử
1. Lớp vỏ: Bao gồm các electron mang điện tích âm.
- Điện tích: qe = -1,602.10-19C = 1-
- Khối lượng: me = 9,1095.10-31 kg
2. Hạt nhân: Bao gồm các proton và các nơtron
a. Proton
- Điện tích: qp = +1,602.10-19C = 1+
- Khối lượng: mp = 1,6726.10-27 kg » 1u (đvC)
b. Nơtron
- Điện tích: qn = 0
- Khối lượng: mn = 1,6748.10-27 kg » 1u
Kết luận:
- Hạt nhân mang điện dương, còn lớp vỏ mang điện âm
- Tổng số proton = tổng số electron trong nguyên tử
- Khối lượng của electron rất nhỏ so với proton và nơtron
II. Điện tích và số khối hạt nhân
1. Điện tích hạt nhân
Nguyên tử trung hòa điện, cho nên ngoài các electron mang điện âm, nguyên tử còn có hạt nhân mang điện dương. Điện tích hạt nhân là Z+, số đơn vị điện tích hạt nhân là Z.
Số đơn vị điện tích hạt nhân (Z) = số proton = số electron
Thí dụ: Nguyên tử có 17 electron thì điện tích hạt nhân là 17+
2. Số khối hạt nhân
A = Z + N
Thí dụ: Nguyên tử có natri có 11 electron và 12 nơtron thì số khối là:
A = 11 + 12 = 23 (Số khối không có đơn vị)
3. Nguyên tố hóa học
- Là tập hợp các nguyên tử có cùng số điện tích hạt nhân.
- Số hiệu nguyên tử (Z): Z = P = e
- Kí hiệu nguyên tử:
 Trong đó A là số khối nguyên tử, Z là số hiệu nguyên tử.
Trong đó A là số khối nguyên tử, Z là số hiệu nguyên tử.
III. Đồng vị, nguyên tử khối trung bình
1. Đồng vị
- Là tập hợp các nguyên tử có cùng số proton nhưng khác nhau số nơtron (khác nhau số khối A).
- Thí dụ: Nguyên tố cacbon có 3 đồng vị: 
2. Nguyên tử khối trung bình
Gọi  là nguyên tử khối trung bình của một nguyên tố. A1, A2 ... là nguyên tử khối của các đồng vị có % số nguyên tử lần lượt là a%, b%...
là nguyên tử khối trung bình của một nguyên tố. A1, A2 ... là nguyên tử khối của các đồng vị có % số nguyên tử lần lượt là a%, b%...
Ta có:
IV. Sự chuyển động của electron trong nguyên tử. Obitan nguyên tử.
- Trong nguyên tử, các electron chuyển động rất nhanh xung quanh hạt nhân và không theo một quỹ đạo nào.
- Khu vực xung quanh hạt nhân mà tại đó xác suất có mặt của electron là lớn nhất được gọi là obitan nguyên tử.
- Obitan s có dạng hình cầu, obitan p có dạng hình số 8 nổi, obitan d, f có hình phức tạp.
V. Lớp và phân lớp
1. Lớp
- Các electron trong nguyên tử được sắp xếp thành lớp và phân lớp.
- Các electron trong cùng một lớp có mức năng lượng gần bằng nhau.
- Thứ tự và kí hiệu các lớp:
n | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
Tên lớp | K | L | M | N | O | P | Q |
2. Phân lớp
- Được kí hiệu là: s, p, d, f
- Số phân lớp trong một lớp chính bằng số thứ tự của lớp.
- Số obitan có trong các phân lớp s, p, d, f lần lượt là 1, 3, 5 và 7
- Mỗi obitan chứa tối đa 2 electron
VI. Cấu hình electron trong nguyên tử
1. Mức năng lượng
- Trật tự mức năng lượng: 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s ...
- Sự phân bố electron trong nguyên tử tuân theo các nguyên lí và quy tắc: Nguyên lí Pau-li, nguyên lí vững bền, quy tắc Hun.
2. Cấu hình electron
Sự phân bố các electron vào obitan trong nguyên tử tuân theo các quy tắc và nguyên lí:
- Nguyên lí Pauli: Trên một obitan có thể có nhiều nhất hai electron và hai electron này chuyển động tự quay khác chiều nhau xung quanh trục riêng của mỗi obitan.
- Nguyên lí vững bền: ở trạng thái cơ bản, trong nguyên tử các electron chiếm lần lượt những obitan có mức năng lượng từ thấp đến cao.
- Quy tắc Hun: Trong cùng một phân lớp, các electron sẽ phân bố trên obitan sao cho số electron độc thân là tối đa và các electron này phải có chiều tự quay giống nhau.
Cách viết cấu hình electron trong nguyên tử:
+ Xác định số electron
+ Sắp xếp các electron vào phân lớp theo thứ tự tăng dần mức năng lượng
+ Viết electron theo thứ tự các lớp và phân lớp.
Thí dụ: Viết cấu hình electron của Fe (Z = 26)
1s2 2s2 2p6 3s2 3p6 4s23d6 " 1s2 2s2 2p6 3s2 3p6 3d6 4s2
Sắp xếp theo mức năng lượng Cấu hình electron
B. BÀI TẬP CÓ LỜI GIẢI
1.1 Vì sao từ những ý tưởng đầu tiên về nguyên tử, cách đây 2500 năm của Democrit, mãi đến cuối thế kỉ XIX người ta mới chúng minh được nguyên tử là có thật và có cấu tạo phức tạp ? Mô tả thí nghiệm tìm ra electron.
1.2 Nguyên tử khối của neon là 20,179. Hãy tính khối lượng của một nguyên tử neon theo kg.
1.3 Kết quả phân tích cho thấy trong phân tử khí CO2 có 27,3% C và 72,7% O theo khối lượng. Biết nguyên tử khối của C là 12,011. Hãy xác định nguyên tử khối của oxi.
1.4 Biết rằng khối lượng một nguyên tử oxi nặng gấp 15,842 lần và khối lượng của nguyên tử cacbon nặng gấp 11,9059 lần khối lượng của nguyên tử hiđro. Hỏi nếu chọn  khối lượng nguyên tử cacbon làm đơn vị thì H, O có nguyên tử khối là bao nhiêu ?
khối lượng nguyên tử cacbon làm đơn vị thì H, O có nguyên tử khối là bao nhiêu ?
1.5 Mục đích thí nghiệm của Rơ-dơ-pho là gì? Trình bày thí nghiệm tìm ra hạt nhân nguyên tử của Rơ-dơ-pho và các cộng sự của ông.
1.6 Hãy cho biết số đơn vị điện tích hạt nhân, số proton, số nơtron và số electron của các nguyên tử có kí hiệu sau đây :
1.7 Cách tính số khối của hạt nhân như thế nào ? Nói số khối bằng nguyên tử khối thì có đúng không ? tại sao ?
1.8 Nguyên tử khối trung bình của bạc bằng 107,02 lần nguyên tử khối của hiđro. Nguyên tử khối của hiđro bằng 1,0079. Tính nguyên tử khối của bạc.
1.9 Cho hai đồng vị hiđro với tỉ lệ % số nguyên tử :  (99,984%),
(99,984%),  (0,016%) và hai đồng vị của clo :
(0,016%) và hai đồng vị của clo :  (75,53%),
(75,53%),  (24,47%).
(24,47%).
a) Tính nguyên tử khối trung bình của mỗi nguyên tố.
b) Có thể có bao nhiêu loại phân tử HCl khác nhau được tạo nên từ hai loại đồng vị của hai nguyên tố đó.
c) Tính phân tử khối gần đúng của mỗi loại phân tử nói trên.
1.10 Nguyên tử khối trung bình của đồng bằng 63,546. Đồng tồn tại trong tự nhiên dưới hai dạng đồng vị  và
và  . Tính tỉ lệ % số nguyên tử đồng
. Tính tỉ lệ % số nguyên tử đồng  tồn tại trong tự nhiên.
tồn tại trong tự nhiên.
1.11 Cho hai đồng vị  (kí hiệu là H),
(kí hiệu là H),  (kí hiệu là D).
(kí hiệu là D).
a) Viết các công thức phân tử hiđro có thể có.
b) Tính phân tử khối của mỗi loại phân tử.
c) Một lit khí hiđro giàu đơteri ( ) ở điều kiện tiêu chuẩn nặng 0,10g. Tính thành phần % khối lượng từng đồng vị của hiđro.
) ở điều kiện tiêu chuẩn nặng 0,10g. Tính thành phần % khối lượng từng đồng vị của hiđro.
1.12 Có thể mô tả sự chuyển động của electron trong nguyên tử bằng các quỹ đạo chuyển động được không ? tại sao ?
1.13 Theo lí thuyết hiện đại, trạng thái chuyển động của electron trong nguyên tử được mô tả bằng hình ảnh gì ?
1.14 Trình bày hình dạng của các obitan nguyên tử s và p và nêu rõ sự định hướng khác nhau của chúng trong không gian.
1.15 Biết rằng nguyên tố agon có ba đồng vị khác nhau, ứng với số khối 36, 38 và A. Phần trăm các đồng vị tương ứng lần lượt bằng : 0,34% ; 0,06% và 99,6%.
Tính số khối của đồng vị A của nguyên tố agon, biết rằng nguyên tử khối trung bình của agon bằng 39,98.
1.16 Nguyên tử Mg có ba đồng vị ứng với thành phần phần trăm như sau :
% 78,6 10,1 11,3
a) Tính nguyên tử khối trung bình của Mg.
b) Giả sử trong hỗn hợp nói trên có 50 nguyên tử  , thì số nguyên tử tương ứng của hai đồng vị còn lại là bao nhiêu ?
, thì số nguyên tử tương ứng của hai đồng vị còn lại là bao nhiêu ?
1.17 Hãy cho biết tên của các lớp electron ứng với các giá trị của n = 1, 2, 3, 4 và cho biết các lớp đó lần lượt có bao nhiêu phân lớp electron ?
1.18 Hãy cho biết số phân lớp, số obitan có trong lớp N và M.
1.19 Vẽ hình dạng các obitan 1s, 2s và các obitan 2px, 2py, 2pz.
1.20 Sự phân bố electron trong phân tử tuân theo những nguyên lí và quy tắc nào ? Hãy phát biểu các nguyên lí và quy tắc đó. Lấy thí dụ minh họa.
 1.21 Tại sao trong sơ đồ phân bố electron của nguyên tử cacbon (C : 1s22s22p2) phân lớp 2p lại biểu diễn như sau :
1.21 Tại sao trong sơ đồ phân bố electron của nguyên tử cacbon (C : 1s22s22p2) phân lớp 2p lại biểu diễn như sau :
1.22 Hãy viết cấu hình electron của các nguyên tố có Z = 20, Z = 21, Z = 22,
Z = 24, Z = 29 và cho nhận xét cấu hình electron của các nguyên tố đó khác nhau như thế nào ?
1.23 Hãy cho biết số electron lớp ngoài cùng của các nguyên tử H, Li, Na, K, Ca, Mg, C, Si, O.
1.24 Cấu hình electron trên các obitan nguyên tử của các nguyên tố K (Z = 19) và Ca (Z = 20) có đặc điểm gì ?
1.25 Viết cấu hình electron của F (Z = 9) và Cl (Z = 17) và cho biết khi nguyên tử của chúng nhận thêm 1 electron, lớp electron ngoài cùng khi đó có đặc điểm gì ?
1.26 Khi số hiệu nguyên tử Z tăng, trật tự năng lượng AO tăng dần theo chiều từ trái qua phải và đúng trật tự như dãy sau không ?
1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 6s 5d 6p 7s 5f 6d...
Nếu sai, hãy sửa lại cho đúng.
1.27 Viết câú hình electron nguyên tử của các nguyên tố có Z = 15, Z = 17, Z = 20, Z = 21, Z = 31.
1.28 Nguyên tử Fe có Z = 26. Hãy viết cấu hình elctron của Fe.
Nếu nguyên tử Fe bị mất hai electron, mất ba electron thì các cấu hình electron tương ứng sẽ như thế nào ?
1.29 Phản ứng hạt nhân là quá trình biến đổi hạt nhân nguyên tử do sự phân ró tự nhiên, hoặc do tương tác giữa hạt nhân với các hạt cơ bản, hoặc tương tác của các hạt nhân với nhau. Trong phản ứng hạt nhân số khối và điện tích là các đại lượng được bảo toàn. Trên cơ sở đó, hãy hoàn thành các phản ứng hạt nhân dưới đây:
1.30 Biết rằng quá trình phân rã tự nhiên phát xạ các tia  ,
,  và
và  (một dạng bức xạ điện từ). Hãy hoàn thành các phương trình phản ứng hạt nhân:
(một dạng bức xạ điện từ). Hãy hoàn thành các phương trình phản ứng hạt nhân:
C. BÀI TẬP TỰ LUYỆN
1.31 Bằng cách nào, người ta có thể tạo ra những chùm tia electron. Cho biết điện tích và khối lượng của electron. So sánh khối lượng của electron với khối lượng của nguyên tử nhẹ nhất trong tự nhiên là hiđro, từ đó có thể rút ra nhận xét gì?
1.32 Tính khối lượng nguyên tử trung bình của niken, biết rằng trong tự nhiên, các đồng vị của niken tồn tại như sau:
Thành phần % 67,76 26,16 1,25 3,66 1,16
1.33 Trong nguyên tử, những electron nào quyết định tính chất hóa học của một nguyên tố hóa học?
1.34 Cho biết cấu hình electron của nguyên tử một số nguyên tố sau:
a. 1s22s22p63s1 b. 1s22s22p63s23p5
c.1s22s22p2 d. 1s22s22p63s23p63d64s2
1. Hãy cho biết những nguyên tố nào là kim loại, phi kim?
2. Nguyên tố nào trong các nguyên tố trên thuộc họ s, p hay d?
3. Nguyên tố nào có thể nhận 1 electron trong các phản ứng hóa học?
1.35 Tổng số hạt proton, nơtron, electron trong nguyên tử là 28, trong đó số hạt không mang điện chiếm xấp xỉ 35% tổng số hạt. Tính số hạt mỗi loại và viết cấu hình electron của nguyên tử .
1.36 Biết khối lượng nguyên tử của một loại đồng vị của Fe là 8,96. 10 - 23 gam. Biết Fe có số hiệu nguyên tử Z = 26 . Tính số khối và số nơtron có trong hạt nhân nguyên tử của đồng vị trên.
1.37 a, Dựa vào đâu mà biết được rằng trong nguyên tử các electron được sắp xếp theo từng lớp ?
b, Electron ở lớp nào liên kết với hạt nhân chặt chẽ nhất? Kém nhất ?
1.38 Vỏ electron của một nguyên tử có 20 electron . Hỏi
a, Nguyên tử đó có bao nhiêu lớp electron ?
b, Lớp ngoài cùng có bao nhiêu electron ?
c, Đó là kim loại hay phi kim ?
1.39 Cấu hình electron của nguyên tử có ý nghĩa gì? Cho thí dụ.
1.40 Các nguyên tử A, B, C, D, E có số proton và số nơtron lần lượt như sau:
A: 28 proton và 31 nơtron.
B: 18 proton và 22 nơtron.
C: 28 proton và 34 nơtron.
D: 29 proton và 30 nơtron.
E: 26 proton và 30 nơtron.
Hỏi những nguyên tử nào là những đồng vị của cùng một nguyên tố và nguyên tố đó là nguyên tố gì? Những nguyên tử nào có cùng số khối?
1.41 Cho biết tên, kí hiệu, số hiệu nguyên tử của:
a) 2 nguyên tố có số electron ở lớp ngoài cùng tối đa.
b) 2 nguyên tố có 2 electron ở lớp ngoài cùng.
c) 2 nguyên tố có 7 electron ở lớp ngoài cùng.
d) 2 nguyên tố có 2 electron độc thân ở trạng thái cơ bản.
e) 2 nguyên tố họ d có hóa trị II và hóa trị III bền.
1.42 Viết cấu hình eletron đầy đủ cho các nguyên có lớp electron ngoài cùng là:
a) 2s1 b) 2s22p3 c) 2s22p6
d) 3s23p3 đ) 3s23p5 e) 3s23p6
1.43 a)Viết cấu hình electron của nguyên tử nhôm (Z =13). Để đạt được cấu hình electron của khí hiếm gần nhất trong bảng tuần hoàn nguyên tử nhôm nhường hay nhận bao nhiêu electron? Nhôm thể hiện tính chất kim loại hay phi kim?
b) Viết cấu hình electron của nguyên tử clo (Z =17). Để đạt được cấu hình electron của khí hiếm gần nhất trong bảng tuần hoàn, nguyên tử clo nhường hay nhận bao nhiêu electron? Clo thể hiện tính chất kim loại hay phi kim?
1.44 Cấu hình electron của nguyên tử lưu huỳnh là 1s22s22p63s23p4. Hỏi:
a) Nguyên tử lưu huỳnh có bao nhiêu electron ?
b) Số hiệu nguyên tử của lưu huỳnh là bao nhiêu?
c) Lớp nào có mức năng lượng cao nhất?
d) Có bao nhiều lớp, mỗi lớp có bao nhiêu electron?
e) Lưu huỳnh là kim loại hay phi kim? Vì sao?
1.45 Biết tổng số hạt p, n, e trong một nguyên tử là 155. Số hạt mang điện nhiều hơn số hạt không mang điện là 33 hạt. Tính số khối của nguyên tử.
D. BÀI TẬP TRẮC NGHIỆM
1.46 Cho những nguyên tử của các nguyên tố sau:
1 2 3 4
Những nguyên tử nào sau đây là đồng vị của nhau ?
A. 1 và 2 B. 2 và 3
C. 1, 2 và 3 D. Cả 1, 2, 3, 4
 1.47 :Nguyên tử nào trong hình vẽ dưới đây có khả năng nhận 3 electron trong các phản ứng hóa học?
1.47 :Nguyên tử nào trong hình vẽ dưới đây có khả năng nhận 3 electron trong các phản ứng hóa học?
1 2 3 4
A. 1 và 2 B.1 và 3
C. 3 và 4 D.1 và 4
1.48 Hình vẽ nào sau đây vi phạm nguyên lý Pauli khi điền electron vào AO?
a b c d
A. a B. b
C. a và b D.c và d
1.49 Cấu hình của nguyên tử sau biểu diễn bằng ô lượng tử. Thông tin nào không đúng khi nói về cấu hình đã cho?
1s2 2s2 2p3
A.Nguyên tử có 7 electron
B.Lớp ngoài cùng có 3 electron
C.Nguyên tử có 3 electron độc thân
D.Nguyên tử có 2 lớp electron
1.50 Khi phân tích một mẫu brom lỏng, người ta tìm được 3 giá trị khối lượng phân tử hơn kém nhau 2 đơn vị, điều đó chứng tỏ:
A. Có hiện tượng đồng vị
B. Có sự tồn tại của đồng phân
C. Brom có 3 đồng vị
D. Brom có 2 đồng vị
1.51 Phát biểu nào sau đây không đúng?
A. Các electron chuyển động xung quanh hạt nhân theo những hình tròn.
B. Các electron chuyển động xung quanh hạt nhân không theo quỹ đạo xác định nào.
C. Obitan là khu vực xung quanh hạt nhân mà tại đó xác suất có mặt của electron là lớn nhất.
D. Obitan của các phân lớp khác nhau có hình dạng khác nhau.
1.52 Cho các nguyên tử sau N (Z = 7), O (Z = 8), S (Z = 16), Cl (Z = 17). Trong số đó các nguyên tử có 2 electron độc thân ở trạng thái cơ bản là:
A. N và S B. S và Cl
C. O và S D. N và Cl
1.53 Ion A2+ có cấu hình electron phân lớp ngoài cùng là 3p6. Tổng số electron trong nguyên tử A là:
A. 18 B. 19 C. 20 D. 21
1.54 Cấu hình electron của ion nào sau đây khác cấu hình electron của khí hiếm ?
A. Na+ B. Cu2+ C. Cl- D. O2-
1.55 Các nguyên tử và ion : F-, Na+, Ne có đặc điểm nào chung ?
A. Có cùng số electron B. Có cùng số nơtron
C. Cùng số khối D. Cùng điện tích hạt nhân
1.56 Một nguyên tử có tổng cộng 7 electron ở các phân lớp p. Số proton của nguyên tử đó là :
A. 10 B. 11 C. 12 D. 13
1.57 Nguyên tử X có cấu hình electron là : 1s22s22p5. Ion mà X có thể tạo thành là :
A. X+ B. X2+ C. X- D. X2-
1.58 Biết 1 mol nguyên tử sắt có khối lượng bằng 56g, một nguyên tử sắt có 26 electron. Số hạt electron có trong 5,6g sắt là
A. 15,66.1024 B. 15,66.1021
C. 15,66.1022 D. 15,66.1023
1.59 Nguyên tử nào trong số các nguyên tử sau đây có 20 proton, 20 electron, 20 nơtron?
1.60 Trong nguyên tử cacbon, hai electron 2p được phân bố trên 2 obitan p khác nhau và được biểu diễn bằng hai mũi tên cùng chiều. Nguyên lí hay quy tắc được áp dụng ở đây là
A. nguyên lí Pauli B. quy tắc Hund
C. quy tắc Kletkopski D. cả A, B và C
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP
1.46. C | 1.47. D | 1.48. D | 1.49. B | 1.50. D |
1.51. A | 1.52. C | 1.53. C | 1.54. B | 1.55. A |
1.56. D | 1.57. C | 1.58. D | 1.59. C | 1.60. B |
1.1 Hướng dẫn :
Trong một thời kì dài, người ta không có đủ các thiết bị khoa học để kiểm chứng ý tưởng về nguyên tử. Sự phát triển của khoa học và kĩ thuật cuối thế kỉ XIX cho phép chế tạo được thiết bị có độ chân không cao (p = 0,001mmHg), có màn huỳnh quang để quan sát đường đi của các tia không nhìn thấy bằng mắt thường và nguồn điện có thế hiệu rất cao (15000V).
Thí nghiệm phát minh electron của Tom-xơn (1897)
 Tom-xơn đã cho phóng điện với thế hiệu 15000 vôn qua hai điện cực gắn vào hai đầu của một ống thủy tinh kín đã rút gần hết không khí, áp suất 0,001mmHg, thì thấy màn huỳnh quang lóe sáng. Màn huỳnh quang phát sáng do sự xuất hiện của các tia không nhìn thấy được đi từ cực âm sang cực dương, tia này được gọi là tia âm cực. Tia âm cực bị hút lệch về phía cực dương khi đặt ống thủy tinh trong một điện trường. Thí nghiệm này chứng tỏ nguyên tử có cấu tạo phức tạp. Một trong những thành phần cấu tạo của nguyên tử là các electron.
Tom-xơn đã cho phóng điện với thế hiệu 15000 vôn qua hai điện cực gắn vào hai đầu của một ống thủy tinh kín đã rút gần hết không khí, áp suất 0,001mmHg, thì thấy màn huỳnh quang lóe sáng. Màn huỳnh quang phát sáng do sự xuất hiện của các tia không nhìn thấy được đi từ cực âm sang cực dương, tia này được gọi là tia âm cực. Tia âm cực bị hút lệch về phía cực dương khi đặt ống thủy tinh trong một điện trường. Thí nghiệm này chứng tỏ nguyên tử có cấu tạo phức tạp. Một trong những thành phần cấu tạo của nguyên tử là các electron.
1.2 Hướng dẫn:
Ta có mNe = 1,66005.10-27. 20,179 = 33,498.10-27 kg.
1.3 Hướng dẫn :
Gọi nguyên tử khối của oxi là X, ta có :
( 2X + 12,011).27,3% = 12,011
Þ X = 15,99
1.4 Hướng dẫn: Theo đề bài :
MC = 11,9059.MH
1.5 Hướng dẫn:
Sau thí nghiệm tìm ra electron -loại hạt mang điện tích âm, bằng cách suy luận người ta biết rằng nguyên tử có các phần tử mang điện dương, bởi vì nguyên tử trung hòa điện. Tuy nhiên có một câu hỏi đặt ra là các phần tử mang điện dương phân bố như thế nào trong nguyên tử? Tom-xơn và những người ủng hộ ông cho rằng các phần tử mang điện dương phân tán đều trong toàn bộ thể tích nguyên tử. Trong khi đó Rơ-dơ-pho và các cộng sự muốn kiểm tra lại giả thuyết của Tom-xơn. Họ làm thí nghiệm để tìm hiểu sự phân bố các điện tích dương trong nguyên tử.
Thí nghiệm tìm ra hạt nhân nguyên tử của Rơ-dơ-pho (1911)
 Để kiểm tra giả thuyết của Tom-xơn, Rơ-dơ-pho đã dùng tia a bắn phá một lá vàng mỏng, xung quanh đặt màn huỳnh quang để quan sát sự chuyển động của các hạt a. Kết quả là hầu hết các hạt a đi thẳng, một số ít bị lệch hướng, một số ít hơn bị bật ngược trở lại. Điều này cho phép kết luận giả thuyết của Tom-xơn là sai. Phần mang điện tích dương tập trung ở hạt nhân của nguyên tử, kích thước rất nhỏ bé so với kích thước nguyên tử. Nguyên tử có cấu tạo rỗng.
Để kiểm tra giả thuyết của Tom-xơn, Rơ-dơ-pho đã dùng tia a bắn phá một lá vàng mỏng, xung quanh đặt màn huỳnh quang để quan sát sự chuyển động của các hạt a. Kết quả là hầu hết các hạt a đi thẳng, một số ít bị lệch hướng, một số ít hơn bị bật ngược trở lại. Điều này cho phép kết luận giả thuyết của Tom-xơn là sai. Phần mang điện tích dương tập trung ở hạt nhân của nguyên tử, kích thước rất nhỏ bé so với kích thước nguyên tử. Nguyên tử có cấu tạo rỗng.
1.6 Hướng dẫn:
Số đơn vị điện tích hạt nhân, số proton, số nơtron và số electron của các nguyên tử:
Số p = số e = Z = 19 ; N = 20
Số p = số e = Z = 20 ; N = 20
Số p = số e = Z = 90 ; N = 144
Số p = số e = Z = 1 ; N = 1
Số p = số e = Z = 2 ; N = 2
Số p = số e = Z = 6 ; N = 6
Số p = số e = Z = 8 ; N = 8
Số p = số e = Z = 26 ; N =30
Số p = số e = Z = 15; N = 17
1.7 Hướng dẫn: Cách tính số khối của hạt nhân :
Số khối hạt nhân (kí hiệu A) bằng tổng số proton (p) và số nơtron (n).
A = Z + N
Nói số khối bằng nguyên tử khối là sai, vì số khối là tổng số proton và notron trong hạt nhân, trong khi nguyên tử khối là khối lượng tương đối của nguyên tử. Nguyên tử khối cho biết khối lượng của một nguyên tử nặng gấp bao nhiêu lần đơn vị khối lượng nguyên tử.
Do khối lượng của mỗi hạt proton và nơtron ~1u, cho nên trong các tính toán không cần độ chính xác cao, coi số khối bằng nguyên tử khối.
1.8 Hướng dẫn: Ta có AAg = 107,02. mà
mà  =
=  = 1,0079
= 1,0079
AAg = 107,02 . 1,0079 = 107,865
1.9 Hướng dẫn:
a) Nguyên tử khối trung bình của hiđro và clo là:
b). Có bốn loại phân tử HCl khác nhau tạo nên từ hai loại đồng vị của hai nguyên tử hiđro và clo.
c) Phân tử khối lần lượt: 36 38 37 39
1.10 Hướng dẫn:
Gọi tỉ lệ % số nguyên tử của đồng vị  là x , % đồng vị
là x , % đồng vị  là 100 - x
là 100 - x
Þ 63x + 6500 - 65x = 6354,6
Þ x = 72,7
Vậy % số nguyên tử của đồng vị  là 72,7%.
là 72,7%.
1.11 Hướng dẫn:
a) Công thức phân tử : H2 ; HD ; D2
b) Phân tử khối : 2 3 4
c) Đặt a là thành phần % của H và 100 - a là thành phần % của D về khối lượng.
% H = 88% ; %D = 12%
1.12 Hướng dẫn:
Không thể mô tả được sự chuyển động của electron trong nguyên tử bằng các quỹ đạo chuyển động. Bởi vì trong nguyên tử, các electron chuyển động rất nhanh xung quanh hạt nhân không theo một quỹ đạo xác định nào. Người ta chỉ nói đến khả năng quan sát electron tại một thời điểm nào đó trong không gian của nguyên tử.
1.13 Hướng dẫn:
Theo lý thuyết hiện đại trạng thái chuyển động của electron trong nguyên tử được mô tả bằng hình ảnh được gọi là obitan nguyên tử.
1.14 Hướng dẫn:
Hình dạng của các obitan nguyên tử s và p :
+ Obitan s : Có dạng hình cầu, tâm là hạt nhân nguyên tử. Obitan s không có sự định hướng trong không gian của nguyên tử.
+ Obitan p : Gồm ba obitan : px, py và pz có dạng hình số 8 nổi. Mỗi obitan có sự định hướng khác nhau trong không gian. Chẳng hạn : Obitan px định hướng theo trục x, py định hướng theo trục y,...
Gọi số khối của đồng vị A của nguyên tố agon là X
Þ XA = 40
1.16 Hướng dẫn:
Ta có
a) Nguyên tử khối trung bình của Mg là
b) Giả sử trong hỗn hợp nói trên có 50 nguyên tử  , thì số nguyên tử tương ứng của 2 đồng vị còn lại là:
, thì số nguyên tử tương ứng của 2 đồng vị còn lại là:
Số nguyên tử  =
=  x78,6 = 389 (nguyên tử).
x78,6 = 389 (nguyên tử).
Số nguyên tử  =
=  x 11,3 = 56 (nguyên tử).
x 11,3 = 56 (nguyên tử).
1.17 Hướng dẫn:
Ta có
n : 1 2 3 4
Tên lớp : K L M N
Lớp K có một phân lớp 1s
Lớp L có hai phân lớp 2s, 2p
Lớp M có ba phân lớp 3s, 3p, 3d
Lớp N có bốn phân lớp 4s, 4p, 4d, 4f
1.18 Hướng dẫn:
+) Lớp N có : - 4 phân lớp 4s, 4p, 4d, 4f
+) Lớp M có : - 3 phân lớp 3s, 3p, 3d
1.19 Hướng dẫn:
Vẽ hình dạng các obitan 1s, 2s và các obitan 2px, 2py, 2pz
1.20 Hướng dẫn:
Sự phân bố electron trong nguyên tử tuân theo nguyên lý Pau-li, nguyên lý vững bền và quy tắc Hun.
- ¯
Nguyên lý Pau-li : Trên một obitan chỉ có thể có nhiều nhất là 2 electron và 2 electron này chuyển động tự quay khác chiều nhau xung quanh trục riêng của mỗi electron.
Thí dụ : Nguyên tố He có Z = 2
1s2
- Nguyên lý vững bền : ở trạng thái cơ bản trong nguyên tử các electron chiếm lần lượt những obitan có mức năng lượng từ thấp đến cao.
 Thí dụ : Nguyên tử B (Z = 5) :
Thí dụ : Nguyên tử B (Z = 5) :
1s2 2s2 2p1
 - Quy tắc Hun : Trong cùng 1 phân lớp các electron sẽ phân bố trên các obitan sao cho có số electron độc thân là tối đa và các electron này phải có chiều tự quay giống nhau.
- Quy tắc Hun : Trong cùng 1 phân lớp các electron sẽ phân bố trên các obitan sao cho có số electron độc thân là tối đa và các electron này phải có chiều tự quay giống nhau.
Thí dụ : Nguyên tử C (Z = 6)
1s2 2s2 2p2
1.21 Hướng dẫn:
 Theo nguyên tắc Hun cho nên trong sơ đồ phân bố electron của nguyên tử cacbon ( C : 1s2 2s2 2p2) phân lớp 2p được biểu diễn :
Theo nguyên tắc Hun cho nên trong sơ đồ phân bố electron của nguyên tử cacbon ( C : 1s2 2s2 2p2) phân lớp 2p được biểu diễn :
1.22 Hướng dẫn:
Cấu hình electron của các nguyên tố có :
- Z = 20 : 1s2 2s2 2p6 3s2 3p6 4s2
- Z = 21 : 1s2 2s2 2p6 3s2 3p6 3d14s2
- Z = 22 : 1s2 2s2 2p6 3s2 3p6 3d2 4s2
- Z = 24 : 1s2 2s2 2p6 3s2 3p6 3d5 4s1
- Z = 29 : 1s2 2s2 2p6 3s2 3p6 3d10 4s1
Nhận xét :
+ Cấu hình Z =20 khác với các cấu hình còn lại ở chỗ không có phân lớp 3d.
+ Cấu hình Z =24 và Z = 29 có 1 electron ở phân lớp 4s.
1.23 Hướng dẫn:
Số e ở lớp ngoài cùng của nguyên tử các nguyên tố:
H : có 1e Ca : có 2e O : có 6e
Li : có 1e Mg: có 2e
Na: có 1e C : có 4e
K : có 1e Si : có 4e
1.24 Hướng dẫn:
K (Z= 19) : 1s22s22p63s23p64s1
Ca (Z = 20) : 1s22s22p63s23p64s2
Vậy sự phân bố electron trên các obitan nguyên tử của các nguyên tố K và Ca có đặc điểm là có 1 hay 2 electron ở lớp ngoài cùng. Những electron này có liên kết yếu với hạt nhân, do đó trong các phản ứng hóa học, K và Ca dễ nhường đi để trở thành các ion dương bền vững.
1.25 Hướng dẫn:
Cấu hình e của F và Cl là :
F (Z = 9) 1s22s22p5
Cl (Z = 17) : 1s22s22p63s23p5
Đặc điểm : lớp electron ngoài cùng có 7e, những electron này liên kết chặt chẽ với hạt nhân, do đó trong các phản ứng hóa học, F và Cl có xu hướng nhận thêm 1 electron để đạt cấu hình bão hòa, bền vững như khí hiếm đứng sau chúng.
1.26 Hướng dẫn:
Trật tự theo dãy đã cho là sai, sửa lại là :
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 5d 6p 7s 5f 6d ...
Sai ở vị trí của AO 3d và AO 4s.
1.27 Hướng dẫn:
Cấu hình e nguyên tử của các nguyên tố có :
Z = 15 : 1s2 2s2 2p6 3s2 3p3
Z = 17 : 1s2 2s2 2p6 3s2 3p5
Z = 20 : 1s2 2s2 2p6 3s2 3p6 4s2
Z = 21 : 1s2 2s2 2p6 3s2 3p6 3d1 4s2
Z = 31 : 1s2 2s2 2p6 3s2 3p63d104s2 4p1
1.28 Hướng dẫn:
Fe Z = 26 : 1s2 2s2 2p6 3s2 3p63d6 4s2
Fe2+ Z = 26 : 1s2 2s2 2p6 3s2 3p63d6
Fe3+ Z = 26 : 1s2 2s2 2p6 3s2 3p63d5
1.29 Hướng dẫn:
b) ![]()
c) ![]()
d) ![]()
1.30 Hướng dẫn:
a) ![]()
b) ![]()
F. MỘT SỐ THÔNG TIN BỔ SUNG
Năng lượng hạt nhân có nên được sử dụng ở Việt Nam?
1. Những ý kiến ủng hộ việc xây dựng nhà máy điện hạt nhân
Để duy trì một tốc độ tăng trưởng kinh tế cao thứ hai châu Á, khoảng 7,5 -8% một năm như hiện nay, theo nghiên cứu của tổng công ty điện lực Việt Nam (EVN), tăng trưởng nguồn điện phải đạt trung bình 15% một năm. Một số nước phát triển như Pháp và Hàn Quốc có tỷ trọng điện hạt nhân trong tổng nguồn năng lượng rất cao (trên 60%).
Các nguồn điện chủ yếu hiện nay của nước ta là thủy điện và nhiệt điện. Thủy điện có ưu điểm tận dụng tài nguyên nước, nhưng nguồn điện lại phụ thuộc nhiều vào nguồn nước. Vào những tháng 4, 5 hàng năm, nguồn nước cho thủy điện giảm làm nguồn cung cấp điện thiếu hụt dẫn đến phải cắt điện luân phiên, ảnh hưởng không nhỏ đến sản xuất và kinh doanh. Nhiệt điện với các nhiên liệu như than đá (Quảng Ninh), khí đốt ở Bà Rịa-Vũng Tàu đang góp phần làm tăng mức độ ô nhiễm môi trường ở Việt Nam.
Để giải quyết nạn thiếu điện có nhiều phương án được lựa chọn, trong đó có điện hạt nhân. Theo EVN đến năm 2017 nước ta sẽ có nhà máy điện hạt nhân đầu tiên.
Nhà máy điện hạt nhân sẽ cung cấp một nguồn điện ổn định, không làm tăng khí thải CO2 như việc đốt các nhiên liệu hóa thạch như than đá, dầu mỏ.
Nguồn điện hạt nhân sẽ hỗ trợ các nhà máy thủy điện trong mùa khô.
Nhà máy điện hạt nhân còn là biểu tượng của một nền khoa học, công nghệ tiên tiến.
Các nước có nền công nghiệp điện hạt nhân phát triển như Nga, Pháp, Hàn Quốc đang giới thiệu cho Việt Nam các thiết bị điện hạt nhân của họ. Tuy nhiên, cho đến nay chưa có một sự lựa chọn nhà thầu chính thức nào từ phía Việt Nam.
2. Những ý kiến phản đối việc xây dựng nhà máy điện hạt nhân
Thứ nhất là năng lượng hạt nhân có độ rủi ro cao. Bài học về vụ nổ lò phản ứng hạt nhân ở Trecnobyl 20 năm trước, với một sức tàn phá tương đương 400 quả bom nguyên tử mà Mỹ ném xuống thành phố Hirosima, làm cho một khu vực bán kính 30km đến nay hoàn toàn không người ở vì độ nhiễm xạ cao vẫn còn giá trị.
Thứ hai là công nghệ điện hạt nhân phải nhập với giá thành rất cao. Nguyên liệu hoạt động của nhà máy điện hạt nhân ngày càng hiếm và phải nhập khẩu với giá thành ngày càng cao, do đó điện hạt nhân kém tính cạnh tranh so với các nguồn năng lượng khác.
Thứ ba là vấn đề xử lí rác thải hạt nhân. Đây là một vấn đề rất phức tạp, ngay cả với những quốc gia có nền khoa học và công nghệ tiên tiến trên thế giới.
Thứ tư là nhu cầu nước làm mát của nhà máy điện hạt nhân rất lớn. Trong khi các địa điểm dự định xây dựng nhà máy điện hạt nhân của nước ta lại đặt ở những vùng rất hiếm nước.
Thứ năm là nguồn nhân lực để vận hành nhà máy điện hạt nhân đòi hỏi một đội ngũ có tính kỉ luật và kỹ thuật rất cao, là điều không thực hiện được một cách dễ dàng ở nước ta trong giai đoạn trước mắt.
Chính vì những lí do trên cho nên nhiều nước phát triển trên thế giới như Đức, Thụy điển, Italy ... đang có kế hoạch loại bỏ các nhà máy điện hạt nhân vào năm 2020.
Những lí do vừa đề cập trên đây đòi hỏi sự cân nhắc kĩ lưỡng của chính phủ trước khi quyết định xây dựng nhà máy điện hạt nhân đầu tiên của Việt Nam.
3. Còn bạn, bạn theo quan điểm nào?
Chương 2
BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
VÀ ĐỊNH LUẬT TUẦN HOÀN
![]()
A. TÓM TẮT LÍ THUYẾT
1. Bảng tuần hoàn các nguyên tố hóa học
a) Nguyên tắc sắp xếp:
- Các nguyên tố được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
- Các nguyên tố có cùng số lớp electron được xếp thành một hàng.
- Các nguyên tố có số electron hóa trị trong nguyên tử như nhau được xếp thành một cột.
b) Cấu tạo của bảng tuần hoàn
Bảng tuần hoàn các nguyên tố hóa học là sự thể hiện nội dung của định luật tuần hoàn. Trong hơn 100 năm tồn tại và phát triển, đã có khoảng nhiều kiểu bảng tuần hoàn khác nhau. Dạng được sử dụng trong sách giáo khoa hóa học phổ thông hiện nay là bảng tuần hoàn dạng dài, có cấu tạo như sau:
Ô : Số thứ tự của ô bằng số hiệu nguyên tử và bằng số đơn vị điện tích hạt nhân, bằng tổng số electron của nguyên tử..
Chu kì :
Có 7 chu kì, số thứ tự của chu kì bằng số lớp electron của nguyên tử gồm :
+ Chu kì nhỏ là các chu kì 1, 2, 3 chỉ gồm các nguyên tố s và các nguyên tố p. Mỗi chu kì nhỏ gồm 8 nguyên tố, trừ chu kì 1 chỉ có hai nguyên tố.
+ Chu kì lớn là các chu kì 4, 5, 6 ,7 gồm các nguyên tố s, p, d và f. Chu kì 4 và chu kì 5 mỗi chu kì có 18 nguyên tố. Chu kì 6 có 32 nguyên tố. Theo quy luật, chu kì 7 cũng phải có 32 nguyên tố, tuy nhiên chu kì 7 mới phát hiện được 24 nguyên tố hóa học. Lí do là các nguyên tố có hạt nhân càng nặng càng kém bền, chúng có "đời sống" rất ngắn ngủi.
Nhóm: Có 8 nhóm, số thứ tự của nhóm bằng số electron hóa trị.
+ Nhóm A: Số thứ tự của nhóm bằng số electron hóa trị, nhóm A gồm các nguyên tố s và p. Nhóm A còn được gọi là các nguyên tố thuộc phân nhóm chính.
+ Nhóm B: Số thứ tự của nhóm B bằng số electron hóa trị, nhóm B gồm các nguyên tố d và f. Nhóm B còn được gọi là các nguyên tố thuộc phân nhóm phụ.
c) Những tính chất biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân
- Bán kính nguyên tử:
+ Trong chu kì, theo chiều tăng của điện tích hạt nhân, bán kính nguyên tử giảm dần, vì số electron ngoài cùng tăng dần trong khi số lớp electron không thay đổi.
+ Trong nhóm A, theo chiều tăng của điện tích hạt nhân, bán kính nguyên tử tăng dần, do số lớp electron tăng dần.
- Năng lượng ion hoá:
+ Trong chu kì, theo chiều tăng của điện tích hạt nhân, năng lượng ion hóa của nguyên tử tăng dần, vì số electron ngoài cùng tăng dần trong khi số lớp electron không thay đổi.
+ Trong nhóm A, theo chiều tăng của điện tích hạt nhân, năng lượng ion hóa của nguyên tử giảm dần vì electron ở xa hạt nhân hơn, liên kết với hạt nhân yếu hơn.
- Độ âm điện: Độ âm điện là một khái niệm mang tính chất kinh nghiệm và thay đổi theo thang đo và chỉ có ý nghĩa tương đối. Độ âm điện đặc trưng cho khả năng hút electron về phía mình của nguyên tử trong phân tử.
+ Trong chu kì, theo chiều tăng của điện tích hạt nhân, độ âm điện của nguyên tử tăng dần.
+ Trong nhóm A, theo chiều tăng của điện tích hạt nhân, độ âm điện của nguyên tử giảm dần.
- Tính kim loại - phi kim:
+ Trong chu kì, theo chiều tăng của điện tích hạt nhân, tính kim loại giảm dần và tính phi kim tăng dần.
+ Trong nhóm A, theo chiều tăng của điện tích hạt nhân, tính kim loại tăng dần và tính phi kim giảm dần.
Tính axit - bazơ của oxit và hiđroxit:
+ Trong chu kì, theo chiều tăng của điện tích hạt nhân, tính bazơ giảm dần và tính axit tăng dần.
+ Trong nhóm A, theo chiều tăng của điện tích hạt nhân, tính bazơ tăng dần và tính axit dần giảm (trừ nhóm VII).
2. Định luật tuần hoàn
Tính chất của các nguyên tố và đơn chất cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử.
3. Ý nghĩa của định luật tuần hoàn
- Biết vị trí của một nguyên tố trong bảng tuần hoàn, có thể suy ra cấu tạo nguyên tử của nguyên tố đó và ngược lại.

- Biết vị trí của một nguyên tố trong bảng tuần hoàn, có thể suy ra tính chất hóa học cơ bản của nó.

- So sánh tính chất hóa học của một nguyên tố với các nguyên tố lân cận.
B. BÀI TẬP CÓ LỜI GIẢI
2.1 Xác định vị trí (số thứ tự, chu kỳ, nhóm, phân nhóm) các nguyên tố sau đây trong bảng tuần hoàn, cho biết cấu hình electron của nguyên tử các nguyên tố đó như sau:
1. 1s2 2s2 2p6 3s23p6 4s2 2. 1s2 2s2 2p6 3s2 3p6 3d5 4s2
2.2 Ion M3+ có cấu hình electron lớp ngoài cùng là 3s23p63d5.
1. Xác định vị trí (số thứ tự, chu kỳ, nhóm) của M trong bảng tuần hoàn. Cho biết M là kim loại gì?
2. Trong điều kiện không có không khí, cho M cháy trong khí Cl2 thu được một chất A và nung hỗn hợp bột (M và S) được một hợp chất B. Bằng các phản ứng hóa học, hãy nhận biết thành phần và hóa trị của các nguyên tố trong A và B.
2.3 Giả sử nguyên tố M ở ô số 19 trong bảng tuần hoàn chưa được tìm ra và ô này vẫn còn được bỏ trống. Hãy dự đoán những đặc điểm sau về nguyên tố đó:
1. Tính chất đặc trưng.
2. Công thức oxit. Oxit đó là oxit axit hay oxit bazơ?
2.4 Nguyên tử của nguyên tố R có phân mức năng lượng cao nhất là 4s2.
1. Viết cấu hình electron của nguyên tử R
2. Vị trí trong bảng tuần hoàn.
3. Viết các phương trình hóa học xảy ra khi cho:
R + H2O![]() hiđroxit + H2
hiđroxit + H2
Oxit của R + H2O ![]()
Muối cacbonat của R + HCl![]()
Hiđroxit của R + Na2CO3![]()
2.5 Một hợp chất có công thức là MAx, trong đó M chiếm 46,67% về khối lượng. M là kim loại, A là phi kim ở chu kì 3. Trong hạt nhân của M có n - p = 4, trong hạt nhân của A có n' = p'. Tổng số proton trong MAx là 58.
1. Xác định tên nguyên tố, số khối của M, số thứ tự A trong bảng tuần hoàn.
2. Hoàn thành các phương trình hóa học:
a. MXx + O2 ![]() M2O3 + XO2
M2O3 + XO2
b. MXx + HNO3 ![]() M(NO3)3 + H2XO4 + NO2 + H2O
M(NO3)3 + H2XO4 + NO2 + H2O
2.6 M là kim loại thuộc nhóm IIA.Hòa tan hết 10,8 gam hỗn hợp gồm kim loại M và muối cacbonat của nó trong dung dịch HCl, thu được 4,48 lit hỗn hợp khí A (đktc). Tỉ khối của A so với khí hiđro là 11,5.
1. Tìm kim loại M
2. Tính % thể tích các khí trong A.
2.7 X, Y là hai kim loại có electron cuối cùng là 3p1 và 3d6.
1. Dựa vào bảng tuần hoàn, hãy xác định tên hai kim loại X, Y.
2. Hòa tan hết 8,3 gam hỗn hợp X, Y vào dung dịch HCl 0,5M (vừa đủ), ta thấy khối lượng dung dịch sau phản ứng tăng thêm 7,8 gam. Tính khối lượng mỗi kim loại và thể tích dung dịch HCl đã dùng.
2.8 Hòa tan hết a gam oxit kim loại M (thuộc nhóm IIA) bằng một lượng vừa đủ dung dịch H2SO4 17,5% thu được dung dịch muối có nồng độ 20%.
Xác định công thức oxit kim loại M.
2.9 A, B là 2 kim loại nằm ở 2 chu kỳ liên tiếp thuộc nhóm IIA. Cho 4,4 gam một hỗn hợp gồm A và B tác dụng với dung dịch HCl 1M (dư) thu được 3,36 lit khí (đktc).
1. Viết các phương trình phản ứng và xác định tên 2 kim loại.
2. Tính thể tích dung dịch HCl đã dùng, biết rằng HCl dùng dư 25% so với lượng cần thiết.
2.10 Cho 0,85 gam hai kim loại thuộc hai chu kỳ kế tiếp trong nhóm IA vào cốc chứa 49,18 gam H2O thu được dung dịch A và khí B. Để trung hòa dung dịch A cần 30 ml dung dịch HCl 1M.
a. Xác định hai kim loại
b. Tính nồng độ % của các chất trong dung dịch A.
2.11 Nguyên tố R có hóa trị cao nhất trong oxit gấp 3 lần hóa trị trong hợp chất với hiđro.
a. Hãy cho biết hóa trị cao nhất của R trong oxit.
b. Trong hợp chất của R với hiđro có tỉ lệ khối lượng: ![]() .
.
Không dùng bảng tuần hoàn, cho biết kí hiệu của nguyên tử R.
2.12 Nguyên tố R ở chu kì 3, nhóm VA trong bảng tuần hoàn. Không sử dụng bảng tuần hoàn, hãy cho biết:
a. Cấu hình electron của R.
b. Trong oxit cao nhất của R thì R chiếm 43,66% khối lượng. Tính số lượng mỗi loại hạt của nguyên tử R.
2.13 A và B là hai nguyên tố ở cùng một nhóm và thuộc hai chu kì liên tiếp trong bảng tuần hoàn. Tổng số proton trong hai hạt nhân nguyên tử của A và B bằng 32.
Hãy viết cấu hình electron của A , B và của các ion mà A và B có thể tạo thành.
2.14 Hai nguyên tố A và B ở hai nhóm A liên tiếp trong bảng tuần hoàn, B thuộc nhóm VA, ở trạng thái đơn chất A, B không phản ứng với nhau. Tổng số proton trong hạt nhân nguyên tử của A và B là 23.
1. Viết cấu hình electron nguyên tử của A, B.
2. Từ các đơn chất A, B và các hóa chất cần thiết, hãy viết các phương trình hóa học (ghi rõ điều kiện) điều chế hai axit trong đó A và B có số oxi hóa cao nhất.
2.15 Cho biết tổng số electron trong anion ![]() là 42. Trong các hạt nhân A và B đều có số proton bằng số nơtron.
là 42. Trong các hạt nhân A và B đều có số proton bằng số nơtron.
1. Tìm số khối của A và B
2. Cho biết vị trí của A, B trong bảng tuần hoàn.
2.16 Tổng số hạt proton, nơtron, electron của nguyên tử một nguyên tố R nhóm VIIA là 28.
1. Tính số khối.
2. Viết ký hiệu nguyên tử nguyên tố đó.
2.17 Một hợp chất ion được cấu tạo từ M+ và X2-. Trong phân tử M2X có tổng số hạt proton, nơtron, electron là 140 hạt. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của ion M+ lớn hơn số khối của ion X2- là 23. Tổng số hạt proton, nơtron, electron trong ion M+ nhiều hơn trong ion X2- là 31.
1. Viết cấu hình electron của M và X.
2. Xác định vị trí của M và của X trong bảng tuần hoàn.
2.18 Khi biết được số thứ tự Z của một nguyên tố trong bảng tuần hoàn, ta có thể biết được các thông tin sau đây không, giải thích ngắn gọn:
1. Cấu hình electron 4. Tính chất cơ bản
2. Số khối 5. Hóa trị cao nhất trong oxit
3. Kí hiệu nguyên tử 6. Hóa trị trong hợp chất với hiđro
2.19 Khi biết cấu hình lớp electron ngoài cùng của nguyên tử một nguyên tố nhóm A, ta có thể biết được các thông tin sau đây không?
1. Tính chất hóa học cơ bản 2. Cấu hình electron
3. Vị trí nguyên tố trong bảng tuần hoàn 4. Công thức oxit cao nhất
5. Kí hiệu nguyên tử 6. Công thức hợp chất với hiđro
Giải thích ngắn gọn các câu trả lời.
2.20 Một số đặc điểm của các nguyên tố kim loại kiềm được trình bày ở bảng sau:
Nguyên tố | Li | Na | K | Rb | Cs | |
Cấu hình electron | [He]2s1 | [Ne]3s1 | [Ar]4s1 | [Kr]5s1 | [Xe]6s1 | |
Bán kính nguyên tử (nm) | 0,155 | 0,189 | 0,236 | 0,248 | 0,268 | |
Năng lượng ion hóa, kJ/mol | I1 | 520 | 496 | 419 | 403 | 376 |
I2 | 7295 | 4565 | 3069 | 2644 | 2258 | |
1. Giải thích sự biến đổi năng lượng ion hóa thứ nhất? Tại sao năng lượng ion hóa thứ hai lớn hơn rất nhiều so với năng lượng ion hóa thứ nhất?
2. Tại sao trong các hợp chất, số oxi hóa của các kim loại kiềm luôn là +1, chúng có thể tạo ra số oxi hóa cao hơn hay không ?
2.21 Tổng số hạt proton, nơtron, electron trong hai nguyên tử kim loại A và B là 142, trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 42. Số hạt mang điện của nguyên tử B nhiều hơn của nguyên tử A là 12.
a. Xác định 2 kim loại A và B. Cho biết số hiệu nguyên tử của một số nguyên tố: Na (Z = 11), Mg (Z= 12), Al (Z =13), K (Z = 19), Ca (Z = 20), Fe (Z = 26), Cu (Z = 29), Zn (Z = 30).
b. Viết phương trình phản ứng điều chế A từ muối cacbonat của A và điều chế B từ một oxit của B.
(Trích Đề thi ĐH - CĐ khối B, năm 2003)
2.22 Cho 10 gam kim loại M (thuộc nhóm IIA) tác dụng với nước, thu được 6,11 lit khí hiđro (đo ở 25oC và 1 atm).
a. Hãy xác định tên của kim loại M đã dùng.
b. Cho 4 gam kim loại M vào cốc đựng 2,5lit dung dịch HCl 0,06M thu được dung dịch B.
Tính nồng độ mol/l các chất trong cốc sau phản ứng. Coi thể tích dung dịch trong cốc vẫn là 2,5 l.
2.23 Một hợp chất có công thức XY2 trong đó X chiếm 50% về khối lượng. Trong hạt nhân của X và Y đều có số proton bằng số nơtron. Tổng số proton trong phân tử XY2 là 32.
a. Viết cấu hình electron của X và Y.
b. Xác định vị trí của X và Y trong bảng tuần hoàn.
2.24 Cho biết cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố (thuộc chu kỳ 3) A, M, X lần lượt là ns1, ns2np1, ns2np5.
1. Xác định vị trí của A, M, X trong bảng tuần hoàn và cho biết tên của chúng.
2. Hoàn thành các phương trình hóa học theo sơ đồ sau:
- A(OH)m + MXy ![]() A1
A1![]() + ...
+ ...
- A1![]() + A(OH)m
+ A(OH)m ![]() A2 (tan) + ...
A2 (tan) + ...
- A2 + HX + H2O ![]() A1
A1![]() + ...
+ ...
- A1![]() + HX
+ HX ![]() A3 (tan) + ...
A3 (tan) + ...
Trong đó M, A, X là các nguyên tố tìm thấy ở câu 1.
2.25 Có 5,56 gam hỗn hợp A gồm Fe và kim loại M (hóa trị n). Chia A làm hai phần bằng nhau:
Phần 1: Hòa tan hết trong dung dịch HCl được 1,568 lit khí H2.
Phần 2: Hòa tan hết trong dung dịch H2SO4 đặc nóng thu được 2,016 lit khí SO2.
Viết các phương trình phản ứng và xác định tên kim loại M. Các khí đo ở đktc.
2.26 R là kim loại hóa trị II. Đem hòa tan 2 gam oxit của kim loại này vào 48 gam dung dịch H2SO4 6,125% loãng thu được dung dịch A trong đó nồng độ H2SO4 chỉ còn 0,98%.
1. Viết phương trình hóa học và xác định R. Biết RSO4 là muối tan.
2. Tính thể tích dung dịch NaOH 8% (d =1,05 g/ml) cần cho vào A để thu được lượng kết tủa lớn nhất.
2.27 M là kim loại hóa trị II. Hòa tan m gam M vào 200 gam dung dịch H2SO4 loãng, vừa đủ thì thu được dung dịch A và 0,672 lit khí (ở 54,60C và 2 atm). Chia A thành 2 phần bằng nhau:
Phần 1: cho tác dụng với dung dịch NaOH dư, lọc kết tủa đem nung đến khối lượng không đổi thu được 1 gam chất rắn.
Xác định kim loại M và tính nồng độ % dung dịch axit đã dùng.
Phần 2: làm bay hơi nước thu được 6,15 gam muối ngậm nước dạng MSO4.nH2O. Xác định công thức muối ngậm nước.
2.28 Hòa tan 16,2 gam kim loại M (nhóm IIIA) vào 5 lit dung dịch HNO3 0,5M (d = 1,25 g/ml). Sau khi kết thúc phản ứng thu được 5,6 lit hỗn hợp khí NO và N2 (đktc). Tỉ khối của hỗn hợp khí này so với hiđro là 14,4.
1. Xác định kim loại R.
2. Tính nồng độ % của dung dịch HNO3 trong dung dịch sau phản ứng.
2.29 Cấu tạo các lớp electron của nguyên tử các nguyên tố A, B, C, D, E như sau:
A: 2/2 B: 2/8/8/2 C: 2/7 D: 2/8/7 E: 2
1. Xác định vị trí của các nguyên tố trong bảng tuần hoàn.
2. Nguyên tố nào có tính kim loại mạnh nhất? Phi kim mạnh nhất? Nguyên tố nào kém hoạt động nhất? Giải thích?
2.30 Hòa tan hết 46 gam hỗn hợp gồm Ba và hai kim loại kiềm A, B thuộc hai chu kì kế tiếp vào nước, thu được dung dịch D và 11,2 lit khí đo ở đktc.
Nếu thêm 0,18 mol Na2SO4 vào dung dịch D thì dung dịch sau phản ứng vẫn chưa kết tủa hết bari. Nếu thêm 0,21 mol Na2SO4 vào dung dịch D thì dung dịch sau phản ứng còn dư Na2SO4.
Xác định tên hai kim loại kiềm.
Cho: Ba = 137, Li =7, Na = 23, K =39, Rb = 85, Cs = 133.
C. BÀI TẬP TỰ LUYỆN
2.31 Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kì trong bảng tuần hoàn, có tổng điện tích hạt nhân là 25.
1. Xác định vị trí của A, B trong bảng tuần hoàn.
2. So sánh tính chất hóa học của A và B; tính bazơ của oxit tạo thành từ A và B.
2.32 Hãy giải thích tại sao:
1. Trong một chu kì, độ âm điện tăng dần theo chiều từ trái sang phải; còn trong một nhóm, độ âm điện giảm dần theo chiều từ trên xuống dưới.
2. Trong một chu kì, năng lượng ion hóa tăng dần theo chiều từ trái sang phải; còn trong một nhóm, năng lượng ion hóa giảm dần theo chiều từ trên xuống dưới.
3. Trong một chu kì, tính phi kim tăng dần, tính kim loại giảm dần theo chiều tăng của điện tích hạt nhân.
2.33 Cho biết bán kính nguyên tử các nguyên tố sau (tính theo Å, 1Å = 10-10 m).
Nguyên tố | Na | Mg | Al | Si | P | S | Cl |
r (Å) | 1,86 | 1,60 | 1,43 | 1,17 | 1,10 | 1,04 | 0,99 |
Nguyên tố | Li | Na | K | Rb | Cs | ||
r (Å) | 1,52 | 1,86 | 2,31 | 2,44 | 2,62 |
Nhận xét sự thay đổi bán kính của các nguyên tử trên có tuân theo quy luật nào hay không? Nếu có, hãy giải thích tại sao?
2.34 X là nguyên tố thuộc chu kì 3, X tạo với hiđro một hợp chất khí có công thức H2X, trong đó X có số oxi hóa thấp nhất.
1. Xác định vị trí của X trong bảng tuần hoàn.
2. Viết phương trình phản ứng khi lần lượt cho H2X tác dụng với nước Cl2, dung dịch FeCl3, dung dịch CuSO4.
2.35 R là một nguyên tố phi kim. Tổng đại số số oxi hóa dương cao nhất với 2 lần số oxi hóa âm thấp nhất của R là +2. Tổng số proton và nơtron của R nhỏ hơn 34.
1. Xác định R
2. X là hợp chất khí của R với hiđro, Y là oxit của R có chứa 50% oxi về khối lượng. Xác định công thức phân tử của X và Y.
2.36 Một dung dịch nước có chứa 35 gam một hỗn hợp muối cacbonat của hai kim loại kiềm thuộc hai chu kì liên tiếp. Thêm từ từ và khuấy đều dung dịch HCl 0,5M vào dung dịch trên. Khi phản ứng xong, thu được 2,24 lit khí CO2 ở đktc và một dung dịch A. Thêm một lượng nước vôi trong dư vào dung dịch A, thu được 20 gam kết tủa.
1. Xác định các kim loại kiềm.
2. Tính khối lượng của mỗi muối trong hỗn hợp đầu.
2.37 A và B là hai kim loại thuộc nhóm IIA. Hòa tan hoàn toàn 15,05 gam hỗn hợp X gồm hai muối clorua của A và B vào nước thu được 100 gam dung dịch Y. Để kết tủa hết ion Cl- có trong 40 gam dung dịch Y bằng dung dịch AgNO3 thì thu được 17,22 gam kết tủa. Hãy xác định các kim loại A và B, biết tỉ số khối lượng nguyên tử của chúng là 3:5.
2.38 Hỗn hợp A gồm hai muối cacbonat của hai kim loại kế tiếp nhau trong nhóm IIA. Hòa tan hoàn toàn 3,6 gam hỗn hợp A trong dung dịch HCl thu được khí B, cho toàn bộ lượng khí B hấp thụ hết bởi 3 lit dung dịch Ca(OH)2 0,015M, thu được 4 gam kết tủa.
Xác định hai muối cacbonat và tính khối lượng của mỗi muối trong hỗn hợp A.
2.39 Để khử hoàn toàn 8 gam oxit của một kim loại thành kim loại cần dùng 3,36 lit H2. Hòa tan hết lượng kim loại thu được vào dung dịch HCl loãng thấy thoát ra 2,24 lit khí H2.
Xác định công thức của oxit. Biết các khí đo ở đktc.
2.40 Bảng dưới đây cho biết bán kính nguyên tử, năng lượng ion hóa của các nguyên tử nguyên tố chu kỳ 3
Nguyên tố | Na | Mg | Al | Si | P | S | Cl |
r (nm) | 0,186 | 0,160 | 0,143 | 0,117 | 0,110 | 0,104 | 0,099 |
I1 (kJ/mol) | 497 | 738 | 578 | 786 | 1012 | 1000 | 1251 |
1. Dựa vào các dữ kiện trên hãy cho nhận xét về sự biến đổi bán kính và sự biến đổi năng lượng ion hóa I1 của các nguyên tố trong chu kỳ.
2. Cho biết sự biến đổi tính chất axit - bazơ trong dãy oxit và hiđroxit dưới đây:
Na2O - MgO - Al2O3 - SiO2 - P2O5 - SO3 - Cl2O7
NaOH - Mg(OH)2 - Al(OH)3 - H2SiO3 - H3PO4 - H2SO4 - HClO4.
D. BÀI TẬP TRẮC NGHIỆM
2.41 Dãy nguyên tử nào sau đậy được xếp theo chiều bán kính nguyên tử tăng ?
A. I, Br, Cl, P B. C, N, O, F
C. Na, Mg, Al, Si D. O, S, Se, Te.
2.42 Tính chất kim loại của các nguyên tố trong dãy Mg – Ca – Sr - Ba biến đổi theo chiều :
A. Tăng B. giảm
C. Không thay đổi D. Vừa giảm vừa tăng
2.43 Tính chất phi kim của các nguyên tố trong dãy N- P-As-Sb-Bi biến đổi theo chiều :
A. Tăng B. giảm
C. Không thay đổi D. Vừa giảm vừa tăng.
2.44 Tính chất bazơ của hiđroxit của nhóm IA theo chiều tăng của số thứ tự là:
A. Tăng B. giảm
C. Không thay đổi D. Vừa giảm vừa tăng.
2.45 Cho các hình vẽ sau, mỗi hình cầu là 1 trong các nguyên tử Na, Mg, Al, K.

![]()
![]()
![]()
a b c d
a, b, c, d tương ứng theo thứ tự sẽ là:
A. Na, Mg, Al, K B. K, Na, Mg, Al
C. Al, Mg, Na, K D. K, Al, Mg, Na
2.46 Cho các nguyên tử a, b, c, d thuộc nhóm IA có bán kính trung bình như hình vẽ dưới đây:

![]()
![]()
![]()
a b c d
Năng lượng ion hóa I1 tăng dần theo thứ tự:
A.a < b < c < d B.d < c < b < a
C.a < c < b < d D.d < b < c < a
 2.47 Cho nguyên tử của nguyên tố X có cấu tạo như sau:
2.47 Cho nguyên tử của nguyên tố X có cấu tạo như sau:
Vị trí của nguyên tố X trong bảng tuần hoàn là:
- Ô số 7, chu kì 2, nhóm VIIA.
- Ô số 7, chu kì 2, nhóm VA
- Ô số 5, chu kì 2, nhóm VA
- Ô số 5, chu kì 7, nhóm VIIA.
 2.48 Cho ion đơn nguyên tử X có điện tích 2+ có cấu tạo như sau:
2.48 Cho ion đơn nguyên tử X có điện tích 2+ có cấu tạo như sau:
Cho biết vị trí của X trong bảng tuần hoàn.
A.Ô số 10, chu kì 2, nhóm VIIIA.
B.Ô số 12, chu kì 3, nhóm VIIIA.
C.Ô số 12, chu kì 3, nhóm IIA.
D.Ô số 10, chu kì 2, nhóm IIA.
2.49 Cho cấu hình của nguyên tố X sau, cho biết kết luận nào đúng?
![]()
1s2 2s2 2p6 3s2
- X ở ô số 12, chu kỳ 3, nhóm IIIA trong bảng tuần hoàn.
- X ở ô số 12, chu kỳ 3, nhóm IIIB trong bảng tuần hoàn.
- X ở ô số 12, chu kỳ 2, nhóm IIA trong bảng tuần hoàn.
- X ở ô số 12, chu kỳ 3, nhóm IIA trong bảng tuần hoàn.
2.50 Nguyên tử nguyên tố X, các ion Y+ và Z2- đều có cấu hình electron phân lớp ngoài cùng là 3p6. Số thứ tự của X, Y, Z trong bảng tuần hoàn lần lượt là
A. 18, 19 và 16 B. 10, 11 và 8
C. 18, 19 và 8 D. 1, 11 và 16
2.51 Tổng số hạt cơ bản (p, n, e) trong nguyên tử nguyên tố X là 46, biết số hạt mang điện nhiều hơn số hạt không mang điện là 14. Xác định chu kì, số hiệu nguyên tử của X trong bảng tuần hoàn.
A. Chu kì 2, ô 7 B. Chu kì 3, ô 15
C. Chu kì 3 ô 16 D. Chu kì 3 ô 17
2.52 Hòa tan hoàn toàn 3,1g hỗn hợp hai kim loại kiềm thuộc hai chu kì liên tiếp vào nước thu được 1,12 lít hiđro (đktc). Hai kim loại kiềm đã cho là
A. Li và Na B. Na và K
C. K và Rb D. Rb và Cs
2.53 Cho 0,64 g hỗn hợp gồm kim loại M và oxit của nó MO, có số mol bằng nhau, tác dụng hết với H2SO4 loãng. Thể tích khí H2(đktc) thu được là 0,224 lit. Cho biết M thuộc nhóm IIA. Xác định M là nguyên tố nào sau đây ?
A. Mg B. Ca C. Sr D. Ba
2.54 Hai kim loại X và Y đứng kế tiếp nhau trong một chu kỳ có tổng số proton trong hai hạt nhân nguyên tử là 25. Số electron lớp ngoài cùng của X và Y lần lượt là :
A. 1 và 2 B. 2 và 3 C. 1 và 3 D. 3 và 4
2.55 Ion M2+ có cấu tạo lớp vỏ electron ngoài cùng là 2s2 2p6. Cấu hình electron của M và vị trí của nó trong bảng tuần hoàn là
A. 1s22s22p4 , ô 8 chu kỳ 2, nhóm VIA.
B. 1s22s22p63s2 , ô 12 chu kỳ 3, nhóm IIA.
C. 1s22s22p63s 3p , ô 12 chu kỳ 3, nhóm IIA.
D. 1s22s22p63s23p , ô 13 chu kỳ 3, nhóm IIIA.
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP
2.41. D | 2.42. A | 2.43. B | 2.44. A | 2.45. B |
2.46. A | 2.47. B | 2.48. A | 2.49. D | 2.50. A |
2.51. B | 2.52. B | 2.53. A | 2.54. B | 2.55. A |
2.1 Trả lời
1. Số thứ tự 20, chu kì 4, nhóm IIA.
2. Số thứ tự 25, chu kì 4, nhóm VIIB.
2.2 Trả lời
1. Tổng số electron của nguyên tử M là 26. Số thứ tự 26, chu kì 4, nhóm VIIIB. M là Fe.
2. - Fe cháy trong khí clo: 2Fe + 3Cl2 ![]() 2FeCl3
2FeCl3
Hòa tan sản phẩm thu được vào nước thu được dung dịch. Lấy vài ml dung dịch cho tác dụng với dung dịch AgNO3, có kết tủa trắng chứng tỏ có gốc clorua:
FeCl3 + 3AgNO3 ![]() Fe(NO3)3 + 3AgCl
Fe(NO3)3 + 3AgCl![]()
Lặp lại thí nghiệm với dung dịch NaOH, có kết tủa nâu đỏ chứng tỏ có Fe(III): FeCl3 + 3NaOH ![]() Fe(OH)3
Fe(OH)3![]() + 3NaCl
+ 3NaCl
- Nung hỗn hợp bột Fe và bột S: Fe + S ![]() FeS
FeS
Cho B vào dung dịch H2SO4 loãng, có khí mùi trứng thối bay ra chứng tỏ có gốc sunfua: FeS + H2SO4 ![]() FeSO4 + H2S
FeSO4 + H2S ![]() (trứng thối)
(trứng thối)
Nhỏ dung dịch NaOH vào dung dịch thu được, có kết tủa trắng xanh chứng tỏ có Fe(II): FeSO4 + 2NaOH ![]() Na2SO4 + Fe(OH)2
Na2SO4 + Fe(OH)2![]() (trắng xanh)
(trắng xanh)
2.3 Trả lời
1. Cấu hình electron của nguyên tố đó là: 1s2 2s2 2p6 3s2 3p6 4s1
Tính chất đặc trưng của M là tính kim loại.
2. Nguyên tố đó nằm ở nhóm IA nên công thức oxit là M2O. Đây là một oxit bazơ.
2.4 Giải
1. Cấu hình electron của nguyên tử R là: 1s2 2s2 2p6 3s2 3p6 4s2
2. Nguyên tố A nằm ở ô số 20, chu kỳ 4, nhóm IIA trong bảng tuần hoàn.
3. R hóa trị II (R thuộc nhóm IIA).
Các phương trình hóa học:
R + 2H2O![]() R(OH)2 + H2
R(OH)2 + H2
2.5 Giải
1. Trong hợp chất MAx, M chiếm 46,67% về khối lượng nên:
 . Thay n - p = 4 và n' = p' ta có:
. Thay n - p = 4 và n' = p' ta có:
Tổng số proton trong MAx là 58 nên: p + xp' = 58.
Từ đây tìm được: p = 26 và xp' = 32.
Do A là phi kim ở chu kì 3 nên 15  p'
p'  17. Vậy x = 2 và p' = 16 thỏa mãn.
17. Vậy x = 2 và p' = 16 thỏa mãn.
Vậy M là Fe và M là S.
2. Hoàn thành các phương trình phản ứng:
a. 4FeS2 + 11O2  2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
b. FeS2 + 18HNO3  Fe(NO3)3 + 2H2SO4 + 15NO2 + 7H2O
Fe(NO3)3 + 2H2SO4 + 15NO2 + 7H2O
2.6 Giải
1. Gọi số mol các chất trong hỗn hợp đầu: M = a mol; MCO3 = b mol.
(mol): a a
MCO3 + 2HCl  MCl2 + CO2
MCl2 + CO2 + H2O (2)
+ H2O (2)
(mol): b b
Số mol H2 =  = 0,2 nên: a + b = 0,2 (3)
= 0,2 nên: a + b = 0,2 (3)
MA = 11,5 2 = 23 nên
2 = 23 nên  hay 2a + 44b = 4,6 (4)
hay 2a + 44b = 4,6 (4)
Theo bài: Ma + (M + 60)b = 10,8 (5)
Từ (3), (4), (5) ta tìm được: a = 0,1 mol; b = 0,1 mol; M = 24 (Mg).
2.7 Giải
1. Phân mức năng lượng của nguyên tử X và Y lần lượt là:
1s22s22p63s23p1 và 1s22s22p63s23p64s23d6.
Cấu hình electron của nguyên tử X và Y lần lượt là:
1s22s22p63s23p1 và 1s22s22p63s23p63d64s2.
Dựa vào bảng tuần hoàn ta tìm được X là Al và Y là Fe.
2. Gọi số mol các chất trong hỗn hợp: Al = a mol; Fe = b mol.
Ta có: 27a + 56b = 8,3 (1)
(mol): a 3a 1,5a
(mol): b 2b b
Khối lượng dung dịch sau phản ứng tăng thêm 7,8 gam nên: 8,3 -  = 7,8.
= 7,8.
Vậy:  = 0,5 gam
= 0,5 gam
 = 0,25 mol
= 0,25 mol  1,5a + b = 0,25 (4)
1,5a + b = 0,25 (4)
Từ (1) và (4) ta tìm được: a = 0,1 mol; b = 0,1 mol.
mAl = 27 0,1 = 2,7 (gam); mFe = 56
0,1 = 2,7 (gam); mFe = 56 0,1 = 5,6 (gam); VHCl =
0,1 = 5,6 (gam); VHCl =  = 1 (lit).
= 1 (lit).
2.8 Giải
Gọi số mol oxit MO = x mol.
(mol): x x x
Ta có: (M + 16)x = a
Khối lượng dung dịch axit H2SO4 ban đầu =  = 560x (gam).
= 560x (gam).
Khối lượng dung dịch sau phản ứng = a + 560x = (M + 16)x + 560x.
Theo bài: C% (MSO4) = 20% nên: .
.
Từ đây tìm được M = 24 (magie). Oxit kim loại cần tìm là MgO.
2.9 Giải
1. Gọi công thức chung của hai kim loại là M = a mol.
(mol): a 2a a
Số mol H2 = 0,15 mol nên a = 0,15 mol.
A và B là 2 kim loại nằm ở 2 chu kỳ liên tiếp thuộc nhóm IIA nên A là Mg và B là Ca.
2. Thể tích dung dịch HCl cần dùng =  = 0,3 (lit) = 300 (ml).
= 0,3 (lit) = 300 (ml).
Thể tích dung dịch HCl đã dùng = 300 + 25%.300 = 375 (ml).
2.10 Giải
a. Gọi công thức chung của kim loại là R = a mol.
(mol): a a a 0,5a
(mol): a a
Số mol HCl = 0,03 mol nên a = 0,03 mol.
Ta có: Ra = 0,85  R = 28,33. Vậy hai kim loại là Na và K.
R = 28,33. Vậy hai kim loại là Na và K.
Gọi số mol Na = b mol và K = c mol. Ta có: b + c = 0,03 và 23b + 39c = 0,85.
Từ đây tìm được b = 0,02 (mol); c = 0,01 (mol).
b. Dung dịch A gồm NaOH = 0,02 mol và KOH = 0,01 mol.
Khối lượng dung dịch A = 49,18 + 0,85 - 0,015 2 = 50 (gam).
2 = 50 (gam).
2.11 Giải
a. Gọi hóa trị cao nhất của R trong oxit là m, hóa trị trong hợp chất với hiđro là n. Ta có: m + n = 8.
Theo bài: m = 3n. Từ đây tìm được m =6; n = 2.
b. Công thức hợp chất R với hiđro là H2R. Theo bài:  nên R = 32.
nên R = 32.
Gọi tổng số hạt proton, nơtron của R là P, N. Ta có P + N = 32.
Mặt khác, R thuộc nhóm VI (hóa trị cao nhất trong oxit bằng VI) nên dựa vào cấu hình electron khi P = 13, 14, 15, 16 ta thấy P = 16 thỏa mãn.
Vậy kí hiệu của nguyên tử R là:  .
.
2.12 Giải
a. R nằm ở chu kỳ 3 nên lớp electron ngoài cùng là lớp thứ 3. Mặt khác, R thuộc phân nhóm chính nhóm VA nên nguyên tử R có 5 electron ở lớp ngoài cùng. Vậy cấu hình lớp electron ngoài cùng của R là 3s23p3.
Cấu hình electron của R là 1s22s22p63s23p3.
b. R thuộc nhóm V nên hóa trị cao nhất của R trong oxit là V. Công thức oxit là R2O5.
Theo bài: %R = 43,66% nên 
 R = 31 (photpho).
R = 31 (photpho).
Tổng số hạt electron = tổng số hạt proton = 15 (dựa vào cấu hình electron).
Tổng số hạt nơtron = 31 -15 = 16.
2.13 Giải
A và B là hai nguyên tố ở cùng một phân nhóm và thuộc hai chu kì liên tiếp trong bảng tuần hoàn nên số thứ tự của chúng hơn kém nhau 8 hoặc 18 đơn vị (đúng bằng số nguyên tố trong một chu kỳ).
Theo bài ra, tổng số proton trong hai hạt nhân nguyên tử của A và B bằng 32 nên ZA + ZB = 32.
Trường hợp 1: ZB - ZA = 8. Ta tìm được ZA = 12; ZB = 20.
Cấu hình electron:
A : 1s22s22p63s2 (chu kỳ 3, nhóm IIA).
và B: 1s22s22p63s23p64s2 (chu kỳ 4, nhóm IIA).
Ion A2+: 1s22s22p6 và B2+: 1s22s22p63s23p6.
Trường hợp 2: ZB - ZA = 18. Ta tìm được ZA = 7; ZB = 25.
Cấu hình electron:
A : 1s22s22p3 (chu kỳ 2, nhóm VA).
và B: 1s22s22p63s23p63d54s2 (chu kỳ 4, nhóm VIIB).
Trường hợp này A, B không cùng nhóm nên không thỏa mãn.
2.14 Giải
1. Hai nguyên tố A và B ở hai nhóm A liên tiếp trong bảng tuần hoàn, B thuộc nhóm VA, do đó A thuộc nhóm IVA hoặc nhóm VIA.
Theo bài: ZA + ZB = 23.
Vì: ZA + ZB = 23 và B thuộc nhóm V, còn A thuộc nhóm IV hoặc nhóm VI nên A, B thuộc các chu kì nhỏ (chu kỳ 2 và chu kỳ 3).
Mặt khác, A và B không thể cùng chu kỳ vì hai nguyên tố thuộc hai nhóm A kế tiếp trong một chu kỳ hơn kém nhau 1 proton, nghĩa là ở ô số 11 và 12 (tổng số proton bằng 23), không thuộc các nhóm IV và V hay V và VI.
Trường hợp 1: B thuộc chu kỳ 2. Theo bài, B ở nhóm VA nên ZB = 7 (nitơ). Vậy ZA = 23 - 7 = 16 (lưu huỳnh). Trường hợp này thỏa mãn vì ở trạng thái đơn chất nitơ không phản ứng với lưu huỳnh.
Trường hợp 2: B thuộc chu kỳ 3. Theo bài, B ở nhóm VA nên ZB = 15 (phopho). Vậy ZA = 23 - 15 = 8 (oxi). Trường hợp này không thỏa mãn vì ở trạng thái đơn chất oxi phản ứng với phopho.
Cấu hình electron của A và B là:
A: 1s22s22p63s23p4 và B: 1s22s22p3
2. Điều chế HNO3 từ N2 và H2SO4 từ S.
Điều chế HNO3: N2  NH3
NH3  NO
NO  NO2
NO2  HNO3
HNO3
![]()
N2 + 3H2 2NH3
Điều chế H2SO4: S  SO2
SO2  SO3
SO3  H2SO4
H2SO4
![]()
2SO2 + O2 2SO3
2.15 Giải
1. Gọi số hạt proton của A là P và của B là P', ta có:
P + 3P' = 42 - 2. Ta thấy 3P' < P + 3P' = 40 nên P' <  = 13,3.
= 13,3.
Do B tạo được anion nên B là phi kim. Mặt khác P' < 13,3 nên B chỉ có thể là nitơ, oxi hay flo.
Nếu B là nitơ (P' = 7)  P = 19 (K). Anion là
P = 19 (K). Anion là  : loại
: loại
Nếu B là oxi (P' = 8)  P = 16 (S). Anion là
P = 16 (S). Anion là  : thỏa mãn
: thỏa mãn
Nếu B là flo (P' = 9)  P = 13 (Al). Anion là
P = 13 (Al). Anion là  : loại
: loại
Vậy A là lưu huỳnh, B là oxi.
2. O (P' = 8) : 1s22s22p4 (ô số 8, chu kỳ 2, nhóm VIA)
S (P = 16) : 1s22s22p63s23p4 (ô số 16, chu kỳ 3, nhóm VIA)
2.16 Giải
1. Gọi tổng số hạt proton, nơtron, electron của nguyên tử R là P, N, E. Trong đó P = E.
Theo bài: P + N + E = 28  2P + N = 28
2P + N = 28  N = 28 - 2P.
N = 28 - 2P.
Mặt khác, P  N
N  1,5P
1,5P  P
P  28 - 2P
28 - 2P  1,5P
1,5P  8
8  P
P  9,3
9,3
Vậy P = 8 hoặc 9. Do nguyên tố R thuộc nhóm VIIA nên nguyên tử nguyên tố R có 7 electron ở lớp ngoài cùng.
P = 8: 1s22s22p4: loại
P = 9: 1s22s22p5: thỏa mãn. Vậy P = E = 9; N = 10.
1. Số khối A= N + P = 19.
Nguyên tố đã cho là flo.
2.17 Giải
Gọi tổng số hạt proton, nơtron, electron của nguyên tử M là P, N, E và của nguyên tử X là P', N', E'. Ta có P = E và P' = E'.
Theo bài ta lập được các sự phụ thuộc sau:
2(P + N + E) + P' + N' + E' = 140  4P + 2P' + 2N + N' = 140 (1)
4P + 2P' + 2N + N' = 140 (1)
2(P + E) + P' + E' - 2N - N' = 44  4P + 2P' - 2N - N' = 44 (2)
4P + 2P' - 2N - N' = 44 (2)
P + N - P' - N' = 23 « P + N - P' - N' = 23 (3)
(P + N + E - 1) - (P' + N' + E' + 2) = 31  2P + N - 2P' - N' = 34 (4)
2P + N - 2P' - N' = 34 (4)
Từ (1) và (2) ta có: 2P + P' = 46 và 2N + N' = 48.
Từ (3), (4) ta có: P - P' = 11 và N - N' = 12.
Giải ra ta được P = 19 (K); N = 20 ; P' = 8 (O); N' = 8. Vậy X là K2O.
Cấu hình electron:
K (P = 19): 1s22s22p63s23p64s1 (chu kỳ 4, nhóm IA).
O (P' = 8): 1s22s22p4 (chu kỳ 2, nhóm VIA)
2.18 Trả lời
1. Viết được cấu hình electron vì số electron ở lớp vỏ nguyên tử bằng số thứ tự Z.
2. Không biết số khối vì chỉ biết số proton bằng Z, nhưng không biết số nơtron.
3. Không viết được kí hiệu nguyên tử vì không biết số khối và ký hiệu nguyên tố.
4. Từ cấu hình electron ta biết được tính chất cơ bản.
5. Từ cấu hình electron ta biết được số thứ tự nhóm, và đó chính là hóa trị cao nhất trong oxit.
6. Hóa trị trong hợp chất với hiđro = 8 - hóa trị cao nhất trong oxit.
2.19 Trả lời
1. Biết được tính chất cơ bản dựa vào số electron lớp ngoài cùng.
2. Biết được cấu hình electron vì từ cấu hình lớp electron lớp ngoài cùng, chúng ta có thể hoàn chỉnh tiếp cấu hình electron các lớp bên trong.
3. Dựa vào cấu hình electron chúng ta biết được vị trí trong bảng tuần hoàn.
4. Ta lập được công thức oxit cao nhất vì hóa trị của cao nhất của nguyên tố bằng số thứ tự nhóm và bằng số electron lớp ngoài cùng.
5. Không viết được ký hiệu nguyên tử vì không biết số khối và ký hiệu nguyên tố.
6. Ta lập được công thức hợp chất với hiđro vì hóa trị của nguyên tố trong hợp chất với hiđro = 8 - hóa trị cao nhất trong oxit.
2.20 Giải
1. Năng lượng ion hóa thứ nhất giảm dần do bán kính nguyên tử tăng dần, lực hút của hạt nhân với electron hóa trị giảm dần.
Năng lượng ion hóa thứ hai ứng với quá trình: M+ (khí) - 1e  M2+ (khí). Vì ion M+ có cấu hình bền vững của khí hiếm và mang một điện tích dương nên việc bứt đi một electron khó khăn hơn nhiều, đòi hỏi cần cung cấp năng lượng rất lớn.
M2+ (khí). Vì ion M+ có cấu hình bền vững của khí hiếm và mang một điện tích dương nên việc bứt đi một electron khó khăn hơn nhiều, đòi hỏi cần cung cấp năng lượng rất lớn.
2. Dựa vào cấu hình electron ta thấy, trong các phản ứng hóa học các kim loại kiềm có khuynh hướng nhường 1 electron lớp ngoài cùng để đạt được cấu hình bền vững của khí hiếm. Mặt khác, các kim loại kiềm là các nguyên tố có độ âm điện bé nhất nên chúng luôn có số oxi hóa +1 trong các hợp chất.
Các kim loại kiềm không thể tạo được hợp chất có số oxi hóa lớn hơn +1 vì sự nhường tiếp các electron thứ hai, thứ ba, đòi hỏi năng lượng rất lớn.
2.21 Giải
a. Gọi tổng số hạt proton, nơtron và electron của nguyên tử A là: PA, NA, EA và B là PB, NB, EB. Ta có PA = EA và PB = EB.
Theo bài: Tổng số các loại hạt proton, nơtron và electron của hai nguyên tử A và B là 142 nên: PA + NA + EA + PB + NB + EB = 142
Tổng số hạt mang điện nhiều hơn số hạt không mang điện là 42 nên:
PA + EA + PB + EB - NA - NB = 42  2PA + 2PB - NA - NB = 42 (2)
2PA + 2PB - NA - NB = 42 (2)
Số hạt mang điện của nguyên tử B nhiều hơn của nguyên tử A là 12 nên:
PB + EB - PA - EA = 12  2PB - 2PA = 12
2PB - 2PA = 12  PB - PA = 6 (3)
PB - PA = 6 (3)
Từ (1), (2), (3) ta có: PA = 20 (Ca) và PB = 26 (Fe)
b. Điều chế Ca từ CaCO3 và Fe từ Fe2O3.
Điều chế Ca:
CaCO3 + 2HCl  CaCl2 + CO2 + H2O
CaCl2 + CO2 + H2O
Điều chế Fe: Fe2O3 + 3CO  2Fe + 3CO2
2Fe + 3CO2
2.22 Giải
a. Gọi số mol kim loại M là a mol.
(mol): a a
Số mol khí H2 =  = 0,25 (mol) nên: a = 0,25
= 0,25 (mol) nên: a = 0,25
b. Số mol Ca = 0,1 mol. Các phương trình phản ứng:
(mol): 0,075 0,15 0,075
(mol): 0,025 0,025
Dung dịch B gồm: CaCl2 = 0,075 mol và Ca(OH)2 = 0,025 mol.
2.23 Giải
a. Gọi số hạt prroton, nơtron, electron của nguyên tử X là P, N, E và của Y là P', N', E'.
Theo bài: P = N = E và P' = N' = E'.
Trong hợp chất XY2, X chiếm 50% về khối lượng nên:
Tổng số proton trong phân tử XY2 là 32 nên P + 2P' = 32.
Từ đây tìm được: P = 16 (S) và P' = 8 (O). Hợp chất cần tìm là SO2.
Cấu hình electron của S: 1s22s22p63s23p4 và của O: 1s22s22p4
b. Lưu huỳnh ở ô số 16, chu kỳ 3, nhóm VIA.
Oxi ở ô số 8, chu kỳ 2, nhóm VIA.
2.24 Giải
1. A, M, X thuộc chu kỳ 3 nên n = 3.
Cấu hình electron, vị trí và tên nguyên tố:
A: 1s22s22p63s1 (ô số 11, nhóm IA), A là kim loại Na.
M: 1s22s22p63s23p1 (ô số 13, nhóm IIIA), M là kim loại Al.
X: 1s22s22p63s23p5 (ô số 17, nhóm VIIA), X là phi kim Cl.
2. Các phương trình phản ứng:
NaAlO2 + HCl + H2O  Al(OH)3
Al(OH)3 + NaCl
+ NaCl
2.25 Giải
Gọi số mol trong mỗi phần: Fe = x mol; M = y mol.
Phần 1:
(mol): x x
(mol): y 0,5ny
Số mol H2 = 0,07 nên x + 0,5ny = 0,07.
Phần 2:
2Fe + 6H2SO4 (đặc)  Fe2(SO4)3 + 3SO2
Fe2(SO4)3 + 3SO2 + 6H2O
+ 6H2O
(mol): x 1,5x
2M + 2nH2SO4 (đặc)  M2(SO4)n + nSO2
M2(SO4)n + nSO2 + 2nH2O
+ 2nH2O
(mol): y 0,5nx
Số mol SO2 = 0,09 nên 1,5x + 0,5ny = 0,09. Vậy x = 0,04 và ny = 0,06.
Mặt khác: 56x + My = 2,78 nên My = 0,54. Vậy  hay M = 9n.
hay M = 9n.
Ta lập bảng sau:
n | 1 | 2 | 3 |
M | 9 (loại) | 18 (loại) | 27 (nhận) |
Vậy M là Al.
2.26 Giải:
1. Gọi số mol oxit RO = a mol.
(mol): a a a
Số mol axit H2SO4 dư =  - a = 0,03 - a.
- a = 0,03 - a.
C% (H2SO4) sau phản ứng = 0,98% 
 =
= 
Ta có: (M + 16)a = 2  M = 64 (Cu).
M = 64 (Cu).
2. Dung dịch A gồm: CuSO4 = 0,025 mol; H2SO4 = 0,005 mol.
(mol): 0,005 0,01
CuSO4 + 2NaOH  Cu(OH)2
Cu(OH)2 + Na2SO4
+ Na2SO4
(mol): 0,025 0,05
Khối lượng dung dịch NaOH cần dùng = 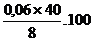 = 30 (gam).
= 30 (gam).
Thể tích dung dịch NaOH cần dùng =  = 28,57 (ml)
= 28,57 (ml)
2.27 Giải
1. Gọi số mol M = a mol.
(mol): a a a
Số mol H2 = 0,05 mol nên a = 0,05 mol.
Phần 1:
(mol): 0,025 0,025
(mol): 0,025 0,025
mRO = 1 gam  (R + 16).0,025 = 1
(R + 16).0,025 = 1  R = 24 (Mg).
R = 24 (Mg).
Phần 2: MgSO4.nH2O = 0,025 mol. Ta có: (120 + 18n).0,025 = 6,15  n = 7.
n = 7.
Vậy công thức muối ngậm nước là MgSO4.7H2O.
2.28 Giải
1. M thuộc nhóm IIIA nên M có hóa trị III.
M + 4HNO3  M(NO3)3 + NO
M(NO3)3 + NO + 2H2O (1)
+ 2H2O (1)
(mol): a 4a a a
10M + 36HNO3  10M(NO3)3 + 3N2
10M(NO3)3 + 3N2 + 18H2O (2)
+ 18H2O (2)
(mol): 10b 36b 10b 3b
Ta có: a + 3b = 0,25. (3)
MA = 14,4 2 = 28,8
2 = 28,8 

 30a + 84b = 7,2 (4)
30a + 84b = 7,2 (4)
Từ (3), (4) ta có: a = 0,1 mol; b = 0,05 mol.
M(a + 10b) = 16,2 M = 27 (Al).
M = 27 (Al).
2. Số mol HNO3 dư = 2,5 - 4a - 36b = 0,3 (mol).
Khối lượng dung dịch HNO3 ban đầu = 5000 1,25 = 6250 (gam).
1,25 = 6250 (gam).
Khối lượng dung dịch sau phản ứng = 6250 + 16,2 - 30a - 84b = 6259 (gam).
C% (HNO3 sau phản ứng) =  = 0,30%.
= 0,30%.
2.29 Giải
1. Vị trí các nguyên tố trong bảng tuần hoàn:
A: ô số 4, chu kỳ 2, nhóm IIA.
B: ô số 20, chu kỳ 4, nhóm IIA.
C: ô số 9, chu kỳ 2, nhóm VIIA.
D: ô số 17, chu kỳ 3, nhóm VIIA.
E: ô số 2, chu kỳ 1, nhóm VIIIA.
2. B là kim loại mạnh nhất. Hai kim loại A, B cùng thuộc nhóm IIA, theo chiều từ trên xuống, tính kim loại tăng dần.
C là phi kim mạnh nhất. Hai phi kim C, D cùng thuộc nhóm VIIA, theo chiều từ trên xuống, tính phi kim giảm dần.
E là nguyên tố kém hoạt động nhất vì lớp vỏ đã bão hòa electron.
2.30 Giải
Gọi kí hiệu chung của hai kim loại kiềm là M.
Gọi số mol trong 46 gam hỗn hợp đầu: M = a mol và Ba = b mol.
Các phương trình phản ứng:
(mol): a a 0,5a
(mol): b b b
Số mol H2 = 0,5 mol nên: 0,5a + b = 0,5  a + 2b = 1. (3)
a + 2b = 1. (3)
Khi cho dung dịch thu được tác dụng với dung dịch Na2SO4:
Ba(OH)2 + Na2SO4  BaSO4 + 2NaOH (4)
BaSO4 + 2NaOH (4)
Khi thêm 0,18 mol Na2SO4, trong dung dịch còn dư Ba(OH)2 nên b > 0,18.
Khi thêm 0,21 mol Na2SO4, trong dung dịch còn dư Na2SO4 nên b < 0,21.
Mặt khác: 0,18 < b < 0,21  29,7 < M < 33,34.
29,7 < M < 33,34.
Khối lượng mol trung bình của 2 kim loại kiềm liên tiếp là: 29,7 < M < 33,34. Hai kim loại đó là Na (Na = 23) và K ( K = 39).
2.31 Hướng dẫn:
1. Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kì trong bảng tuần hoàn nên điện tích hạt nhân hơn kém nhau 1 đơn vị.
Theo bài ra ta tìm được: ZA = 12 và ZB = 13.
A: 1s22s22p63s2 : A thuộc chu kỳ 3, nhóm IIA là Mg
B: 1s22s22p63s23p1 : B thuộc chu kỳ 3, nhóm IIIA.
2. A và B đều là kim loại, tính kim loại của A mạnh hơn B.
Oxit BO có tính bazơ yếu hơn oxit AO.
2.32 Hướng dẫn:
1. Trong một chu kì, theo chiều từ trái sang phải, điện tích hạt nhân tăng dần và bán kính nguyên tử giảm dần, điều đó làm tăng khả năng hút electron của nguyên tử trong phân tử, do đó độ âm điện tăng dần.
Trong một nhóm, theo chiều từ trên xuống dưới, bán kính nguyên tử tăng dần và chiếm ưu thế so với sự tăng điện tích hạt nhân, điều đó làm giảm khả năng hút electron của nguyên tử trong phân tử, do đó độ âm điện giảm dần.
2. Trong một chu kì, theo chiều từ trái sang phải, điện tích hạt nhân tăng dần và bán kính nguyên tử giảm dần, điều đó làm tăng lực hút của hạt nhân đối với các electron hóa trị, do đó năng lượng ion hóa tăng dần.
Trong một nhóm, theo chiều từ trên xuống dưới, bán kính nguyên tử tăng dần và chiếm ưu thế so với sự tăng điện tích hạt nhân, điều đó làm giảm lực hút của hạt nhân đối với các electron hóa trị, do đó năng lượng ion hóa giảm dần.
2.33 Hướng dẫn:
Từ Na đến Cl, bán kính nguyên tử giảm dần tuân theo quy luật biến đổi bán kính trong một chu kỳ. Đó là, trong một chu kỳ, khi đi từ trái sang phải điện tích hạt nhân tăng dần trong khi số lớp electron ở vỏ nguyên tử không đổi, do đó bán kính nguyên tử giảm dần.
Từ Li đến Cs, bán kính nguyên tử tăng dần tuân theo quy luật biến đổi bán kính trong một phân nhóm. Đó là, trong một phân nhóm, khi đi từ trên xuống dưới số lớp electron ở vỏ nguyên tử tăng lên và chiếm ưu thế hơn so với sự tăng điện tích hạt nhân, do đó bán kính nguyên tử tăng dần.
2.34 Hướng dẫn:
1. Theo bài ra, hóa trị của X trong hợp chất với hiđro là II nên hóa trị cao nhất trong oxit là VI.
Vậy X thuộc chu kỳ 3, nhóm VIA trong bảng tuần hoàn. X là S.
2. Các phương trình phản ứng:
H2S + 4Cl2 + 4H2O  H2SO4 + 8HCl
H2SO4 + 8HCl
H2S + 2FeCl3  2FeCl2 + S
2FeCl2 + S + 2HCl
+ 2HCl
H2S + CuSO4 ![]() CuS
CuS![]() + H2SO4
+ H2SO4
2.35 Hướng dẫn:
1. Gọi số oxi hóa dương cao nhất và số oxi hóa âm thấp nhất của R lần lượt là +m và -n. Ta có: m + n = 8.
Mặt khác, theo bài ra: +m + 2(-n) = +2 ![]() m - 2n = 2.
m - 2n = 2.
Từ đây tìm được: m = 6 và n = 2. Vậy R là phi kim thuộc nhóm VI.
Số khối của R < 34 nên R là O hay S. Do oxi không tạo được số oxi hóa cao nhất là +6 nên R là lưu huỳnh.
2. Trong hợp chất X, R có số oxi hóa thấp nhất nên X có công thức là H2S.
Gọi công thức oxit Y là SOn.
Do %S = 50% nên ![]() =
=![]()
![]() n = 2. Công thức của Y là SO2.
n = 2. Công thức của Y là SO2.
2.36 Hướng dẫn:
1. Gọi công thức chung của hai muối là M2CO3 = a mol.
M2CO3 + HCl ![]() MHCO3 + MCl
MHCO3 + MCl
(mol): a a a
MHCO3 + HCl ![]() MCl + CO2
MCl + CO2![]() + H2O
+ H2O
(mol): 0,1 0,1 0,1 0,1
Dung dịch A gồm MCl = a + 0,1 mol và MHCO3 = a - 0,1 mol.
MHCO3 + Ca(OH)2 ![]() CaCO3
CaCO3![]() + MOH + H2O
+ MOH + H2O
(mol): a - 0,1 a - 0,1
Theo bài: số mol CaCO3 = 0,2 mol nên a - 0,1 = 0,2 ![]() a = 0,3.
a = 0,3.
Ta có: (2M + 60).0,3 = 35 ![]() M = 28,33. Do hai kim loại kiềm thuộc hai chu kì liên tiếp nên đó là Na và K.
M = 28,33. Do hai kim loại kiềm thuộc hai chu kì liên tiếp nên đó là Na và K.
2. Gọi số mol Na2CO3 = b mol và K2CO3 = c mol.
Ta có b + c = 0,3 và 106b + 138c = 35.
Từ đây tìm được b = 0,2 mol; c = 0,1 mol.
m![]() 21,2 gam; m
21,2 gam; m![]() 13,8 gam.
13,8 gam.
2.37 Hướng dẫn:
1. Gọi công thức chung của hai muối là MCl2 và số mol có trong 15,05 gam hỗn hợp là a mol.
MCl2 + 2AgNO3 ![]() M(NO3)2 + 2AgCl
M(NO3)2 + 2AgCl![]()
(mol): ![]() 0,8a
0,8a
Số mol AgNO3 = 0,12 mol nên 0,8a = 0,12 ![]() a = 0,15 mol.
a = 0,15 mol.
Ta có: (M + 71)a = 15,05 ![]() M = 29,33.
M = 29,33.
Như vậy, A có khối lượng nguyên tử nhỏ hơn 29,33, A có thể là Be hoặc Mg.
Nếu A là Be thì MB = ![]() = 15: loại
= 15: loại
Nếu A là Mg thì MB = ![]() = 40: Vậy B là Ca.
= 40: Vậy B là Ca.
2.38 Hướng dẫn:
1. Gọi công thức chung của hai muối là MCO3 và số mol có trong 3,6 gam hỗn hợp là a mol.
MCO3 + 2HCl ![]() MCl2 + CO2
MCl2 + CO2![]() + H2O
+ H2O
(mol): a a
Khí B là CO2 = a mol. Cho toàn bộ lượng khí B hấp thụ hết bởi dung dịch chứa 0,045 mol Ca(OH)2, xảy ra 2 trường hợp:
Trường hợp 1: Ca(OH)2 dư ( a < 0,045 mol)
CO2 + Ca(OH)2 ![]() CaCO3
CaCO3![]() + H2O
+ H2O
(mol): a a a
Số mol CaCO3 = 0,04 mol ![]() a = 0,04 (thỏa mãn điều kiện a < 0,045 mol).
a = 0,04 (thỏa mãn điều kiện a < 0,045 mol).
Ta có: (M + 60).0,04 = 3,6 ![]() M = 30. Hai kim loại kế tiếp là Mg và Ca.
M = 30. Hai kim loại kế tiếp là Mg và Ca.
Trường hợp 2: Ca(OH)2 không dư ( a ![]() 0,045 mol)
0,045 mol)
CO2 + Ca(OH)2 ![]() CaCO3
CaCO3![]() + H2O
+ H2O
(mol): 0,04 0,04 0,04
2CO2 + Ca(OH)2 ![]() Ca(HCO3)2
Ca(HCO3)2
(mol): 0,01 0,005
Số mol CO2 = 0,05 mol ![]() a = 0,05 (thỏa mãn điều kiện a
a = 0,05 (thỏa mãn điều kiện a ![]() 0,045 mol).
0,045 mol).
Ta có: (M + 60).0,05 = 3,6 ![]() M = 12. Hai kim loại kế tiếp là Be và Mg.
M = 12. Hai kim loại kế tiếp là Be và Mg.
2.39 Hướng dẫn:
Gọi công thức oxit là MxOy , có số mol là a mol.
MxOy + yH2 ![]() xM + yH2O
xM + yH2O
(mol): a ay ax
Ta có: a(Mx + 16y) = 8 và ay = 0,15. Như vậy M.a.x = 5,6.
Đặt n là hóa trị của kim loại M (1 £ n £3).
2M + 2nHCl ![]() 2MCln + nH2
2MCln + nH2![]()
(mol): ax 0,5n.a.x
Ta có: 0,5n.a.x = 0,1 hay n.a.x = 0,2.
Lập tỉ lệ: ![]() . Vậy M = 28n.
. Vậy M = 28n.
Ta lập bảng sau:
n | 1 | 2 | 3 |
M | 28 (loại) | 56 (nhận) | 84 (loại) |
Vậy kim loại M là Fe.
Lập tỉ lệ: ![]() .
.
Vậy công thức oxit kim loại là Fe2O3.
2.40 Hướng dẫn:
1. Từ Na đến Cl, bán kính nguyên tử giảm dần tuân theo quy luật biến đổi bán kính trong một chu kỳ. Đó là, trong một chu kỳ, khi đi từ trái sang phải, theo chiều điện tích hạt nhân tăng dần, số electron ở lớp ngoài cùng tăng dần trong khi số lớp electron ở vỏ nguyên tử không đổi, do đó bán kính nguyên tử giảm dần.
Năng lượng ion hóa thứ nhất tăng dần do điện tích hạt nhân tăng dần, bán kính nguyên tử giảm dần, lực hút của hạt nhân với electron hóa trị tăng dần.
2. Tính chất axit - bazơ trong dãy oxit và hiđroxit biến đổi theo chiều giảm dần tính bazơ và tăng dần tính axit.
Na2O | MgO | Al2O3 | SiO2 | P2O5 | SO3 | Cl2O7 |
Oxit bazơ mạnh | Oxit bazơ trung bình | Oxit lưỡng tính | Oxit axit yếu | Oxit axit trung bình | Oxit axit mạnh | Oxit axit mạnh |
NaOH | Mg(OH)2 | Al(OH)3 | H2SiO3 | H3PO4 | H2SO4 | HClO4 |
Bazơ kiềm | Bazơ trung bình | Hiđroxit lưỡng tính | Axit yếu | Axit trung bình | Axit mạnh | Axit rất mạnh |
F. THÔNG TIN BỔ SUNG
1. Dạng kim tự tháp
2. Dạng bảng tuần hoàn xoáy trôn ốc
3. Dạng bảng tuần hoàn có kí hiệu đặc biệt
Chương 3
 LIÊN KẾT HÓA HỌC
LIÊN KẾT HÓA HỌC
A. TÓM TẮT LÍ THUYẾT
I. Liên kết liên kết ion và cộng hóa trị
- Liên kết hóa học là sự kết hợp giữa các nguyên tố tạo thành phân tử hay tinh thể bền vững hơn.
- Các nguyên tử của các nguyên tố có khuynh hướng liên kết với nguyên tử khác tạo thành để đạt được cấu hình electron bền vững như của khí hiếm (có 2 hoặc 8 electron lớp ngoài cùng).
1. Liên kết ion
 Định nghĩa: Là liên kết được hình thành do lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
Định nghĩa: Là liên kết được hình thành do lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
Nguyên tử kim loại nhường electron hóa trị trở thành ion dương (cation).
Nguyên tử phi kim nhận electron trở thành ion âm (anion). Các ion trái dấu hút nhau tạo thành liên kết ion.
Thí dụ: Liên kết trong phân tử CaCl2
+ Nguyên tử Ca nhường 2 electron tạo thành ion dương.
Ca -® Ca2+ + 2e
+ Nguyên tử clo nhận 1 electron tạo thành ion âm.
Cl2 + 2e ® 2Cl-
Ion Ca2+ và 2 ion Cl- hút nhau tạo thành phân tử CaCl2.
 Điều kiện hình thành liên kết ion
Điều kiện hình thành liên kết ion
Các nguyên tố có tính chất khác hẳn nhau (kim loại và phi kim điển hình).
Quy ước hiệu độ âm điện giữa hai nguyên tử liên kết ³ 1,7 là liên kết ion.
Các hợp chất ion có nhiệt độ nóng chảy và nhiệt độ sôi cao, dẫn điện khi tan trong nước hoặc nóng chảy.
2. Liên kết cộng hóa trị
 Định nghĩa: Là liên kết được hình thành giữa 2 nguyên tử bằng một hay nhiều cặp electron dùng chung.
Định nghĩa: Là liên kết được hình thành giữa 2 nguyên tử bằng một hay nhiều cặp electron dùng chung.
 Điều kiện hình thành liên kết cộng hóa trị
Điều kiện hình thành liên kết cộng hóa trị
Các nguyên tử giống nhau hoặc gần giống nhau, liên kết với nhau bằng cách góp chung các electron hóa trị. Thí dụ Cl2, H2, N2, HCl, H2O...
Quy ước hiệu độ âm điện giữa hai nguyên tử liên kết < 1,7 là liên kết cộng hóa trị.
 Liên kết cộng hóa trị có cực và không cực
Liên kết cộng hóa trị có cực và không cực
Khi cặp electron dùng chung phân bố đối xứng giữa hai hạt nhân nguyên tử tham gia liên kết thì đó là liên kết cộng hóa trị không phân cực.
Khi cặp electron dùng chung bị hút lệch về nguyên tử có độ âm điện lớn hơn thì đó là liên kết cộng hóa trị có cực.
Quy ước hiệu độ âm điện giữa hai nguyên tử liên kết 0,4 £ Dc < 1,7 là liên kết cộng hóa trị có cực, nếu giá trị này nhỏ hơn 0,4 thì liên kết là cộng hóa trị không cực.
II. Sự lai hóa các obitan nguyên tử
1. Sự lai hóa
Sự lai hóa obitan nguyên tử là sự tổ hợp một số obitan nguyên tử trong một nguyên tử để được các obitan lai hóa giống nhau, có số lượng bằng tổng số obitan tham gia lai hóa, nhưng định hướng khác nhau trong không gian.
2. Các kiểu lai hóa thường gặp
a. Lai hóa sp: Là sự tổ hợp 1 obitan s với 1 obitan p tạo thành 2 obitan lai hóa sp nằm thẳng hàng với nhau, hướng về hai phía.

b. Lai hóa sp2: Là sự tổ hợp của 1 obitan s với 2 obitan p của một nguyên tử tham gia liên kết tạo thành 3 obitan lai hóa sp2 nằm trong một mặt phẳng, định hướng từ tâm đến các đỉnh của tam giác đều.

c. Lai hóa sp3: Là sự tổ hợp của 1 obitan s với 3 obitan p của một nguyên tử tham gia liên kết tạo thành 4 obitan lai hóa sp3 định hướng từ tâm đến các 4 đỉnh của tứ diện đều.

III. Sự tạo thành liên kết cộng hóa trị
1. Liên kết đơn
Được hình thành do sự xen phủ trục của các obitan (liên kết s). Các liên kết s thường rất bền vững.
Thí dụ: H - Cl ; H - O - H
2. Liên kết đôi.
Bao gồm 1 liên kết s hình thành do sự xen phủ trục và 1 liên kết ở hình thành do sự xen phủ bên của các obitan lai hóa. Liên kết ở thường kém bền.
Thí dụ CH2 = CH2; O = C = O
3. Liên kết ba.
Bao gồm 1 liên kết s và 2 liên kết ở.
Thí dụ![]()
IV. Hóa trị và số oxi hóa
1. Hóa trị
- Trong các hợp chất ion: hóa trị (còn gọi là điện hóa trị) chính bằng điện tích của ion đó.
- Trong hợp chất cộng hóa trị: hóa trị (cộng hóa trị) chính bằng số liên kết của nguyên tử nguyên tố đó tạo ra được với các nguyên tử khác.
2. Số oxi hóa
Số oxi hóa của một nguyên tố trong hợp chất là điện tích của nguyên tử nguyên tố đó trong phân tử nếu giả định liên kết trong phân tử là liên kết ion.
Xác định số oxi hóa của các nguyên tử trong phân tử theo nguyên tắc:
+ Số oxi hóa của các đơn chất bằng không.
+ Tổng số oxi hóa của các nguyên tử trong phân tử bằng không
. + Số oxi hóa của các ion bằng điện tích của ion đó.
+ Trong hầu hết các hợp chất, số oxi hóa của hiđro là +1, của oxi là -2.
V. Liên kết kim loại
- Liên kết kim loại là liên kết được hình thành giữa các nguyên tử và ion kim loại trong mạng tinh thể do dự tham gia của các electron tự do.
- Các mạng tinh thể kim loại thường gặp: Lập phương tâm khối, lập phương tâm diện, lục phương.
- Các kim loại dẫn điện, dẫn nhiệt tốt, có tính dẻo, có ánh kim là do cấu tạo tinh thể kim loại quy định.
B. BÀI TẬP CÓ LỜI GIẢI
3.1 Viết cấu hình electron của Cl (Z=17) và Ca (Z=20). Cho biết vị trí của chúng (chu kì, nhóm) trong bảng tuần hoàn. Liên kết giữa canxi và clo trong hợp chất CaCl2 thuộc loại liên kết gì? Vì sao? Viết sơ đồ hình thành liên kết đó.
(Trích đề thi tuyển sinh ĐH- CĐ khối B năm 2004)
3.2 Hai nguyên tố M và X tạo thành hợp chất có công thức là M2X. Cho biết:
- Tổng số proton trong hợp chất bằng 46.
- Trong hạt nhân của M có n - p = 1, trong hạt nhân của X có n' = p'.
- Trong hợp chất M2X, nguyên tố X chiếm ![]() khối lượng.
khối lượng.
1. Tìm số hạt proton trong nguyên tử M và X.
2. Dựa vào bảng tuần hoàn hãy cho biết tên các nguyên tố M, X.
3. Liên kết trong hợp chất M2X là liên kết gì? Tại sao? Viết sơ đồ hình thành liên kết trong hợp chất đó.
3.3 Viết cấu hình electron của các nguyên tử A, B biết rằng:
- Tổng số các loại hạt cơ bản trong nguyên tử A là 34. Số hạt mang điện nhiều hơn số hạt không mang điện là 10.
- Kí hiệu của nguyên tử B là ![]() B.
B.
2. Liên kết trong hợp chất tạo thành từ A và B thuộc loại liên kết gì? Vì sao? Viết công thức của hợp chất tạo thành .
3.4 X, Y, Z là những nguyên tố có điện tích hạt nhân lần lượt là 9, 19, 8.
1. Viết cấu hình electron nguyên tử của các nguyên tố đó. Cho biết tính chất hóa học đặc trưng của X, Y, Z.
2. Dự đoán liên kết hóa học có thể có giữa các cặp X và Y, Y và Z, X và Z. Viết công thức phân tử của các hợp chất tạo thành.
3.5 Một hợp chất có công thức XY2 trong đó Y chiếm 50% về khối lượng. Trong hạt nhân của X có n = p và hạt nhân Y có n' = p'. Tổng số proton trong phân tử XY2 là 32.
a. Viết cấu hình electron của X và Y.
b. Dựa vào bảng tuần hoàn, cho biết X, Y là những nguyên tố gì? Cho biết bản chất liên kết và công thức cấu tạo của phân tử XY2.
3.6 Tổng số hạt proton, nơtron, electron của nguyên tử một nguyên tố R nhóm VIIA là 28.
1. Tính số khối của R. Dựa vào bảng tuần hoàn, cho biết R là nguyên tố gì?
2. Viết công thức phân tử và công thức cấu tạo của phân tử đơn chất R.
3. Viết công thức electron và công thức cấu tạo hợp chất của R với hiđro.
3.7 Phân tử NH3 có cấu tạo dạng chóp tam giác với góc liên kết HNH bằng 1070.
1. Theo lý thuyết lai hóa, nguyên tử nitơ trong phân tử NH3 ở trạng thái lai hóa nào? Mô tả sự hình thành liên kết trong NH3 theo giả thiết lai hóa đó.
2. Giải thích tại sao góc liên kết trong phân tử NH3 lại nhỏ hơn so với góc của tứ đều (109,5o)?
3.8 Phân tử H2O có cấu tạo hình chữ V với góc liên kết HOH bằng 104,50.
1. Theo lý thuyết lai hóa, nguyên tử oxi trong phân tử H2O ở trạng thái lai hóa nào? Mô tả sự hình thành liên kết trong H2O theo giả thiết lai hóa đó.
2. Giải thích tại sao góc liên kết trong phân tử H2O lại nhỏ hơn so với góc của tứ đều (109,5o)?
3.9 Trình bày cấu trúc của tinh thể nước đá. Tinh thể nước đá thuộc kiểu tinh thể nguyên tử, phân tử hay ion?
2. Hãy giải thích vì sao nước đá lại nổi trên bề mặt nước lỏng?
3.10 Nguyên tố R có hóa trị cao nhất trong oxit gấp 3 lần hóa trị trong hợp chất với hiđro.
a. Hãy cho biết hóa trị cao nhất của R trong oxit.
b. Trong hợp chất của R với hiđro, R chiếm ![]() phần khối lượng.
phần khối lượng.
Không dùng bảng tuần hoàn, cho biết kí hiệu của nguyên tử R.
c. Dựa vào bảng tuần hoàn cho biết R là nguyên tố gì? Viết công thức electron và công thức cấu tạo oxit cao nhất của R.
3.11 Hợp chất X tạo bởi hai nguyên tố A, B và có phân tử khối là 76. A và B có số oxi hóa cao nhất trong các oxit là +nO và + mO, và số oxi hóa âm trong các hợp chất với hiđro là -nH và -mH thỏa mãn điều kiện nO = nH và mO = 3mH.
1. Tìm công thức phân tử của X, biết rằng A cố số oxi hóa cao nhất trong X.
2. Biết rằng X có cấu trúc phân tử thẳng. Hãy cho biết trạng thái lai hóa của nguyên tử A và bản chất liên kết trong X.
3.12 X là nguyên tố thuộc chu kì 3, X tạo với hiđro một hợp chất khí có công thức H2X, trong đó X có số oxi hóa thấp nhất.
1. Xác định vị trí của X trong bảng tuần hoàn.
2. Trong oxit cao nhất của R thì R chiếm 40% khối lượng. Tìm khối lượng nguyên tử của R.
3. Dựa vào bảng tuần hoàn hãy cho biết X là nguyên tố nào. Viết phương trình phản ứng khi lần lượt cho H2X tác dụng với nước Cl2, dung dịch FeCl3, dung dịch CuSO4.
3.13 R là một nguyên tố phi kim. Tổng đại số số oxi hóa dương cao nhất với 2 lần số oxi hóa âm thấp nhất của R là +2. Tổng số proton và nơtron của R nhỏ hơn 34.
1. Xác định R
2. X là hợp chất khí của R với hiđro, Y là oxit của R có chứa 50% oxi về khối lượng. Xác định công thức phân tử của X và Y.
3. Viết công thức cấu tạo các phân tử RO2; RO3; H2RO4.
3.14 Cation X+ do 5 nguyên tử của 2 nguyên tố hóa học tạo nên. Tổng số proton trong X+ là 11.
1. Xác định công thức và gọi tên cation X+.
2. Viết công thức electron của ion X+. Cho biết cấu trúc hình học của ion này?
3.15 Anion Y2- do 5 nguyên tử của 2 nguyên tố hóa học tạo nên. Tổng số electron trong Y2- là 50.
1. Xác định công thức phân tử và gọi tên ion Y2-, biết rằng 2 nguyên tố trong Y2- thuộc cùng một phân nhóm và thuộc hai chu kì liên tiếp.
2. Viết công thức electron của ion Y2-. Cho biết cấu trúc hình học của ion này?
3.16 Có 5,56 gam hỗn hợp A gồm Fe và kim loại M (hóa trị n). Chia A làm hai phần bằng nhau:
Phần 1: Hòa tan hết trong dung dịch HCl loãng, được 1,568 lit khí H2.
Phần 2: Hòa tan hết trong dung dịch H2SO4 đặc nóng thu được 2,016 lit khí SO2.
Viết các phương trình hóa học và xác định tên kim loại M. Các thể tích khí đo ở đktc.
3.17 Để khử hoàn toàn 8 gam oxit của một kim loại thành kim loại cần dùng 3,36 lit H2. Hòa tan hết lượng kim loại thu được vào dung dịch HCl loãng thấy thoát ra 2,24 lit khí H2. Biết các khí đo ở đktc.
Xác định công thức của oxit. Cho biết số oxi hóa và hóa trị của kim loại trong oxit.
3.18 Khử hoàn toàn 4,06 gam một oxit kim loại bằng CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng dung dịch Ca(OH)2 dư, thấy tạo thành 7 gam kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl dư thì thu được 1,176 lit khí H2 (đktc).
1. Xác định công thức oxit kim loại.
2. Cho 4,06 gam oxit kim loại trên tác dụng hoàn toàn với 500ml dung dịch H2SO4 đặc, nóng (dư) được dung dịch X và có khí SO2 bay ra.
Hãy xác định nồng độ mol/lit của muối trong dung dịch X.
Coi thể tích của dung dịch không thay đổi trong suốt quá trình phản ứng.
(Trích đề thi tuyển sinh ĐH- CĐ khối A năm 2003)
3.19 Hòa tan hoàn toàn 7 gam kim loại M trong 200 gam dung dịch HCl vừa đủ thu được 206,75 gam dung dịch A.
1. Xác định M và nồng độ % của dung dịch HCl.
2. Hòa tan 6,28 gam hỗn hợp X gồm M và một oxit của M trong 170 ml dung dịch HNO3 2M (loãng, vừa đủ) thu được 1,232 lit NO (đktc).
Tìm công thức của oxit. Cho biết số oxi hóa và hóa trị của M trong oxit.
C. BÀI TẬP TỰ LUYỆN
3.20 Trong mạng tinh thể kim loại, người ta dùng độ đặc khít ![]() là phần trăm thể tích mà các nguyên tử chiếm trong tinh thể để đặc trưng cho từng kiểu cấu trúc. Với kiểu cấu trúc lập phương tâm khối,
là phần trăm thể tích mà các nguyên tử chiếm trong tinh thể để đặc trưng cho từng kiểu cấu trúc. Với kiểu cấu trúc lập phương tâm khối, ![]() = 68%; kiểu cấu trúc lập phương tâm diện,
= 68%; kiểu cấu trúc lập phương tâm diện, ![]() = 74%. Bằng tính toán cụ thể, hãy chứng minh các kết quả trên.
= 74%. Bằng tính toán cụ thể, hãy chứng minh các kết quả trên.
3.21 Thừa nhận rằng các nguyên tử Ca, Cu đều có dạng hình cầu sắp xếp đặc khít bên cạnh nhau, thì thể tích chiếm bởi các nguyên tử kim loại chiếm 74% so với toàn bộ khối tinh thể. Hãy tính bán kính nguyên tử Ca, Cu (theo đơn vị Å), biết khối lượng riêng của các tinh thể kim loại ở điều kiện chuẩn tương ứng là 1,55g/cm3 và 8,90g/cm3.
Cho biết: Ca = 40,08; Cu =63,55; 1 Å = 10-8 cm; 1u = 1,67.10-24 g.
3.22 Trình bày bản chất liên kết kim loại. So sánh liên kết kim loại với liên kết cộng hóa trị và liên kết ion.
2. Hãy giải thích tại sao các kim loại có những tính chất vật lý đặc trưng là có ánh kim, có tính dẻo và có khả năng dẫn điện, dẫn nhiệt tốt.
3.23 Kim loại Na có cấu trúc mạng tinh thể theo kiểu lập phương tâm khối với độ dài mỗi cạnh hình lập phương là a = 0,429 nm. Hãy tính:
1. Bán kính nguyên tử Na.
2. Khối lượng riêng (g/cm3) của natri. Natri có thể nổi trên nước không?
Cho biết khối lượng nguyên tử của natri là 23u ( 1u = 1,67.10-24 g).
3.24 Kim loại Ni có cấu trúc mạng tinh thể theo kiểu lập phương tâm diện. Bán kính nguyên tử của Ni là r = 1,24.10-8 cm. Hãy tính:
1. Độ dài mỗi cạnh hình lập phương.
2. Khối lượng riêng (g/cm3) của niken.
Cho biết khối lượng nguyên tử của niken là 58,7u ( 1u = 1,67.10-24 g).
3.25 Cấu trúc mạng tinh thể của hợp chất ion NaCl được biểu diễn dưới đây:

Trong đó các quả cầu lớn (ion Cl-) phân bố theo kiểu lập phương tâm diện, các quả cầu nhỏ (ion Na+) phân bố ở tâm và ở giữa các cạnh của hình lập phương.
1. Tính số ion Na+ và Cl- có trong một hình lập phương.
2. Tính bán kính ion Na+ và Cl-.
Cho biết hình lập phương có cạnh là a = 0,552 nm và tỉ lệ bán kính  .
.
D. BÀI TẬP TRẮC NGHIỆM
3.26 Liên kết hóa học trong phân tử H2 được hình thành nhờ sự xen phủ của các orbitan nào?
A. ![]()
B. ![]()
C. ![]()
D. Một kết quả khác.
3.27 Liên kết hóa học trong phân tử HCl được hình thành nhờ sự xen phủ của các orbitan nào?
A. ![]()
B. ![]()
C. ![]()
D. Một kết quả khác.
3.28 Liên kết hóa học trong phân tử Cl2 được hình thành nhờ sự xen phủ của các orbitan nào?
A. ![]()
B. ![]()
C. ![]()
D. Một kết quả khác.
3.29 Chọn hình vẽ mô tả đúng sự tạo thành liên kết trong phân tử H2S .
A.  B.
B. 
C.  D.
D. 
3.30 Hình nào dưới đây mô tả sự lai hóa sp?
A. ![]()
B.
C. 
D. Một đáp án khác.
3.31 Cho hình vẽ mô tả sự tạo thành orbitan lai hóa sp2.

Sự lai hóa sp2 sau đây xảy ra ở một nguyên tử do:
A. sự tổ hợp của 1orbitan s và 2 orbitan p của nguyên tử đó.
B. sự tổ hợp của 2orbitan s và 2 orbitan p của nguyên tử đó.
C. sự tổ hợp của 2orbitan s và 1 orbitan p của nguyên tử đó
D. sự tổ hợp của 1orbitan s và 3 orbitan p của nguyên tử đó
3.32 Cho 3 dạng lai hóa lần lượt như hình vẽ.
![]()


sp sp2 sp3
Góc giữa các orbitan lai hóa lần lượt là:
A. 1800, 1200, 109028' B. 1200 ; 1800 ; 109028'
C. 109028' ;1200 ;1800 D. 1800 ; 109028' ;1200
3.33 Sự xen phủ nào sau đây tạo thành liên kết σ?
A. ![]()
B. ![]()
C. ![]()
D. cả A, B, C đều đúng.
3.34 Sự xen phủ nào sau đây tạo thành liên kết π.
A. ![]()
B. ![]()
C. 
D. ![]()
3.35 Cho các tinh thể sau:



Kim cương( C ) I2 H2O
Tinh thể nào là tinh thể phân tử:
A.Tinh thể kim cương và Iốt B.Tinh thể kim cương và nước đá.
C.Tinh thể nước đá và Iốt. D.Cả 3 tinh thể đã cho.
3.36 Liên kết trong phân tử nào sau đây hình thành do sự xen phủ của các obitan s
A. HCl B. H2O
C. Cl2 D. H2
3.37 Cho các phân tử N2, HCl, NaCl, MgO. Các phân tử đều có liên kết cộng hóa trị là
A. N2 và HCl B. HCl và MgO
C. N2 và NaCl D. NaCl và MgO
3.38 Một phân tử XY3 có tổng các hạt proton, electron, notron bằng 196. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 60, số hạt mang điện của X ít hơn số hạt mang điện của Y trong phân tử là 76. XY3 là công thức nào sau đây ?
A. SO3 B. AlCl3 C. BF3 D. NH3
3.39 X, Y là hai nguyên tố thuộc cùng một nhóm A, ở hai chu kỳ liên tiếp. Cho biết tổng số electron trong anion XY là 42. Xác định hai nguyên tố X, Y và XY
là 42. Xác định hai nguyên tố X, Y và XY trong số các phương án sau
trong số các phương án sau
A. Be, Mg và MgBe3 B. S, O và SO32-
C. C, O và CO32- D. Si, O và SiO32-
3.40 Liên kết trong phân tử chất nào sau đây mang nhiều tính chất ion nhất?
A. LiCl B. NaCl C. CsCl D. RbCl
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP
3.27. B | 3.28. C | 3.29. A | 3.30. A | |
3.31. A | 3.32. A | 3.33. D | 3.34. C | 3.35. C |
3.36. D | 3.37. A | 3.38. B | 3.39. B | 3.40. C |
3.1 Hướng dẫn:
Cl (Z = 17) : 1s2 2s2 2p6 3s2 3p5
Ca (Z = 20) : 1s2 2s2 2p6 3s2 3p6 4s2
Clo nằm ở ô số 17, chu kỳ 3, nhóm VIIA.
Canxi nằm ở ô số 20, chu kỳ 4, nhóm IIA.
Liên kết trong hợp chất CaCl2 là liên kết ion vì Ca là kim loại điển hình, Cl là phi kim điển hình.
Sơ đồ hình thành liên kết:
2Cl + 2![]() 1e
1e ![]() 2Cl-
2Cl-
Ca ![]() Ca2+ + 2e
Ca2+ + 2e
Các ion Ca2+ và Cl- tạo thành mang điện tích trái dấu, chúng hút nhau bằng lực hút tĩnh điện, tạo thành hợp chất CaCl2:
3.2 Hướng dẫn:
1. Tổng số proton trong hợp chất M2X bằng 46 nên : 2p + p' = 46. (1)
Trong hợp chất M2X, nguyên tố X chiếm  khối lượng nên:
khối lượng nên:
Từ (1), (2) ta tìm được: p = 19; p' = 8.
2. M là kali (K) và X là oxi (O).
3. Liên kết trong hợp chất K2O là liên kết ion vì K là kim loại điển hình, O là phi kim điển hình.
Sơ đồ hình thành liên kết:
Các ion K+ và O2- tạo thành mang điện tích trái dấu, chúng hút nhau bằng lực hút tĩnh điện, tạo thành hợp chất K2O:
3.3 Hướng dẫn:
1. Gọi tổng số hạt proton, nơtron, electron của nguyên tử A là P, N, E (trong đó P = E).
Ta có: P + N + E = 34 và P + E - N = 10.
Từ đây tìm được P = E = 11; N = 12.
Kí hiệu của nguyên tử B là  B nên ZB = 9
B nên ZB = 9
Cấu hình electron của A, B:
A (Z = 11) : 1s2 2s2 2p6 3s1
B (Z = 9) : 1s2 2s2 2p5
2. Liên kết trong hợp chất giữa A và B là liên kết ion vì A là kim loại điển hình (nhóm IA), B là phi kim điển hình (nhóm VIIA).
Sơ đồ hình thành liên kết:
Các ion A+ và B- tạo thành mang điện tích trái dấu, chúng hút nhau bằng lực hút tĩnh điện, tạo thành hợp chất AB:
3.4 Hướng dẫn:
1. Cấu hình electron của các nguyên tử X, Y, Z:
X: (Z = 9) : 1s2 2s2 2p5
Y: (Z = 19) : 1s2 2s2 2p6 3s2 3p6 4s1
Z: (Z = 8) : 1s2 2s2 2p4
Tính chất đặc trưng của Y là tính kim loại, của X và Z là tính phi kim.
2. Liên kết giữa X và Y, giữa Y và Z là liên kết ion.
- Sự hình thành liên kết giữa X và Y:
Các ion Y+ và X- hút nhau bằng lực hút tĩnh điện, tạo thành hợp chất YX.
- Sự hình thành liên kết giữa Y và Z:
Các ion Y+ và Z2- hút nhau bằng lực hút tĩnh điện, tạo thành hợp chất Y2Z.
- X và Z là các phi kim nên liên kết giữa chúng là liên kết cộng hóa trị. Để đạt được cấu hình bền vững, mỗi nguyên tử X cần góp chung 1e, mỗi nguyên tử Z cần góp chung 2e. Như vậy 2 nguyên tử X sẽ tham gia liên kết với 1 nguyên tử Z bằng 2 liên kết cộng hóa trị đơn nhờ 2 cặp electron góp chung. Do đó công thức phân tử của hợp chất là X2Z.
3.5 Hướng dẫn:
a. Trong hợp chất XY2, X chiếm 50% về khối lượng nên:
Tổng số proton trong phân tử XY2 là 32 nên p + 2p' = 32.
Từ đây tìm được: p = 16 và p' = 8 .
Cấu hình electron của X: 1s22s22p63s23p4 và của Y: 1s22s22p4
b. Dựa vào bảng tuần hoàn ta thấy X là S, Y là O. Hợp chất cần tìm là SO2.
Sơ đồ hình thành liên kết trong phân tử SO2:

Tương ứng với công thức cấu tạo:
3.6 Hướng dẫn:
1. Gọi tổng số hạt proton, nơtron, electron của nguyên tử R là P. N, E. Trong đó P = E.
Theo bài: P + N + E = 28  2P + N = 28
2P + N = 28  N = 28 - 2P.
N = 28 - 2P.
Mặt khác, P  N
N  1,5P
1,5P  P
P  28 - 2P
28 - 2P  1,5P
1,5P  8
8  P
P  9,3
9,3
Vậy P = 8 hoặc 9. Do nguyên tố R thuộc nhóm VIIA nên nguyên tử nguyên tố R có 7 electron ở lớp ngoài cùng.
P = 8: 1s22s22p4: loại
P = 9: 1s22s22p5: thỏa mãn. Vậy P = E = 9; N = 10.
Số khối A= N + P = 19. R là flo.
2. Từ cấu hình electron của F ta thấy lớp ngoài cùng của nguyên tử F có 7 electron, còn thiếu một electron để đạt cấu hình bền vững của khí hiếm gần nhất. Do đó ở dạng đơn chất, nguyên tố F tồn tại dưới dạng phân tử 2 nguyên tử, liên kết giữa hai nguyên tử là liên kết cộng hóa trị đơn hình thành từ một cặp electron dùng chung.
Công thức phân tử là F2, công thức cấu tạo là F - F.
3. Công thức electron và công thức cấu tạo hợp chất của R với hiđro như sau:
![]()
H - F
Công thức electron Công thức cấu tạo
3.7 Hướng dẫn:
![]() 1. Để giải thích cấu trúc hình học của phân tử NH3, thuyết lai hóa cho rằng nguyên tử N ở trạng thái lai hóa tứ diện sp3.
1. Để giải thích cấu trúc hình học của phân tử NH3, thuyết lai hóa cho rằng nguyên tử N ở trạng thái lai hóa tứ diện sp3.
Sự hình thành các liên kết trong phân tử NH3 được giải thích như sau:
2. Do cặp electron không liên kết trên nguyên tử N chỉ chịu lực hút của hạt nhân nguyên tử N nên cặp electron này chiếm vùng không gian rộng hơn so với 3 cặp electron liên kết (chịu lực hút của hai hạt nhân). Do vậy nó tạo ra lực đẩy đối với đám mây các cặp electron liên kết, làm các đám mây này hơi bị ép lại, do vậy góc liên kết thực tế là 1070 hơi nhỏ hơn so với góc của tứ diện đều.
3.8 Hướng dẫn:
![]() 1. Để giải thích cấu trúc hình học của phân tử H2O, thuyết lai hóa cho rằng nguyên tử O ở trạng thái lai hóa tứ diện sp3.
1. Để giải thích cấu trúc hình học của phân tử H2O, thuyết lai hóa cho rằng nguyên tử O ở trạng thái lai hóa tứ diện sp3.
Sự hình thành các liên kết trong phân tử H2O được giải thích như sau:
Hai obitan lai hóa chứa electron độc thân sẽ xen phủ với 2 obitan 1s của 2 nguyên tử H tạo thành 2 liên kết  .
.
Hai obitan lai hóa chứa cặp electron của O không tham gia liên kết hướng về hai đỉnh của hình tứ diện.
2. Do 2 cặp electron không liên kết trên nguyên tử O chỉ chịu lực hút của hạt nhân nguyên tử O nên 2 cặp electron này chiếm vùng không gian rộng hơn so với 2 cặp electron liên kết (chịu lực hút của hai hạt nhân). Do vậy nó tạo ra lực đẩy đối với đám mây các cặp electron liên kết, làm các đám mây này hơi bị ép lại, do vậy góc liên kết thực tế là 104,50 nhỏ hơn so với góc của tứ diện đều. |
Hình 2. Cấu tạo phân tử H2O |
3.9 Hướng dẫn:
Mạng tinh thể nước đá thuộc kiểu mạng tinh thể phân tử. Mỗi phân tử nước liên kết với 4 phân tử nước khác gần nó nhất nằm trên bốn đỉnh của một hình tứ diện đều. Như vậy, trong mạng tinh thể, mỗi phân tử nước đều ở tâm của một hình tứ diện đều và liên kết với 4 phân tử nước trên 4 đỉnh nhờ tạo thành 4 liên kết hiđro. |
Hình 3. Mô hình tinh thể nước đá |
2. Cấu trúc tinh thể phân tử nước đá là cấu trúc tứ diện, là cấu trúc rỗng nên có tỉ khối nhỏ hơn khi nước ở trạng thái lỏng, do vậy nước đá nổi trên bề mặt nước lỏng. Thể tích nước của đá khi đông đặc lớn hơn khi ở trạng thái lỏng.
3.10 Hướng dẫn:
a. Gọi hóa trị cao nhất của R trong oxit là m, hóa trị trong hợp chất với hiđro là n.
Hóa trị cao nhất của R trong oxit là m nên ở lớp ngoài cùng nguyên tử R có m electron.
Hóa trị trong hợp chất của R với hiđro là n nên để đạt được cấu hình 8 electron bão hòa của khí hiếm, lớp ngoài cùng nguyên tử R cần nhận thêm n electron.
Như vậy ta có: m + n = 8. Theo bài: m = 3n. Từ đây tìm được m =6; n = 2.
b. Công thức hợp chất R với hiđro là H2R. Theo bài:  nên R = 32.
nên R = 32.
Gọi tổng số hạt proton, nơtron của R là P, N. Ta có P + N = 32.
Mặt khác, R thuộc nhóm VI (hóa trị cao nhất trong oxit bằng VI) nên dựa vào cấu hình electron khi P = 13, 14, 15, 16 ta thấy P = 16 thỏa mãn.
Vậy kí hiệu của nguyên tử R là:  .
.
c. R là lưu huỳnh. Hóa trị cao nhất của S trong oxit là VI nên công thức oxit là SO3. Công thức electron và công thức cấu tạo của oxit SO3 như sau:


Công thức electron Công thức cấu tạo
3.11 Hướng dẫn:
a. A, B có số oxi hóa cao nhất trong các oxit là +nO và + mO nên lớp ngoài cùng của A, B có số electron là nO và mO.
A, B có số oxi hóa âm trong các hợp chất với hiđro là -nH và - mH nên ta thấy để hoàn thành lớp vỏ bão hòa 8 electron, lớp ngoài cùng của A, B cần nhận thêm số electron là nH và mH.
Như vậy: nO + nH = 8 và mO + mH = 8.
Theo bài: nO = nH và mO = 3mH.
Từ đây tìm được nO = nH = 4, mO = 6, nH = 2.
A có số oxi hóa dương cao nhất là +4 nên A thuộc nhóm IV, B có số oxi hóa dương cao nhất là +6 nên B thuộc nhóm VI.
Trong hợp chất X, A có số oxi hóa +4 (nhường 4 electron) nên một nguyên tử A liên kết với 2 nguyên tử B, trong đó B có số oxi hóa -2.
Công thức phân tử của X là AB2.
Theo bài: khối lượng phân tử của X là 76u nên MA + 2MB = 76u.
Mặt khác, B thuộc nhóm VI và tạo được số oxi hóa cao nhất trong oxit là +6 nên B là lưu huỳnh. Vậy MB = 32u, suy ra MA = 76u - 2 32u = 12u. A là cacbon.
32u = 12u. A là cacbon.
Công thức của X là CS2.
2. Theo bài, CS2 có cấu trúc thẳng nên nguyên tử C ở trạng thái lai hóa sp.
Cấu hình electron lớp ngoài cùng của nguyên tử lưu huỳnh:


Liên kết trong phân tử CS2 được hình thành như sau:
Hai obitan lai hóa sp của C xen phủ trục với hai obitan 3p chứa electron độc thân của 2 lưu huỳnh tạo thành 2 liên kết  .
.
Hai obitan 2px, 2py không tham gia lai hóa của C xen phủ bên với hai obitan 3p chứa electron độc thân của 2 lưu huỳnh tạo thành 2 liên kết  .
.
Như vậy, nguyên tử cacbon tạo với mỗi nguyên tử lưu huỳnh 1 liên kết  và 1 liên kết
và 1 liên kết  . Công thức cấu tạo của phân tử CS2 như sau:
. Công thức cấu tạo của phân tử CS2 như sau:
![]()
3.12 Hướng dẫn:
1. Theo bài ra, hóa trị của X trong hợp chất với hidro là II nên hóa trị cao nhất trong oxit là VI.
Vậy X thuộc chu kỳ 3, nhóm VIA trong bảng tuần hoàn.
2. R thuộc nhóm VI nên hóa trị cao nhất trong oxit là VI, vậy công thức oxit cao nhất có dạng RO3. Trong oxit này R chiếm 40% khối lượng nên:
3. X là S. Các phương trình phản ứng:
H2S + 4Cl2 + 4H2O  H2SO4 + 8HCl
H2SO4 + 8HCl
H2S + 2FeCl3  2FeCl2 + S
2FeCl2 + S + 2HCl
+ 2HCl
3.13 Hướng dẫn:
1. Gọi số oxi hóa dương cao nhất và số oxi hóa âm thấp nhất của R lần lượt là +m và -n.
Số oxi hóa cao nhất của R trong oxit là +m nên ở lớp ngoài cùng nguyên tử R có m electron.
Số oxi hóa trong hợp chất của R với hiđro là -n nên để đạt được cấu hình 8 electron bão hòa của khí hiếm, lớp ngoài cùng nguyên tử R cần nhận thêm n electron.
Ta có: m + n = 8. Mặt khác, theo bài ra: +m + 2(-n) = +2  m - 2n = 2.
m - 2n = 2.
Từ đây tìm được: m = 6 và n = 2. Vậy R là phi kim thuộc nhóm VI.
Số khối của R < 34 nên R là O hay S. Do oxi không tạo được số oxi hóa cao nhất là +6 nên R là lưu huỳnh.
2. Trong hợp chất X, S có số oxi hóa thấp nhất nên X có công thức là H2S.
Gọi công thức oxit Y là SOn.
Do %S = 50% nên  =
=
 n = 2. Công thức của Y là SO2.
n = 2. Công thức của Y là SO2.
3. Công thức cấu tạo của SO2; SO3; H2SO4:

3.14 Hướng dẫn:
1. Số proton trung bình của một hạt nhân nguyên tử trong X+ là  = 2,2. Vậy một nguyên tố trong X+ có điện tích hạt nhân nhỏ hơn 2,2, nguyên tố đó là H (Z = 1). Ta loại trường hợp He (Z = 2) vì He là khí hiếm không tạo được hợp chất.
= 2,2. Vậy một nguyên tố trong X+ có điện tích hạt nhân nhỏ hơn 2,2, nguyên tố đó là H (Z = 1). Ta loại trường hợp He (Z = 2) vì He là khí hiếm không tạo được hợp chất.
Vậy công thức ion X+ có dạng: [A5-nHn]+. Trong đó : (5-n).ZA + n = 11.
Ta lập bảng sau:
N | 1 | 2 | 3 | 4 |
ZA (A) | 2,5 (loại) | 3 (Li) | 4 (Be) | 7 (N) |
Ta loại các trường hợp A là Li, Be vì các ion X+ tương ứng không tồn tại.
Trường hợp A là nitơ thỏa mãn vì ion amoni tồn tại. Vậy X+ là ion NH .
.

 2. Công thức electron của ion NH
2. Công thức electron của ion NH như sau:
như sau:
Công thức electron Công thức cấu tạo
3.15 Hướng dẫn:Gọi công thức của Y2- là 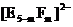 .
.
Theo bài, tổng số electron trong Y2- bằng 50 nên tổng số proton trong Y2- bằng 48.
Ta có: (5-m)ZE + mZF = 48. (1)
Ta nhận thấy:
Số proton trung bình của một hạt nhân nguyên tử trong Y2- là  = 9,6 nên E thuộc chu kỳ 2, F ở chu kỳ kế tiếp với E nên F thuộc chu kỳ 3. Mặt khác, hai nguyên tố E và F thuộc cùng một phân nhóm nên ZF - ZE = 8. (2)
= 9,6 nên E thuộc chu kỳ 2, F ở chu kỳ kế tiếp với E nên F thuộc chu kỳ 3. Mặt khác, hai nguyên tố E và F thuộc cùng một phân nhóm nên ZF - ZE = 8. (2)
Từ (1), (2) ta có: 5ZE + 8m = 48.
Ta lập bảng sau:
M | 1 | 2 | 3 | 4 |
ZE (E) | 8 (O) | 6,4 (loại) | 4,8 (loại) | 3,2 (loại) |
Vậy E là O. Từ đó suy ra F là S. Ion Y2- cần tìm là ion sunfat SO .
.
2. Công thức electron của ion SO như sau:
như sau:

Công thức electron Công thức cấu tạo
3.16 Hướng dẫn:
Gọi số mol trong mỗi phần: Fe = x mol; M = y mol.
Phần 1:
(mol): x x
(mol): y 0,5ny
Số mol H2 = 0,07 nên x + 0,5ny = 0,07.
Phần 2:
2Fe + 6H2SO4 (đặc)  Fe2(SO4)3 + 3SO2
Fe2(SO4)3 + 3SO2 + 6H2O
+ 6H2O
(mol): x 1,5x
2M + 2nH2SO4 (đặc)  M2(SO4)n + nSO2
M2(SO4)n + nSO2 + 2nH2O
+ 2nH2O
(mol): y 0,5nx
Số mol SO2 = 0,09 nên 1,5x + 0,5ny = 0,09. Vậy x = 0,04 và ny = 0,06.
Mặt khác: 56x + My = 2,78 nên My = 0,54. Vậy  hay M = 9n.
hay M = 9n.
Ta lập bảng sau:
N | 1 | 2 | 3 | |
M | 9 (loại) | 18 (loại) | 27 (nhận) |
Vậy M là Al.
3.17 Hướng dẫn:
Gọi công thức oxit là MxOy = a mol.
(mol): a ay ax
Ta có: a(Mx + 16y) = 8 và ay = 0,15. Như vậy Max = 5,6.
(mol): ax 0,5nax
Ta có: 0,5nax = 0,1 hay nax = 0,2.
Ta lập bảng sau:
N | 1 | 2 | 3 |
M | 28 (loại) | 56 (nhận) | 84 (loại) |
Vậy kim loại M là Fe.
Lập tỉ lệ:  . Vậy công thức oxit là Fe2O3.
. Vậy công thức oxit là Fe2O3.
Số oxi hóa của sắt trong oxit là +3, hóa trị của sắt là III.
3.18 Hướng dẫn:
Gọi công thức oxit là: MxOy = a mol. Ta có: a(Mx + 16y) = 4,06.
(mol): a ax ay
(mol): ay ay
Ta có: ay = 0,07. Từ đây suy ra: Max = 2,94.
(mol): ax 0,5nax
Ta có: 0,5nax = 0,0525 hay nax = 0,105.
Ta lập bảng sau:
N | 1 | 2 | 3 |
M | 28 (loại) | 56 (nhận) | 84 (loại) |
Vậy kim loại M là Fe.
Lập tỉ lệ:  . Vậy công thức oxit là Fe3O4.
. Vậy công thức oxit là Fe3O4.
3.19 Hướng dẫn:
1. Gọi hóa trị kim loại là n và số mol là a mol. Ta có: Ma = 7.
(mol): a a 0,5na
Khối lượng dung dịch sau phản ứng tăng 6,75 gam nên:
7 - 0,5na 2 = 6,75 hay na = 0,25.
2 = 6,75 hay na = 0,25.
Ta lập bảng sau:
N | 1 | 2 | 3 |
M | 28 (loại) | 56 (nhận) | 84 (loại) |
Vậy kim loại M là Fe.
2. Gọi số mol: Fe = b và FexOy = c mol. Ta có 56b + (56x + 16y)c = 6,28.
Fe + 4HNO3  Fe(NO3)3 + NO
Fe(NO3)3 + NO + 2H2O
+ 2H2O
(mol): b 4b b
3FexOy + (12x - 2y)HNO3  3xFe(NO3)3 + (3x - 2y)NO
3xFe(NO3)3 + (3x - 2y)NO + (6x - y)H2O
+ (6x - y)H2O
Ta có: 4b +  = 0,34 và b +
= 0,34 và b +  = 0,055.
= 0,055.
Từ đây tính được: b = 0,05 mol; xc = 0,045 mol và yc = 0,06 mol.
Lập tỉ lệ:  . Vậy công thức oxit là Fe3O4.
. Vậy công thức oxit là Fe3O4.
Số oxi hóa của sắt trong oxit là + , hóa trị của sắt là II và III (FeO.Fe2O3).
, hóa trị của sắt là II và III (FeO.Fe2O3).
3.20 Hướng dẫn:
Gọi a là độ dài mỗi cạnh của hình lập phương và r là bán kính của nguyên tử kim loại.
- Độ đặc khít của mạng tinh thể lập phương tâm khối.
Trong mạng thể lập phương tâm khối, mỗi quả cầu đều ở tâm của một hình lập phương và tiếp xúc trực tiếp với 8 quả cầu ở 8 đỉnh. Xét hình chữ nhật ABCD.
Theo bài: AB = a nên ta tính được: BC = a ; AC = a
; AC = a = 4r.
= 4r.

Số quả cầu trong một hình lập phương: 1 + 8 = 2.
= 2.
Tổng thể tích các quả cầu trong một hình lập phương: V = 2
 r3.
r3.
Thể tích của một hình lập phương: V' = a3 =  .
.
- Độ đặc khít của mạng tinh thể lập phương tâm diện. Xét hình chữ nhật ABCD.
 Theo bài: AB = BC = a nên ta tính được: AC = a
Theo bài: AB = BC = a nên ta tính được: AC = a = 4r.
= 4r.
Số quả cầu trong một hình lập phương: 6
 + 8
+ 8 = 4.
= 4.
Tổng thể tích các quả cầu trong một hình lập phương: V = 4
 r3.
r3.
Thể tích của một hình lập phương: V' = a3 =  .
.
3.21 Hướng dẫn:
Gọi bán kính nguyên tử Ca, Cu lần lượt là r1, r2.
Xét khối tinh thể kim loại có thể tích V = 1cm3, khi đó thể tích chiếm bởi các quả cầu kim loại là 0,74 cm3.
Gọi số nguyên tử Ca, Cu có trong 1 cm3 tinh thể kim loại là lần lượt là N1, N2:
Thể tích chiếm bởi N1 một quả cầu kim loại Ca là 0,74 cm3 nên:
N1. .
. .
.  = 0,74 cm3
= 0,74 cm3 
 .
. .
. .
.  = 0,74 cm3
= 0,74 cm3
Thể tích chiếm bởi N2 một quả cầu kim loại Cu là 0,74 cm3 nên:
N2. .
. .
.  = 0,74 cm3
= 0,74 cm3 
 .
. .
. .
.  = 0,74 cm3
= 0,74 cm3
3.22 Hướng dẫn:
1. Trong tinh thể kim loại, ion dương kim loại và nguyên tử kim loại ở các nút của mạng tinh thể. Các electron hóa trị liên kết yếu với hạt nhân nên dễ tách khỏi nguyên tử và chuyển động tự do trong mạng tinh thể, lực hút giữa các electron này và các ion dương tạo nên liên kết kim loại.
Như vậy, liên kết kim loại là liên kết được hình thành giữa các nguyên tử và ion kim loại trong mạng tinh thể do sự tham gia của các electron độc thân.
Liên kết kim loại và liên kết cộng hóa trị giống nhau là có những electron chung của các nguyên tử, nhưng electron chung trong liên kết kim loại là của tất cả những nguyên tử kim loại có mặt trong đơn chất.
Liên kết kim loại và liên kết ion đều được hình thành do lực hút tĩnh điện giữa các phần tử tích điện trái dấu, nhưng các phần tử tích điện trái dấu trong liên kết kim loại là ion dương kim loại và các electron tự do.
2. Tính có ánh kim: Trong tinh thể kim loại có các electron tự do có khả năng phản xạ hầu hết các tia sáng trong vùng nhìn thấy nên kim loại tinh khiết thường có ánh kim.
Tính dẻo: Khi tác dụng lực lên tinh thể kim loại, các nguyên tử kim loại chỉ bị xê dịch vị trí trong mạng tinh thể, liên kết kim loại vẫn được duy trì nên tinh thể kim loại chỉ bị biến dạng mà không bị phá vỡ.
Tính dẫn điện: Khi nối hai đầu dây dẫn kim loại với một hiệu điện thế, dưới tác dụng của từ trường, các electron tự do chuyển động có hướng gây ra dòng điện.
Tính dẫn nhiệt: Khi đốt nóng một đầu dây dẫn kim loại, các electron ở đó sẽ chuyển động nhiệt mạnh và di chuyển đến các vùng có nhiệt độ thấp hơn, trên đường đi chúng va chạm với các nút mạng và các electron khác, biến một phần động năng thành nhiệt năng và làm cho các vùng đó nóng dần lên, gây ra tính dẫn nhiệt của kim loại.
3.23 Hướng dẫn:
1. Gọi bán kính nguyên tử của Na là r.
Theo bài 15, trong mạng tinh thể lập phương tâm khối ta có: a = 4r.
= 4r.
2. Số nguyên tử Na trong một hình lập phương là: 1 + 8 = 2.
= 2.
Khối lượng 2 nguyên tử Na trong một hình lập phương:
M = 2 = 46u = 46.1,67.10-24 g = 7,68.10-23 g
= 46u = 46.1,67.10-24 g = 7,68.10-23 g
Thể tích của một hình lập phương:
V = a3 = (0,429.10-9 m)3 = (0,429.10-7 cm)3 = 7,89.10-23 cm3.
Vậy:  =
=  = 0,97 g/cm3. (Giá trị thực tế là 0,97g/cm3).
= 0,97 g/cm3. (Giá trị thực tế là 0,97g/cm3).
Như vậy khối lượng riêng của Na nhỏ hơn khối lượng riêng của nước (1g/cm3) nên Na nổi trên nước.
3.24 Hướng dẫn:
1. Gọi bán kính nguyên tử của Na là r.
Theo bài 15, trong mạng tinh thể lập phương tâm diện ta có: a![]() = 4r.
= 4r.
Do đó: a = ![]() = 3,51.10-8 (cm).
= 3,51.10-8 (cm).
2. Số quả cầu trong một hình lập phương: 6![]()
![]() + 8
+ 8![]() = 4.
= 4.
Khối lượng 4 nguyên tử Ni trong một hình lập phương:
M = 4![]() = 4
= 4![]()
![]() 1,67.10-24 g = 392,12.10-24 g
1,67.10-24 g = 392,12.10-24 g
Thể tích của một hình lập phương:
V = a3 = (3,51.10-8 cm)3 = 43,24.10-24 cm3.
Vậy: ![]() =
= ![]() = 9,06 g/cm3. (Giá trị thực tế là 8,90g/cm3).
= 9,06 g/cm3. (Giá trị thực tế là 8,90g/cm3).
3.25 Hướng dẫn:
1. Tính số lượng mỗi loại ion trong một hình lập phương:
Số ion Na+ = 1 (tâm) ![]() 1 + 12 (cạnh)
1 + 12 (cạnh) ![]()
![]() = 4
= 4
Số ion Cl- = 6 (mặt) ![]()
![]() + 8 (góc)
+ 8 (góc) ![]()
![]() = 4
= 4
2. Từ hình vẽ ta thấy: a = 2(![]() ) nên
) nên ![]() = 0,276 nm.
= 0,276 nm.
Kết hợp với tỉ lệ bán kính  ta tìm được:
ta tìm được:
![]() = 0,095 nm và
= 0,095 nm và ![]() = 0,181 nm.
= 0,181 nm.
F. THÔNG TIN BỔ SUNG
Vì sao cột sắt Newdeli ở ấn Độ bền vững sau hơn 15 thế kỉ?
 Khi Ấn Độ còn là thuộc địa của Anh, có một nguời Anh dự định xây dựng một nhà máy dệt tại Ấn Độ. Ông ta đặt mua máy móc ở Anh, sau hai tháng lênh đênh trên biển, chuyến tàu chở máy móc, thiết bị cho nhà máy dệt tương lai đã cập cảng an toàn. Tuy nhiên, khi kiểm tra lại, ông ta rất sửng sốt và thất vọng khi thấy toàn bộ các thiết bị, do không được bảo quản tốt trong quá trình vận chuyển đã thành phế liệu, han gỉ. May mắn cho nhà công nghiệp là ông đã mua bảo hiểm cho nhà máy của mình. Trong thời gian chờ đợi nhận được tiền bồi thường từ hãng bảo hiểm, ông đã thăm Newdeli. Điều làm ông ngạc nhiên nhất là cột sắt ở Newdeli đã tồn tại 1500 năm mà vẫn bền vững, không có dấu hiệu bị han gỉ. Vì sao cột sắt Newdeli bền vững ở ngoài trời, trong khi các thiết bị máy móc đã bị phá hủy sau hai tháng? Phải chăng có một bí mật nào đó về luyện kim, về liên kết hóa học đặc biệt của sắt ở cột này? Ông ta rất tò mò muốn biết điều bí ẩn, thần kì của cột sắt và đã bí mật đánh cắp một mẩu sắt nhỏ từ cột sắt nổi tiếng này. Ông chia mẫu sắt làm năm phần, sau đó gửi đi phân tích ở các phòng thí nghiệm hàng đầu thế giới lúc bấy giờ. Kết quả làm ông kinh ngạc, sắt để chế tạo cột là sắt nguyên chất, 99,99%. Sắt nguyên chất hầu như không bị ăn mòn hóa học, trong khi đó thép, một hợp kim của sắt với C, Mn, Si lại bị phá hủy dễ dàng. Hiện tượng trên được gọi là sự ăn mòn điện hóa học. Hiện tượng ăn mòn điện hóa học gây ra những tác hại rất lớn, phá hủy hàng triệu tấn kim loại mỗi năm, thiệt hại kinh tế lên đến hàng tỉ USD. Người ta đã nghiên cứu nhiều cách để bảo vệ kim loại. Trong đó đáng chú ý là các phương pháp bảo vệ bề mặt như sơn, mạ, lau dầu, mỡ,... và phương pháp điện hóa.
Khi Ấn Độ còn là thuộc địa của Anh, có một nguời Anh dự định xây dựng một nhà máy dệt tại Ấn Độ. Ông ta đặt mua máy móc ở Anh, sau hai tháng lênh đênh trên biển, chuyến tàu chở máy móc, thiết bị cho nhà máy dệt tương lai đã cập cảng an toàn. Tuy nhiên, khi kiểm tra lại, ông ta rất sửng sốt và thất vọng khi thấy toàn bộ các thiết bị, do không được bảo quản tốt trong quá trình vận chuyển đã thành phế liệu, han gỉ. May mắn cho nhà công nghiệp là ông đã mua bảo hiểm cho nhà máy của mình. Trong thời gian chờ đợi nhận được tiền bồi thường từ hãng bảo hiểm, ông đã thăm Newdeli. Điều làm ông ngạc nhiên nhất là cột sắt ở Newdeli đã tồn tại 1500 năm mà vẫn bền vững, không có dấu hiệu bị han gỉ. Vì sao cột sắt Newdeli bền vững ở ngoài trời, trong khi các thiết bị máy móc đã bị phá hủy sau hai tháng? Phải chăng có một bí mật nào đó về luyện kim, về liên kết hóa học đặc biệt của sắt ở cột này? Ông ta rất tò mò muốn biết điều bí ẩn, thần kì của cột sắt và đã bí mật đánh cắp một mẩu sắt nhỏ từ cột sắt nổi tiếng này. Ông chia mẫu sắt làm năm phần, sau đó gửi đi phân tích ở các phòng thí nghiệm hàng đầu thế giới lúc bấy giờ. Kết quả làm ông kinh ngạc, sắt để chế tạo cột là sắt nguyên chất, 99,99%. Sắt nguyên chất hầu như không bị ăn mòn hóa học, trong khi đó thép, một hợp kim của sắt với C, Mn, Si lại bị phá hủy dễ dàng. Hiện tượng trên được gọi là sự ăn mòn điện hóa học. Hiện tượng ăn mòn điện hóa học gây ra những tác hại rất lớn, phá hủy hàng triệu tấn kim loại mỗi năm, thiệt hại kinh tế lên đến hàng tỉ USD. Người ta đã nghiên cứu nhiều cách để bảo vệ kim loại. Trong đó đáng chú ý là các phương pháp bảo vệ bề mặt như sơn, mạ, lau dầu, mỡ,... và phương pháp điện hóa.
Ảnh bên là cột sắt Newdeli ở Ấn Độ.
Chương 4
A. TÓM TẮT LÍ THUYẾT
I. Phân loại phản ứng hóa học
Các phản ứng hóa học trong tự nhiên được chia thành hai loại, loại có sự thay đổi số oxi hóa và loại không thay đổi số oxi hóa của các nguyên tố. Loại phản ứng hóa học thứ nhất còn gọi là phản ứng oxi hóa khử.
Phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự chuyển electron giữa các chất phản ứng; hay phản ứng oxi hóa-khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của một số nguyên tố. Chất có số oxi hóa tăng sau phản ứng là chất khử, chất có số oxi hóa giảm là chất oxi hóa.
Thí dụ: 2Na + Cl2 ® 2NaCl là một phản ứng oxi hóa khử. Số oxi hóa của Na tăng từ 0 lên +1, còn số oxi hóa của Cl giảm từ 0 xuống -1.
Phản ứng oxi hóa-khử có thể chia thành ba loại là: phản ứng oxi hóa-khử thông thường, phản ứng oxi hóa -khử nội phân tử và phản ứng tự oxi hóa, tự khử.
Thí dụ: 2KMnO4 ![]() K2MnO4 + MnO2 + O2 là phản ứng oxi hóa-khử nội phân tử, trong đó chất khử và chất oxi hóa thuộc cùng một chất.
K2MnO4 + MnO2 + O2 là phản ứng oxi hóa-khử nội phân tử, trong đó chất khử và chất oxi hóa thuộc cùng một chất.
Cl2 + 2NaOH ® NaCl + NaClO + H2O là phản ứng tự oxi hóa, tự khử, trong đó chất khử và chất oxi hóa thuộc cùng một nguyên tố và cùng số oxi hóa ban đầu.
II. Số oxi hóa và cách xác định số oxi hóa
Số oxi hóa của một nguyên tố trong phân tử là điện tích của nguyên tử của nguyên tố đó, nếu giả định rằng liên kết giữa các nguyên tử trong phân tử đều là liên kết ion.
- Xác định số oxi hóa từ công thức phân tử:
Để xác định số oxi hóa từ công thức phân tử người ta dựa vào các quy tắc sau:
Quy tắc 1: Số oxi hóa của các nguyên tố trong đơn chất bằng 0.
Thí dụ: Số oxi hóa của các nguyên tố Na, Fe, H, O, Cl trong đơn chất tương ứng Na, Fe, H2, O2, Cl2 đều bằng 0.
Quy tắc 2: Trong hầu hết các hợp chất,
+ Số oxi hóa của H là +1 (trừ các hợp chất của H với kim loại như NaH, CaH2, thì H có số oxi hóa -1).
+ Số oxi hóa của O là -2 (trừ một số trường hợp như H2O2, F2O, O có số oxi hóa lần lượt là -1, +1).
Quy tắc 3: Trong một phân tử, tổng đại số số oxi hóa của các nguyên tố bằng 0. Theo quy tắc này có thể tìm số oxi hóa của một nguyên tố nào đó trong phân tử nếu biết số oxi hóa của các nguyên tố còn lại.
Thí dụ: Tìm số oxi hóa của S trong phân tử H2SO4?
Gọi số oxi hóa của S trong H2SO4 là x, ta có:
2.(+1) + 1.x + 4.(-2) = 0 ® x = +6
Vậy số oxi hóa của S là +6.
Quy tắc 4: Trong ion đơn nguyên tử, số oxi hóa của nguyên tử bằng điện tích của ion đó. Trong ion đa nguyên tử, tổng đại số số oxi hóa của các nguyên tử trong ion đó bằng điện tích của nó.
Thí dụ 1: số oxi hóa của Na, Zn, S và Cl trong các ion Na+, Zn2+, S2-, Cl- lần lượt là +1, +2, -2, -1.
Tổng đại số số oxi hóa của các nguyên tố trong các ion SO42-, MnO4-, NH4+ lần lượt là -2, -1, +1.
Thí dụ 2: Tìm số oxi hóa của N trong ion NO3- ?
Gọi số oxi hóa của N là x, ta có:
1.x + 3.(-2) = -1 Þ x = +5
Vậy số oxi hóa của N là +5.
Chú ý: Để biểu diễn số oxi hóa thì viết dấu trước, số sau, còn để biểu diễn điện tích của ion thì viết số trước, dấu sau.
Nếu điện tích là 1+ (hoặc 1-) có thể viết đơn giản là + (hoặc -), nhưng đối với số oxi hóa phải viết đầy đủ cả dấu và chữ (+1 hoặc -1).
- Xác định số oxi hóa từ công thức cấu tạo
Trong một số phân tử hay ion đa nguyên tử có cấu tạo phức tạp, số oxi hóa của các nguyên tử của cùng một nguyên tố có thể khác nhau. Việc xác định số oxi hóa theo công thức phân tử chỉ cho ta số oxi hóa trung bình, còn để xác định chính xác số oxi hóa của từng nguyên tử trong phân tử phải dựa vào công thức cấu tạo. Điều này đặc biệt giúp chúng ta có thể thiết lập các phương trình phản ứng oxi hóa - khử của hợp chất hữu cơ khi chỉ có một phần phân tử tham gia phản ứng oxi hóa - khử một cách đơn giản và dễ dàng hơn.
Nguyên tắc: coi các cặp electron đều lệch hoàn toàn về phía nguyên tử của nguyên tố có độ âm điện lớn hơn, khi đó theo số electron mà 1 nguyên tử nhường hay nhận để xác định số oxi hóa của nó.
Thí dụ:

II. Các khái niệm cần nắm vững và dấu hiệu nhận biết:
1. Sự oxi hóa (hay quá trình oxi hóa) là sự nhường electron.
2. Sự khử (hay quá trình khử) là sự nhận electron.
3. Chất oxi hóa là chất nhận electron. Chất oxi hóa còn gọi là chất bị khử.
4. Chất khử là chất nhường electron. Chất khử còn gọi là chất bị oxi hóa .
Cách nhớ: Đối với chất oxi hóa và chất khử: khử cho o nhận (o là chất oxi hóa). Đối với quá trình oxi hóa, khử: chất oxi hóa tham gia quá trình khử, chất khử tham gia quá trình oxi hóa .
5. Phản ứng oxi hóa - khử là phản ứng hóa học xảy ra trong đó có sự chuyển electron giữa các chất phản ứng.
Chú ý: Do electron không tồn tại ở trạng thái tự do nên hai quá trình oxi hóa và khử luôn xảy ra đồng thời (tức là có quá trình oxi hóa thì phải có quá trình khử và ngược lại). Tổng số electron do chất khử nhường bằng tổng số electron do chất oxi hóa nhận.
Dấu hiệu nhận biết
1. Sự oxi hóa: là sự tăng số oxi hóa
2. Sự khử: là sự giảm số oxi hóa
3. Chất oxi hóa là chất có số oxi hóa giảm.
4. Chất khử là chất có số oxi hóa tăng.
5. Phản ứng oxi hóa - khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của một hoặc nhiều nguyên tố.
IV. Dự đoán tính chất oxi hóa-khử của một hợp chất dựa vào số oxi hóa
Một nguyên tố có thể tồn tại ở nhiều trạng thái oxi hóa (số oxi hóa) khác nhau. Thí dụ:
N có thể có các số oxi hóa : -3, 0, +1, +2, +3, +4, +5.
S có thể có các số oxi hóa : -2, 0, +4, +6
Nhận xét:
- Nếu một nguyên tố tồn tại ở trạng thái oxi hóa cao nhất thì chỉ có thể giảm số oxi hóa nên chỉ có thể đóng vai trò là chất oxi hóa .
- Nếu một nguyên tố tồn tại ở trạng thái oxi hóa thấp nhất thì chỉ có thể tăng số oxi hóa nên chỉ có thể đóng vai trò là chất khử.
- Nếu một nguyên tố tồn tại ở trạng thái oxi hóa trung gian thì có thể tăng số oxi hóa hoặc có thể giảm số oxi hóa nên có thể đóng vai trò là chất oxi hóa hoặc chất khử.
Căn cứ vào trạng thái oxi hóa có thể dự đoán tính chất oxi hóa, khử của các nguyên tố trong phân tử.
Thí dụ:
Trong NH3, N có số oxi hóa -3 là số oxi hóa thấp nhất nên chỉ có thể tăng số oxi hóa tức là chỉ có thể đóng vai trò là chất khử trong các phản ứng hóa học.
Trong HNO3, N có số oxi hóa +5 là số oxi hóa cao nhất nên chỉ có thể giảm số oxi hóa tức là chỉ có thể đóng vai trò là chất oxi hóa .
Trong NO2, N có số oxi hóa trung gian là +4 nên có thể là chất oxi hóa hay chất khử.
· Cách xác định các số oxi hóa có thể có của một nguyên tố:
- Số oxi hóa âm thấp nhất của một nguyên tố chính bằng số electron tối đa mà một nguyên tử của nguyên tố đó có thể nhận để đạt được cấu hình của khí hiếm (chỉ xảy ra đối với các phi kim, các kim loại không có số oxi hóa âm).
- Thí dụ: Các nguyên tố nhóm VA (N, P,...), có 5 electron hóa trị, có thể nhận tối đa 3 electron nên số oxi hóa thấp nhất là -3.
Các nguyên tố nhóm IVA (C, Si), có 4 electron hóa trị, có thể nhận tối đa 4 electron nên số oxi hóa thấp nhất là - 4.
Các nguyên tố nhóm VIIA (F, Cl, Br, I), có 7 electron hóa trị. Có thể nhận tối đa 1 electron nên có số oxi hóa thấp nhất là -1.
Số oxi hóa dương: số oxi hóa dương cao nhất của một nguyên tố bằng số thứ tự nhóm của nó.
Thí dụ: các nguyên tố nhóm IA (Na, K,...) có 1 electron hóa trị nên có số oxi hóa dương cao nhất là +1.
Các nguyên tố nhóm VIIA (F, Cl, Br, I) có 7 electron hóa trị nên có số oxi hóa dương cao nhất có thể là +7.
Các kim loại thường chỉ có một số oxi hóa dương bằng số electron hóa trị, với Fe có 2 số oxi hóa dương là +2 và +3, Cr có 3 số oxi hóa dương là +2, +3 và +6, Cu có 2 số oxi hóa dương là +1 và +2.
V. Thiết lập phương trình của phản ứng oxi hóa - khử
Có một số cách để thiết lập phương trình của phản ứng oxi hóa - khử như phương pháp thăng bằng electron, phương pháp ion - electron, tất cả đều dựa vào nguyên lí bảo toàn khối lượng và bảo toàn điện tích. Ở đây chỉ đề cập đến phương pháp thăng bằng electron, vì đây là phương pháp đơn giản nhưng lại có thể cân bằng hầu hết các phản ứng oxi hóa khử. Các bước cân bằng theo phương pháp này như sau:
Bước 1: Xác định số oxi hóa của các nguyên tố trong phản ứng (chỉ nên biểu diễn số oxi hóa của những nguyên tố nào có sự thay đổi số oxi hóa). Từ đó dựa vào dấu hiệu nhận biết để xác định chất oxi hóa, chất khử.
Bước 2: Viết các quá trình oxi hóa và quá trình khử và cân bằng mỗi quá trình.
Bước 3: Tìm hệ số thích hợp cho chất oxi hóa và chất khử theo nguyên tắc: tổng số electron cho bằng tổng số electron nhận. Tức là đi tìm bội số chung nhỏ nhất của số electron cho và số electron nhận, sau đó lấy bội số chung đó chia cho số electron cho hoặc nhận thì được hệ số của chất khử và chất oxi hóa tương ứng.
Bước 4: Đặt hệ số của chất oxi hóa và chất khử vào phương trình phản ứng. Sau đó chọn hệ số thích hợp cho các chất không tham gia vào phản ứng oxi
hóa - khử.
Thí dụ 1: Phản ứng oxi hóa - khử đơn giản, không có môi trường
![]()
Bước 1: Xác định số oxi hóa , chất oxi hóa , chất khử
![]()
Chất oxi hóa : Fe+3 (trong Fe2O3)
Chất khử: H02
Bước 2: Viết các quá trình oxi hóa, khử
2Fe+3 + 2x3e ![]() 2Fe0 (quá trình khử)
2Fe0 (quá trình khử)
H02 ![]() 2H+ + 2x1e (quá trình oxi hóa)
2H+ + 2x1e (quá trình oxi hóa)
Chú ý: Khi chất oxi hóa (khử) có chỉ số lớn hơn 1 trong phân tử thì phải thêm hệ số (bằng chỉ số trong phân tử) vào quá trình khử (oxi hóa ) tương ứng. Ở thí dụ trên: Fe+3, H0 có chỉ số là 2 trong phân tử tương ứng Fe2O3, H2 do vậy cần thêm hệ số 2 vào quá trình khử, oxi hóa .
Bước 3: Tìm hệ số cho hai quá trình oxi hóa và khử
Bội số chung nhỏ nhất (BSCNN) = 6 do đó hệ số mỗi quá trình như sau:
1x½ 2Fe+3 + 2 x 3e ® 2Fe0
3x½ H02 ® 2H+1 +2 x 1e
Bước 4: Đặt hệ số chất oxi hóa , chất khử vào phương trình
Thí dụ 2: Phản ứng oxi hóa - khử trong đó chất oxi hóa (khử) còn có vai trò làm môi trường
![]()
Bước 1: Xác định số oxi hóa , chất oxi hóa , chất khử
![]()
Chất oxi hóa : S+6 (trong H2SO4)
Chất khử: Cu0
Bước 2: Viết quá trình oxi hóa, quá trình khử:
Cu ® Cu+2 + 2e (quá trình oxi hóa )
S+6 + 2e ® S+4 (quá trình khử)
Bước 3: Tìm hệ số cho hai quá trình oxi hóa và khử
BSCNN = 2
1 x ½ Cu ® Cu+2 + 2e
1 x ½ S+6 + 2e ® S+4
Bước 4: Đặt hệ số chất oxi hóa , chất khử vào phương trình
Do H2SO4 vừa đóng vai trò là chất oxi hóa vừa đóng vai trò là môi trường nên hệ số của nó trong phương trình không phải là hệ số của quá trình khử mà phải cộng thêm phần tham gia làm môi trường. Những hợp chất đóng hai vai trò như vậy thường cân bằng hệ số cuối cùng.
![]()
Thí dụ 3: Phản ứng oxi hóa - khử phức tạp: có nhiều chất oxi hóa hoặc khử
![]()
Bước 1: Xác định số oxi hóa, chất oxi hóa , chất khử
![]()
Chất oxi hóa : O20
Chất khử: Fe+2, S-1 (trong FeS2)
Bước 2: Viết quá trình oxi hóa, quá trình khử:
Do có hai chất khử là Fe+2, S-1 trong một phân tử nên lần lượt viết quá trình oxi hóa của chúng rồi cộng hai quá trình đó lại, chú ý đảm bảo tỉ lệ số nguyên tử trong phân tử FeS2 giữa Fe+2 và S-1 là 1:2
1 x ½2Fe+2 ® 2Fe+3 + 2e (trong Fe2O3, Fe+3 có hệ số 2)
2 x ½![]() 2S-1 ® 2S+4 + 10e (trong FeS2 , S-1 có hệ số 2)
2S-1 ® 2S+4 + 10e (trong FeS2 , S-1 có hệ số 2)
2FeS2 ® 2Fe+3 + 4S+4 + 22e
2FeS2 ® 2Fe+3 + 4S+4 + 22e (quá trình oxi hóa )
O![]() + 4e ® 2O-2 (quá trình khử)
+ 4e ® 2O-2 (quá trình khử)
Bước 3: Tìm hệ số cho hai quá trình oxi hóa và khử
BSCNN = 44
2 x ½2FeS2 ® 2Fe+3 + 4S+4 + 22e
11 x ½O![]() + 4e ® 2O-2
+ 4e ® 2O-2
Bước 4: Đặt hệ số chất oxi hóa , chất khử vào phương trình
![]()
Thí dụ 4: Phản ứng oxi hóa - khử của hợp chất hữu cơ
![]()
Bước 1: Xác định số oxi hóa , chất oxi hóa , chất khử
![]()
Chất oxi hóa : C-8/3 (trong C3H8)
Chất khử: O![]()
Nhận xét: trong phản ứng trên tất cả các nguyên tử C đều bị oxi hóa thành CO2 nên sử dụng số oxi hóa trung bình để cân bằng phương trình hóa học.
Bước 2: Viết quá trình oxi hóa, quá trình khử:
3C-8/3 ® 3C+4 + 20e (quá trình oxi hóa )
O![]() + 4e ® 2O-2 (quá trình khử)
+ 4e ® 2O-2 (quá trình khử)
Bước 3: Tìm hệ số cho hai quá trình oxi hóa và khử
BSCNN = 20
1 x ½ 3C-8/3 ® 3C+4 + 20e
5 x ½ O![]() + 4e ® 2O-2
+ 4e ® 2O-2
Bước 4: Đặt hệ số chất oxi hóa, chất khử vào phương trình
![]()
Thí dụ 5: Phản ứng oxi hóa - khử của hợp chất hữu cơ
![]()
Bước 1: Xác định số oxi hóa, chất oxi hóa , chất khử
![]()
Chất oxi hóa : C-1 và C-2 (trong CH3-CH=CH2)
Chất khử: Mn+7 (trong KMnO4)
Nhận xét: trong phản ứng trên, chỉ có hai nguyên tử C trong nhóm CH và CH2 bị oxi hóa, coi hai nguyên tử này là hai chất khử trong một hợp chất với tỉ lệ 1:1 và cân bằng phản ứng tương tự như với thí dụ 3.
Bước 2: Viết quá trình oxi hóa, quá trình khử:
C-1 + C-2 ® C0 + C-1 + 2e (quá trình oxi hóa )
Mn+7 + 3e ® Mn+4 (quá trình khử)
Bước 3: Tìm hệ số cho hai quá trình oxi hóa và khử
BSCNN = 6
3 x ½ C-1 + C-2 ® C0 + C-1 + 2e
2 x ½ Mn+7 + 3e ® Mn+4
Bước 4: Đặt hệ số chất oxi hóa, chất khử vào phương trình
![]() (H2O và KOH không tham gia vào quá trình oxi hóa khử nên cân bằng cuối cùng)
(H2O và KOH không tham gia vào quá trình oxi hóa khử nên cân bằng cuối cùng)
VI. Điều kiện xảy ra phản ứng oxi hóa khử
Khi một chất khử gặp một chất oxi hóa liệu có xảy ra phản ứng hóa học trong mọi trường hợp không? Thực tế không phải như vậy. Phản ứng oxi hóa khử xảy ra theo chiều: chất oxi hóa mạnh phản ứng với chất khử mạnh tạo ra chất oxi hóa yếu hơn và chất khử yếu hơn.
Xét hai cặp oxi hóa - khử: Oxh1/Kh1 và Oxh2/Kh2
Oxh1 + Kh2 ® Kh1 + Oxh2
Phản ứng trên xảy ra khi :
Tính oxi hóa : Oxh1 > Oxh2
Tính khử : Kh2 > Kh1
Thí dụ: Fe có tính khử mạnh hơn Cu và ion Cu2+ có tính oxi hóa mạnh hơn ion Fe2+ nên Fe đẩy được Cu ra khỏi muối của nó:
![]()
Nhận xét:
+ Từ phản ứng oxi hóa - khử có thể so sánh được khả năng oxi hóa hoặc khử của các chất.
+ Hoặc nếu biết khả năng oxi hóa - khử của các chất có thể dự đoán được một phản ứng oxi hóa - khử có xảy ra hay không.
VII. Các chất oxi hóa, chất khử thường gặp
1. Đơn chất có thể là chất oxi hóa, có thể là chất khử
- Chất oxi hóa có thể là các đơn chất phi kim như: C, N2, O2, Cl2, Br2,.. những nguyên tử có cấu hình electron lớp ngoài cùng ns2np2 (C, Si), ns2np3 (N, P), ns2np4(O, S), ns2np5 (F, Cl, Br, I). Trong đó các halogen và oxi là những đơn chất oxi hóa mạnh nhất.
- Trong các nhóm IVA, VA, VIA, VIIA tính oxi hóa giảm theo chiều tăng dần của bán kính nguyên tử.
- Chất khử điển hình là những nguyên tử có số electron ở lớp ngoài cùng chứa từ một đến ba electron. Các kim loại kiềm và kiềm thổ ở các nhóm IA và IIA, là những chất khử mạnh. Trong từng nhóm A, theo chiều tăng của điện tích hạt nhân, bán kính nguyên tử của kim loại tăng và khả năng khử của chúng cũng tăng lên. Thí dụ trong nhóm IA, tính khử yếu nhất là liti (Li) và tính khử mạnh nhất là xesi (Cs) trừ nguyên tố Fr là nguyên tố phóng xạ.
- Các phi kim cũng thể hiện tính khử như C, Si, H2.
- Có thể tóm tắt sự biến thiên tính chất oxi hóa - khử của các đơn chất trong bảng tuần hoàn theo bảng sau:
Các hợp chất có thể là chất oxi hóa hoặc là chất khử. Các chất oxi hóa như KMnO4 (kali pemanganat), K2Cr2O7 (kali đicromat), KClO3 (kali clorat), NaClO (natri hipoclorit),...Các axit như H2SO4 đặc nóng, axit HNO3. Các hợp chất chứa oxi của halogen có tính chất oxi hóa biến đổi theo chiều sau:
![]() HClO HClO2 HClO3 HClO4
HClO HClO2 HClO3 HClO4
Chiều tăng tính axit, chiều giảm của tính oxi hóa.
Chú ý:
- Với KMnO4 tùy theo môi trường xảy ra phản ứng mà Mn+7 bị khử xuống các trạng thái oxi hóa khác nhau:
+ Môi trường axit (H+): Mn+7 ® Mn+2 (tồn tại ở dạng muối Mn2+)
+ Môi trường trung tính (H2O): Mn+7 ® Mn+4 (tồn tại ở dạng MnO2)
+ Môi trường kiềm (OH-): Mn+7 ® Mn+6 (tồn tại ở dạng K2MnO4)
Thí dụ:
(1) 2KMnO4 + 10KI + 8H2SO4 ® 2MnSO4 + 5I2 + 6K2SO4 + 8H2O
(2) 2KMnO4 + 6KI + 4H2O ® 2MnO2 + 3I2 + 8KOH
(3) 2KMnO4 + H2O2 + 2KOH ® 2K2MnO4 + O2 + 2H2O
- Với HNO3 tùy theo bản chất của chất khử và nồng độ của axit mà N+5 bị khử xuống các trạng thái oxi hóa khác nhau: N+4 (NO2), N+2 (NO), N+1 (N2O), N0 (N2), N-3 (NH4NO3).
Thí dụ:
(1) Fe + 6HNO3đặc, nóng ® Fe(NO3)3 + 3NO2 + 3H2O
(2) Fe + 4HNO3loãng ® Fe(NO3)3 + NO + 2H2O
3. Các hợp chất khử như H2S, NH3, CO, ...
4. Một số chất vừa có tính oxi hóa vừa có tính khử như H2O2, SO2, ...
B. BÀI TẬP CÓ LỜI GIẢI
4.1 Cho các phản ứng hóa học dưới đây, phản ứng nào là phản ứng oxi hóa khử?
1) 2Na + 2H2O ® 2NaOH + H2
2) CO2 + Ca(OH)2 ® CaCO3¯ + H2O
3) NH4NO3 ![]() N2 + 2H2O + 1/2 O2
N2 + 2H2O + 1/2 O2
4) 2Ag + 2H2SO4 đ ![]() Ag2SO4 + SO2 + 2H2O
Ag2SO4 + SO2 + 2H2O
5) ZnO + 2HCl ® ZnCl2 + H2O
4.2 Cân bằng các phương trình phản ứng sau theo phương pháp thăng bằng electron:
1) Al + Fe2O3 ![]() Al2O3 + Fe
Al2O3 + Fe
2) Al + NaNO3 + NaOH + H2O ® NaAlO2 + NH3
3) Mg + HNO3 ® Mg(NO3)2 + N2O + NO + H2O.
Biết V![]() : VNO = 1:1
: VNO = 1:1
4) C6H5-CH3 + KMnO4 ![]() C6H5-COOK + KOH + MnO2 + H2O
C6H5-COOK + KOH + MnO2 + H2O
5) KMnO4 ![]() MnO2 + K2MnO4 + O2
MnO2 + K2MnO4 + O2
4.3 Hãy giải thích vì sao
a. NH3 chỉ thể hiện tính khử?
b. S vừa thể hiện tính oxi hóa vừa thể hiện tính khử?
c. H2SO4 chỉ thể hiện tính oxi hóa?
Cho thí dụ minh hoạ đối với mỗi trường hợp.
4.4 Cho dãy sau: Fe2+ Cu2+ Fe3+
Fe Cu Fe2+
Biết rằng, theo chiều từ trái sang phải tính oxi hóa tăng dần và tính khử giảm dần. Hỏi:
a. Fe có thể tan trong dung dịch FeCl3 và dung dịch CuCl2 được không?
b. Cu có thể tan trong dung dịch FeCl2 và dung dịch FeCl3 được không?
4.5 Xác định số oxi hóa của các nguyên tố Cl, N, Mn, C trong các chất sau:
a. HCl, Cl2, HClO, HClO2, HClO3, HClO4
b. NH3, N2, N2O, NO, N2O3, NO2, N2O5
c. KMnO4, K2MnO4, MnO2, MnSO4, Mn
d. C, CO2, Na2CO3, CO, Al4C3, CaC2, CH2O
Hãy nhận xét về số oxi hóa của một nguyên tố?
4.6 Cho 19,2 g Cu tác dụng hết với dung dịch HNO3. Tất cả lượng khí NO sinh ra đem oxi hóa thành NO2 rồi sục vào nước cùng với dòng khí oxi để chuyển hết thành HNO3. Tính thể tích oxi (đktc) đã tham gia vào quá trình trên.
4.7 Cho ag hỗn hợp A gồm FeO, CuO, Fe3O4 (có số mol bằng nhau) tác dụng vừa đủ với 250ml dung dịch HNO3 thu được dung dịch B và 3,136 lit hỗn hợp NO2 và NO có tỉ khối so với hiđro là 20,143. Tính a và CM của HNO3.
4.8 Để m g phoi bào sắt (A) ngoài không khí sau một thời gian biến thành hỗn hợp (B) có khối lượng 30g gồm Fe và các oxit FeO, Fe3O4, Fe2O3. Cho B tác dụng hoàn toàn với axit nitric thấy giải phóng ra 5,6 lit khí NO duy nhất (đktc). Tính m?
4.9 Hòa tan hết 4,431g hỗn hợp Al và Mg trong HNO3 loãng thu được dung dịch A và 1,568lit (đktc) hỗn hợp hai khí (đều không màu) có khối lượng 2,59g, trong đó một khí bị hóa nâu trong không khí.
1.Tính thành phần % về thể tích mỗi khí trong hỗn hợp.
2. Tính số mol HNO3 đã tham gia phản ứng.
3. Cô cạn dung dịch A thu được bao nhiêu gam muối khan?
4.10 Điện phân dung dịch chứa 0,02 mol FeSO4 và 0,06mol HCl với dòng điện 1,34 A trong 2 giờ(điện cực trơ, có màng ngăn). Tính khối lượng kim loại thoát ra ở katot và thể tích khí thoát ra ở anot (đktc). Bỏ qua sự hòa tan của clo trong nước và hiệu suất điện phân là 100%.
4.11 Điện phân 200ml dung dịch hỗn hợp Cu(NO3)2 và AgNO3 trong 4 giờ với dòng điện 0,402A thì kim loại trong dung dịch thoát ra hết (không có khí hiđro bay ra). Xác đinh CM của mỗi muối, biết khối lượng kim loại thu được là 3,44g.
4.12 Dung dịch X chứa HCl, CuSO4, Fe2(SO4)3. Lấy 400ml dung dịch X đem điện phân bằng điện cực trơ, cường độ dòng điện 7,72A, đến khi ở katot thu được 5,12g Cu thì dừng lại. Khi đó ở anot có 2,24 lit một chất khí bay ra (đktc). Dung dịch sau điện phân tác dụng vừa đủ với 1,25 lit dung dịch Ba(OH)2 0,2M và đun nóng dung dịch trong không khí cho các phản ứng xảy ra hoàn toàn thì thu được 56,76g kết tủa.
1. Tính thời gian điện phân.
2. Tính CM của các chất trong dung dịch ban đầu.
C. BÀI TẬP TỰ LUYỆN
4.13 Xác định số oxi hóa của các nguyên tố N, S, Zn, Cr, Na, Fe trong các chất và ion sau:
a) NH4+, Li3N, HNO2, HNO3, NO3-, KNO3
b) Na2S, H2S, S, SO2, H2SO3, SO3, H2SO4, SO42-
c) Zn, ZnCl2, ZnO, Zn2+, ZnO22-
d) Cr, CrCl2, Cr2O3, Cr2SO4, CrO3, K2Cr2O7
e) Na, NaH, NaNO3, Na2O, NaBr
f) Fe, Fe(OH)2, Fe(OH)3, FeCl3, FeS, FeO, Fe2O3
Có nhận xét gì về số oxi hóa của các kim loại?
4.14 Xác định số oxi hóa của các nguyên tố Mn, Cr, Cl, P trong các hợp chất sau: Na2MnO4, (NH4)2Cr2O4, KClO3, CaOCl2, NaClO, H3PO4, H4P2O7
4.15 Xác định số oxi hóa của các nguyên tử C trong các chất sau:
a) CH3-CH2-CH3 b) CH3-CH2-CH=CH2
c) C6H5-CH3 d) CH3-CH2-CH=O
e) CH3-COO-CH2-CH3 f) HCOOH
4.16 Xác định vai trò của các chất trong các phản ứng sau:
1) Fe + H2SO4 ® FeSO4 + H2
2) SO2 + 2NaOH ![]() Na2SO3 + H2O
Na2SO3 + H2O
3) KNO3 ![]() KNO2 + 1/2O2
KNO2 + 1/2O2
4) BaCl2 + Na2SO4 ® BaSO4¯ + 2NaCl
5) S + O2 ![]() SO2
SO2
6) 3Al + 3Cl2 ® 2Al Cl3
4.17 Phản ứng nào sau đây là phản ứng oxi hóa khử? Nếu là phản ứng oxi hóa - khử hãy chỉ rõ chất oxi hóa, chất khử, sự oxi hóa và sự khử?
1) CaO + H2O ® Ca(OH)2
2) CuO + H2 ![]() Cu + H2O
Cu + H2O
3) Fe3+ + 3OH- ® Fe(OH)3
4) Fe + NO3- + 4H+ ® Fe3+ + NO + 2H2O
5) Cl2 + 2NaOH ® NaCl + NaClO + H2O
6) Ag+ + Cl- ® AgCl¯
4.18 Trong các quá trình sau đây, quá trình nào là quá trình oxi hóa ? Quá trình khử ? Cả quá trình oxi hóa và quá trình khử? Không phải quá trình oxi hóa lẫn quá trình khử?
1) Na ® Na+ + e
2) Cl2 + 2e ® 2Cl-
3) OH- + H+ ® H2O
4) NH3 + H+ ® NH4+
5) 3Fe + 2O2 ![]() Fe3O4
Fe3O4
6) Fe2+ ® Fe3+ + e
7) MgO + 2HCl ® MgCl2 + H2O
4.19 Các loại phản ứng sau: phản ứng hóa hợp, phản ứng phân tích, phản ứng thế có phải là phản ứng oxi hóa - khử không? Cho thí dụ minh hoạ?
4.20 Thiết lập các phương trình phản ứng oxi hóa - khử sau theo phương pháp thăng bằng electron:
Phản ứng oxi hóa - khử loại không có môi trường
1) HBr + H2SO4 đặc. nóng ® Br2 + SO2 + H2O
2) Cl2 + SO2 + H2O ® HCl + H2SO4
3) C + H2SO4đ ![]() CO2 + SO2 + H2O
CO2 + SO2 + H2O
4) NH3 + O2 ![]() N2O + H2O
N2O + H2O
5) Fe3O4 + Al ![]() Al2O3 + Fe
Al2O3 + Fe
6) CuO + H2 ![]() Cu + H2O
Cu + H2O
7) NO2 + O2 + H2O ® HNO3
8) O3 + KI + H2O ® O2 + I2 + KOH
9) H2S + Cl2 + H2O ® H2SO4 + HCl
10) H2O2 + PbS ® Pb(SO4) + H2O
11) Mg + HCl ® MgCl2 + H2
4.21 Thiết lập các phương trình phản ứng oxi hóa - khử sau theo phương pháp thăng bằng electron:
Phản ứng oxi hóa - khử loại có môi trường
1) Zn + HNO3 (rất loãng) ® Zn(NO3)2 + NH4NO3 + H2O
2) Zn + HNO3 (loãng) ® Zn(NO3)2 + NO + H2O
3) Zn + HNO3 (đặc) ® Zn(NO3)2 + NO2 + H2O
4) Al + H2SO4 (đặc) ![]() Al2(SO4)3 + SO2 + H2O
Al2(SO4)3 + SO2 + H2O
5) Al + NaOH + H2O ® NaAlO2 + H2
6) Zn + NaOH + H2O ® Na2ZnO2 + H2
7) NaBr + H2SO4 + KMnO4 ® Br2 + MnSO4 + K2SO4 + H2O
8) K2Cr2O7 + FeSO4 + H2SO4 ® Cr2(SO4)3 + Fe2(SO4)3 + K2SO4 + H2O
9) H2O2 + KMnO4 + H2SO4 ® O2 + MnSO2 + K2SO4 + H2O
10) Cu + KNO3 + H2SO4 ® Cu(SO4)2 + NO + K2SO4 + H2O
11) PbO2 + HCl ![]() PbCl2 + Cl2 + H2O
PbCl2 + Cl2 + H2O
4.22 Thiết lập các phương trình phản ứng oxi hóa - khử sau theo phương pháp thăng bằng electron:
1) KClO3 ![]() KCl + O2
KCl + O2
2) KMnO4 ![]() K2MnO4 + MnO2 + O2
K2MnO4 + MnO2 + O2
3) HNO3 ![]() NO2 + O2 + H2O
NO2 + O2 + H2O
4) KNO3 ![]() KNO2 + O2
KNO2 + O2
5 ) HgO ![]() Hg + O2
Hg + O2
4.23 Viết các phương trình phản ứng oxi hóa - khử sau theo phương pháp thăng bằng electron:
1) NH4NO2 ![]() N2 + H2O
N2 + H2O
2) NH4NO3 ![]() N2O + H2O
N2O + H2O
3) NO2 + NaOH ® NaNO3 + NaNO2 + H2O
4) Cl2 + NaOH ® NaClO + NaCl + H2O
5) Cl2 + KOH ![]() KClO3 + KCl + H2O
KClO3 + KCl + H2O
6) Cl2 + Ca(OH)2 ® CaOCl2 + CaCl2 + H2O
7) K2MnO4 + H2O ® KMnO4 + MnO2 + KOH
4.24 Hoàn thành các phương trình phản ứng oxi hóa - khử sau theo phương pháp thăng bằng electron:
1) FeS2 + O2 ® Fe2O3 + SO2 (Fe : +2 trong FeS2)
2) As2S3 + HNO3 + H2O ® H2SO4 + H3AsO4 + NO2 + H2O
3) FeCu2S2 + O2 ® Fe2O3 + CuO + SO2
(Fe : +2; Cu : +1 trong FeCu2S2)
4) FeS + H2SO4 đặc, nóng ® Fe2(SO4)3 + SO2 + H2O
5) FeS2 + HNO3 ® H2SO4 + Fe(NO3)3 + NO + H2O
6) FeI2 + H2SO4 đặc, nóng ® Fe2(SO4)3 + I2 + SO2 + H2O
7) FexOy + H2SO4 đặc, nóng ® Fe2(SO4)3 + SO2 + H2O
8) Fe + HNO3 ® Fe(NO3)3 + NmOn + H2O
9) FexOy + HNO3 ® Fe(NO3)3 + NmOn + H2O
10)M2(CO3)n + HNO3 đặc, nóng ® M(NO3)m + NO2 + CO2 + H2O
4.25 Viết các phương trình phản ứng oxi hóa - khử sau theo phương pháp thăng bằng electron .
1) C2H6O + O2 ![]() CO2 + H2O
CO2 + H2O
2) CH3-CH2-OH + KMnO4 + H2SO4 ® CH3-COOH + MnSO4 + K2SO4 + H2O
3) CH2=CH2 + KMnO4 + H2O ® CH2OH-CH2OH + MnO2 + KOH
4) CH3-CºCH + KMnO4 + H2O ® CH3-CO-CH3 + MnO2 + KOH
5) C6H5-CH3 + KMnO4 + H2O ![]() C6H5-COOK + MnO2 + KOH
C6H5-COOK + MnO2 + KOH
6) CH3-CHO + AgNO3 + NH3 ![]() CH3-COOH + Ag + NH4NO3
CH3-COOH + Ag + NH4NO3
4.27 Viết các phương trình phản ứng oxi hóa - khử sau theo phương pháp thăng bằng electron:
1) Al + HNO3 ® Al(NO3)3 + NO + N2O + H2O
Với tỉ lệ thể tích ![]() = 3 : 1
= 3 : 1
2) FeO + HNO3 ® Fe(NO3)3 + NO2 + H2O
Từ phản ứng (2) có thể thiết lập ngay phản ứng (3) sau không?
3) Fe3O4 + HNO3 ® Fe(NO3)3 + NO2 + H2O
Biết Fe3O4 có thể viết dưới dạng FeO.Fe2O3
4.28 Viết các phương trình phản ứng oxi hóa - khử sau theo phương pháp thăng bằng electron:
1) H2S + SO2 ® ... + H2O
2) Al + HNO3 (loãng) ® ... + NO + H2O
3) SO2 + H2O + Br2 ® H2SO4 + ...
4) FeSO4 + HNO3 ® ... + NO2 + ...
5) S + H2SO4 ® ... + H2O
6) KMnO4 + K2SO3 + KOH ® K2SO4 + ... +...
7) K2Cr2O7 + HCl ![]() CrCl3 + ... + ... + ...
CrCl3 + ... + ... + ...
8) P + HNO3 (đặc) ![]() NO2 + ... + ...
NO2 + ... + ...
9) Mg + HNO3 ® ... + NH4NO3 + ...
4.29 Hòa tan hoàn toàn hỗn hợp FeS2, Fe3O4, FeCO3 bằng dung dịch HNO3 đặc nóng thu được dung dịch A và hỗn hợp khí B gồm NO2, CO2. Cho dung dịch A tác dụng với BaCl2 thấy xuất hiện kết tủa trắng. Hấp thụ toàn bộ hỗn hợp khí B và dung dịch NaOH dư. Viết các phương trình hóa học xảy ra.
4.30 Dẫn luồng khí H2 dư qua bình đựng hỗn hợp Fe3O4 và CuO, thu được chất rắn X. Hòa tan hoàn toàn X bằng dung dịch H2SO4 đặc nóng được dung dịch Y và khí Z duy nhất. Khí Z có khả năng làm mất màu dung dịch Br2. Viết các phương trình hóa học xảy ra.
4.31 Cho từ từ khí CO qua ống sứ đựng CuO nung nóng. Khí ra khỏi ống được hấp thụ hoàn toàn vào nước vôi trong dư thu được kết tủa B, chất rắn còn lại trong ống vào dung dịch HNO3 loãng dư thu đựoc khí NO và dung dịch C. Cho dung dịch NaOH dư và dung dịch C thu được kết tủa D. Nung D tới khối lượng không đổi thu được chất rắn E. Xác định các chất và viết phương trình hóa học xảy ra.
4.32 Hãy giải thích vì sao:
a) HNO3 chỉ có tính oxi hóa ?
b) Zn chỉ có tính khử?
c) SO2 vừa có tính oxi hóa, vừa có tính khử?
Cho thí dụ minh hoạ.
4.33 Dự đoán tính chất oxi hóa - khử của các chất sau:
Na, H2S, H2SO4, HBr, O2, Fe3+, Fe2+, SO2, NH3, Al, FeO, Cl-. Viết phương trình hóa học minh hoạ?
4.34 Hãy kể tên các chất chứa Cl có tính chất:
a) Khử
b) Oxi hóa
c) Vừa có tính oxi hóa vừa có tính khử?
4.35 Một chất oxi hóa gặp một chất khử có nhất thiết xảy ra phản ứng oxi hóa - khử hay không? Cho thí dụ minh hoạ?
4.36 Cho các cặp oxi hóa khử sau: Fe2+/Fe; Cu2+/Cu; I2/2I-; Fe3+/Fe2+; Ag+/Ag; Br2/2Br-. Theo chiều từ trái qua phải tính oxi hóa của các ion kim loại, phi kim tăng dần; tính khử của kim loại và ion phi kim giảm dần. Hãy hoàn thành các phản ứng sau (nếu có):
1) Fe + Br2 ® 2) Fe + AgNO3 ®
3) Cu + FeCl3 ® 4) Ag + CuSO4 ®
5) KI + FeCl3 ® 6) Fe(NO3)2 + AgNO3®
4.37 a) Vì sao kim loại đứng trước H trong dãy hoạt động hóa học của các kim loại có thể đẩy H2 ra khỏi dung dịch các axit.
b) Vì sao các kim loại đứng trước đẩy được các kim loại đứng sau ra khỏi muối của nó? Biết rằng trong dãy hoạt động hóa học của các kim loại, tính khử của các kim loại giảm dần từ trái sang phải.
4.38 Hãy sắp xếp các kim loại sau theo thứ tự giảm dần tính khử: Zn, Ag, Fe, Cu. Biết: Zn và Fe có thể đẩy H2 ra khỏi dung dịch axit còn Cu và Ag thì không. Zn đẩy được Fe ra khỏi muối của nó. Cu đẩy được Hg ra khỏi muối của nó, Hg đẩy được Ag ra khỏi muối của nó.
4.39 Tính nhiệt của phản ứng CO(NH2)2 (r) + H2O (l) ® CO2 (k) + 2NH3 (k), biết: nhiệt của các quá trình sau:
CO (k) + H2O(h) ® CO2 (k) + H2 (k) DH1 = - 41,3 kJ
CO (k) + Cl2 (k) ® COCl2 (k) DH2 = - 112,5 kJ
COCl2 (k) + 2NH3 (k) ® CO(NH2)2 (r) + 2HCl (k) DH3 = - 201,0 kJ
Ở điều kiện này, nhiệt tạo thành của HCl(k) là DH4 = - 92,3 kJ/mol và nhiệt hóa hơi của H2O là DH5 = 44,01 kJ/mol.
Gợi ý: Đối với loại toán này ta nên tìm cách tổ hợp từ các quá trình đã cho để loại đi các chất trung gian và được phương trình cần tính nhiệt phản ứng.
Từ các dữ kiện của bài toán ta có:
CO(NH2)2 (r) + 2HCl (k) ® COCl2 (k) + 2NH3 (k) - DH3 = + 201,0 kJ
COCl2 (k) ® CO (k) + Cl2 (k) - DH2 = + 112,5 kJ
CO (k) + H2O(h) ® CO2 (k) + H2 (k) DH1 = - 41,3 kJ
H2O (l) ® H2O (h) DH5 = 44,01 kJ
H2 (k) + Cl2 (k) ® 2HCl (k) 2. DH4 = 2.(- 92,3) = - 184,6 kJ
Cộng theo từng vế các quá trình trên và loại đi các chất trung gian, ta thu được phương trình: CO(NH2)2 (r) + H2O (l) ® CO2 (k) + 2NH3 (k) có nhiệt của phản ứng là DH = (- DH3) + (- DH2) + DH1 + DH5 + 2. DH4. Thay số có DH = 131,61 kJ.
4.40 Nhiệt tỏa ra khi đốt cháy hoàn toàn 1 mol rượu etylic ở 298K là 277,63 kJ. Hỏi khi đốt cháy hoàn toàn 1lít rượu này ở điều kiện đó thì lượng nhiệt tỏa ra là bao nhiêu ? Nếu dùng lượng nhiệt này để đun nước (nhiệt độ ban đầu là 200C) thì có thể đun sôi được bao nhiêu lít (hiệu suất của quá trình này là 70%). Cho biết khối lượng riêng của rượu là d = 0,78513 g/cm3, nhiệt dung riêng của nước là 1cal/g.độ. Khối lượng riêng của nước là 1g/cm3. Mrượu = 46,07.
Gợi ý Khối lượng rượu đem đốt là 1000 x 0,78513 = 785,13 (g).
Số mol rượu là: ![]() Þ nhiệt tỏa ra là 17,042 x 277,63 = 4731,37 (kJ); 1kcal = 4,184 kJ Û
Þ nhiệt tỏa ra là 17,042 x 277,63 = 4731,37 (kJ); 1kcal = 4,184 kJ Û ![]() .
.
Nhiệt lượng cần thiết để đun sôi 1 lit nước từ nhiệt độ ban đầu 200C là:
Q = 1000 cm3 x 1g/cm3 x 1cal/g.độ x (100 độ - 20 độ) x ![]() = 114.285,71 cal.
= 114.285,71 cal.
Vậy thể tích nước có thể được đun sôi là: ![]() = 9,9 (lit).
= 9,9 (lit).
Đáp số : 9,9 lit nước.
4.41 Phản ứng nhiệt phân là gì ? Phản ứng nhiệt phân có phải luôn luôn là phản ứng oxi hóa-khử không ? Viết phương trình phản ứng nhiệt phân KClO3, KMnO4, Fe(OH)3, CaCO3, Cu(OH)2. Những phản ứng nào thuộc loại phản ứng oxi hóa-khử? Tại sao?
4.42 Nhiệt tạo thành của H2O(h) = - 241,8 kJ.mol-1
Nhiệt hóa hơi của H2O(l) = + 44,0 kJ.mol-1
Nhiệt tạo thành của HCl(k) = - 92,3 kJ.mol-1
Nhiệt tạo thành của C2H2(k) = + 226,8 kJ.mol-1
Nhiệt tạo thành của C2H6(k) = - 84,47 kJ.mol-1
Nhiệt tạo thành của CO2(k) = - 393,5 kJ.mol-1
Hãy xác định nhiệt của các phản ứng:
- 4HCl (k) + O2 (k) ® 2H2O (l) + 2Cl2 (k)
- 4HCl (k) + O2 (k) ® 2H2O (h) + 2Cl2 (k)
- C2H2 (k) + 2H2 (k) ® C2H6 (k)
- C2H6 (k) + O2 (k) ® 2CO2 (k) + 3H2O (l)
Đáp số: a. DHa = - 202,4 kJ
b. DHb = - 114,4 kJ
c. DHc = - 311,5 kJ
d. DHd = - 1559,7 kJ
4.43 Hãy tính nhiệt của phản ứng: C (than chì) + ![]() O2 (k) ® CO (k), biết:
O2 (k) ® CO (k), biết:
C(than chì) + O2 (k) ® CO2 (k) DH1 = - 393,5 kJ
CO (k) + ![]() O2 (k) ® CO2 (k) DH1 = - 283,0 kJ
O2 (k) ® CO2 (k) DH1 = - 283,0 kJ
Đáp số: - 110,5 kJ.
D. BÀI TẬP TRẮC NGHIỆM
4.44. Hòa tan hoàn toàn 2,4g kim loại Mg vào dung dịch HNO3 loãng, giả sử chỉ thu được V lít khí N2 duy nhất (đktc). Giá trị của V là
A. 0,672 lít B.6,72lít C.0,448 lít D.4,48 lít
4.45. Cho amoniac NH3 tác dụng với oxi ở nhiệt độ cao có xúc tác thích hợp sinh ra nitơ oxit NO và nước. Phương trình hoá học là
4NH3 + 5O2 ® 4NO + 6H2O
Trong phản ứng trên, NH3 đóng vai trò
A. là chất oxi hoá. B. là chất khử.
C. là một bazơ. D. là một axit.
4.46. Cho phương trình hóa học phản ứng khử hợp chất Fe(II) bằng oxi không khí
4Fe(OH)2 + O2 + 2H2O ® 4Fe(OH)3
Kết luận nào sau đây là đúng?
A. Fe(OH)2 là chất khử, H2O là chất oxi hoá.
B. Fe(OH)2 là chất khử, O2 là chất oxi hoá.
C. O2 là chất khử, H2O là chất oxi hoá.
D. Fe(OH)2 là chất khử, O2 và H2O là chất oxi hoá.
4.47 Trong số các phản ứng sau, phản ứng oxi hoá- khử nội phân tử là
D. 2KMnO4 + 10FeSO4 + 8H2SO4 5Fe2(SO4)3 + 2MnSO4 + K2SO4
5Fe2(SO4)3 + 2MnSO4 + K2SO4
4.48 Dẫn hai luồng khí Cl2 đi qua hai dung dịch (1) KOH loãng và nguội; dung dịch (2) KOH đặc và đun nóng. Viết và cân bằng phương trình phản ứng oxi hóa khử. Nếu lượng muối KCl sinh ra trong hai dung dịch bằng nhau thì tỷ lệ thể tích clo đi qua hai dung dịch KOH (1) và (2) bằng bao nhiêu?
A. 3/5 B. 5/3 C. 4/5 D. 5/4
4.49 Cho ba phản ứng hóa học dưới đây
1) 2Na + 2H2O ® 2NaOH + H2
2) CO2 + Ca(OH)2 ® CaCO3¯ + H2O
Các phản ứng oxi hóa khử là
A. 1 B. 2 C. 1 và 2 D. 1 và 3.
4.50 Cho sơ đồ phản ứng
Fe3O4 + HNO3 ® Fe(NO3)3 + NO + H2O
Sau khi cân bằng, hệ số của phân tử các chất là phương án nào sau đây?
A. 3, 14, 9, 1, 7 B. 3, 28, 9, 1, 14
C. 3, 26, 9, 2, 13 D. 2, 28, 6, 1, 14
4.51Trong các phản ứng dưới đây, phản ứng nào không phải là phản ứng oxi hoá - khử?
A. Fe + 2HCl ® FeCl2 + H2
B. FeS + 2HCl ® FeCl2 + H2S
C. 2FeCl3 + Cu ® 2FeCl2 + CuCl2
D. Fe + CuSO4 ® FeSO4 + Cu
4.52 Trong môi trường H2SO4, dung dịch nào làm mất màu KMnO4?
A. FeCl3 B. CuCl2 C. ZnCl2 D. FeSO4
4.53 Phản ứng nào sau đây thuộc loại phản ứng tự oxi hoá, tự khử (hay tự oxi hoá - khử)?
B. S + 2H2SO4 ® 3SO2 + 2H2O
C. 4NO2 + O2 + 2H2O ® 4HNO3
D. Cl2 + 2KOH ® KClO + KCl + H2O
4.54 Phản ứng oxi hoá - khử xảy ra theo chiều tạo chất nào sau đây?
A. Chất kết tủa
B. Chất ít điện li
C. Chất oxi hoá mới và chất khử mới
D. Chất oxi hoá yếu hơn và chất khử yếu hơn
4.55 Ở phản ứng nào sau đây, H2O không đóng vai trò chất oxi hoá hay chất khử?
A. NaH + H2O ® NaOH + H2
B. 2Na + 2H2O ® 2NaOH + H2
C. 2F2 + 2H2O ® 4HF + O2
D. Al4C3 + 12H2O ® 4Al(OH)3 + 3CH4
4.56 Cho phương trình nhiệt hoá học
Hỏi lượng nhiệt toả ra là bao nhiêu khi cho 0,5 mol phân tử iot tác dụng hoàn toàn với hiđro?
A. 26,57 kJ B. 27,65 kJ
C. 26,75 kJ D. 53,14 kJ
4.57. Cho các phương trình hóa học:
1. KCl + AgNO3 ® AgCl + HNO3
2. 2KNO3 ![]() 2KNO2 + O2
2KNO2 + O2
3. CaO + C ![]() CaC2 + CO
CaC2 + CO
4. 2H2S + SO2 ® 3S + 2H2O
5. CaO + H2O ® Ca(OH)2
6. 2FeCl2 + Cl2 ® 2FeCl3
7. CaCO3 ![]() CaO + CO2
CaO + CO2
8. CuO + H2 ![]() Cu + H2O
Cu + H2O
Phương án nào sau đây chỉ gồm các phản ứng oxi hoá - khử?
A. 1, 2, 3, 4, 5 B. 2, 3, 4, 5, 6
C. 2, 3, 4, 6, 8 D. 4, 5, 6, 7, 8
4.58 Ở phản ứng oxi hoá - khử nào sau đây chỉ có sự thay đổi số oxi hoá của một nguyên tố?
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP
4.44. C | 4.45. B | 4.46. B | 4.47. C | 4.48. B |
4.49. D | 4.50. B | 4.51. B | 4.52. D | 4.53. D |
4.54. D | 4.55. D | 4.56. A | 4.57. C | 4.58. D |
4.1 Hướng dẫn:
1. 2Na + 2H2O ® 2NaOH + H2
Phản ứng trên là phản ứng oxi hóa - khử do có sự thay đổi số oxi hóa :
Na0 ® Na+1
H+1 ® H0
2.
![]()
Phản ứng trên không phải là phản ứng oxi hóa - khử do không có sự thay đổi số oxi hóa .
3.
![]()
Phản ứng trên là phản ứng oxi hóa - khử do có sự thay đổi số oxi hóa :
N-3 ® N0
N+5 ® N0
4. 2Ag + 2H2SO4 đặc ![]() Ag2SO4 + SO2 + H2O
Ag2SO4 + SO2 + H2O
Phản ứng trên là phản ứng oxi hóa - khử do có sự thay đổi số oxi hóa :
Ag0 ® Ag+1
S+6 ® S+4
5.
![]()
Phản ứng trên không phải là phản ứng oxi hóa - khử do không có sự thay đổi số oxi hóa .
4.2 Hướng dẫn:
![]()
1 x ½ 2Al0 ® 2Al+3 + 6e
1 x ½ 2Fe+3 + 6e ® 2Fe0
![]()
8x ½ Al0 ® Al+3 + 3e
3 x ½ N+5 + 8e ® N-3
3) ![]() : VNO = 1:1 Þ n
: VNO = 1:1 Þ n![]() : nNO = 1:1
: nNO = 1:1
![]()
11 x ½ Mg0 ® Mg+2 + 2e
2 x ½ N+5 + 11e ® 2N+1 + N+2
![]()
1 x½ C-3 ® C+3 + 6e
2 x½ Mn+7 + 3e ® Mn+4
![]()
1 x ½ 2O-2 ® O20 + 4e
1 x ½ 2Mn+7 + 4e ® Mn+6 + Mn+4
4.3 Hướng dẫn:
a. Trong phân tử NH3, N có số oxi hóa -3 là số oxi hóa thấp nhất nên chỉ có thể nhường electron để tăng số oxi hóa tức là chỉ thể hiện tính khử.
![]()
b. Vì S có số oxi hóa 0 là số oxi hóa trung gian nên S vừa có thể nhận electron để giảm số oxi hóa vừa có thể nhường electron để tăng số oxi hóa tức là S vừa thể hiện tính oxi hóa vừa thể hiện tính khử.
![]()
![]()
c. Trong phân tử H2SO4, H và S có số oxi hóa lần lượt là +1 và +6 đều là các số oxi hóa cao nhất của các nguyên tố tương ứng nên chỉ có thể nhận electron để giảm số oxi hóa , tức là chỉ thể hiện tính oxi hóa .
Mg + H2SO4 loãng ® MgSO4 + H2
Cu + 2H2SO4 đặc ® CuSO4 + SO2 + 2H2O
4.4 Hướng dẫn:
a. Fe có thể tan trong cả hai dung dịch FeCl3 và CuCl2 theo các phản ứng sau:
![]()
Kh OX OX (Kh)
Vì tính khử : Fe > Fe2+
tính oxi hóa : Fe3+ > Fe2+
![]()
Kh1 Oxh1 Oxh2 Kh2
Vì tính khử : Fe > Cu
tính oxi hóa : Cu2+ > Fe2+
b. Tương tự ta có:
Cu tan trong dung dịch FeCl3 nhưng không tan được trong dung dịch FeCl2.
Cu + 2FeCl3 ® CuCl2 + 2FeCl2
4.5 Hướng dẫn:
Số oxi hóa của các nguyên tố Cl, N, Mn, C lần lượt là:
a) -1, 0, +1, +3, +5, +7
b) -3, 0, +1, +2, +3, +4, +5
c) +7, +6, +4, +2, 0
d) 0, +4, +4, +2, - 4, -1, 0
Nhận xét: Số oxi hóa của clo là các số lẻ 1, 3, 5, 7.
4.6 Hướng dẫn:
Cách giải 1: Tính theo phương trình
3Cu + 8HNO3 ® 3Cu(NO3)2 + 2NO + 4H2O (1)
(mol) 0,3 0,2
2NO + O2 ® 2 NO2 (2)
(mol) 0,2 0,1
4NO2 + 2 H2O + O2 ® 4HNO3 (3)
(mol) 0,2 0,05
![]() = 22,4(0,1 + 0,05) = 3,36 lit
= 22,4(0,1 + 0,05) = 3,36 lit
Cách giải 2: Phương pháp bảo toàn e
![]() Cu - 2e ® Cu+2 4x = 0,6
Cu - 2e ® Cu+2 4x = 0,6
0,3 0,6 x = 0,15 Þ ![]() = 0,15 x 22,4 = 3,36 lit
= 0,15 x 22,4 = 3,36 lit
O2 + 4e ® 2O- 2
x 4x
4.7 Hướng dẫn:
Cách giải 1: Tính theo phương trình
Đặt số mol NO2 và NO là x và y. Ta có: x + y = 3,136: 22,4 = 0,14 (I)
M trung bình của hỗn hợp = (46x + 30y): (x + y) = 20,143 x 2= 40,286 (II)
![]() Giải hệ ta được x = 0,09 y = 0,05 x : y = 9 : 5 ta sử dụng tỷ số này để viết phương trình tổng cộng tạo ra NO và NO2
Giải hệ ta được x = 0,09 y = 0,05 x : y = 9 : 5 ta sử dụng tỷ số này để viết phương trình tổng cộng tạo ra NO và NO2
CuO + 2HNO3 ® Cu(NO3)2 + H2O (1)
24FeO + 86 HNO3 ® 24Fe(NO3)3 + 9 NO2 + 5NO +43H2O (2)
![]()
![]() 9N+5 + 9e ® 9 N+4
9N+5 + 9e ® 9 N+4
5N+5 + 15e ® 5 N+2 x 1
Fe+2 -1e ® Fe+3 x 24
Tương tự ta có:
24Fe3O4 + 230HNO3 = 72 Fe(NO3)3 + 9NO2 + 5 NO + 115H2O (3)
Theo (2) và (3) thì cứ 24 mol FeO (hoặc Fe3O4) tạo ra 14 mol hỗn hợp khí
(FeO, CuO, Fe3O4)
![]() z z z Vậy 2z 0,14mol
z z z Vậy 2z 0,14mol
Þ z = 0,12 a = 80 x 0,12 + 72 x 0,12 + 232 x 0,12 = 46,08 (g)
![]() = 0,24 + (0,12 x 86): 24 + (0,12 x 230): 24 = 1,82 (mol)
= 0,24 + (0,12 x 86): 24 + (0,12 x 230): 24 = 1,82 (mol)
Vậy ![]() = 1,82 : 0,25 = 7,28M.
= 1,82 : 0,25 = 7,28M.
Cách giải 2: Phương pháp bảo toàn e
Số mol e cho = số mol e nhận = 0,09 + (0,05 x3) = 0,24 (mol)
Þ Số mol Fe +2 = 0,24 mặt khác ![]() =
= ![]() = 0,12 (mol)
= 0,12 (mol)
a = 0,12(80 + 72 + 232) = 46,08
![]() = nNO +
= nNO + ![]() +3nFe + 2nCu = 0,14 + 3(0,12x4) + 2x0,12 =1,82 (mol)
+3nFe + 2nCu = 0,14 + 3(0,12x4) + 2x0,12 =1,82 (mol)
Vậy ![]() = 1,82 : 0,25 = 7,28M.
= 1,82 : 0,25 = 7,28M.
4.8 Hướng dẫn:
Cách giải 1: Phương pháp đại số
Các phương trình hóa học:
Fe + 1/2O2 ® FeO (1)
3Fe + 2O2 ® Fe3O4 (2)
2Fe + 3/2O2 ® Fe2O3 (3)
Fe + 4HNO3 ® Fe(NO3)3 + NO + 2H2O (4)
3FeO +10HNO3 ® 3Fe(NO3)3 + NO + 5H2O (5)
3Fe3O4 +28HNO3 ® 9Fe(NO3)3 + NO + 14H2O (6)
Fe2O3 +6HNO3 ® 2Fe(NO3)3 + 3H2O (7)
Có thể coi Fe3O4 là FeO.Fe2O3 nên khi đó có thể coi lượng B (30g) chỉ gồm
Fe, FeO, Fe2O3 với số mol tương ứng là x, y, z > 0.
Ta có : 56x + 72y + 160z = 30 (I)
nNO = x +y/3 = 0,25 hay 3x + y = 0,75 (II)
Số mol của Fe ban đầu là x + y + 2z , ta làm xuất hiện biểu thức bằng cách nhân (II) với 8 rồi cộng với (I) ta được 80(x + y + 2z) = 36
Vậy ![]() = 36: 80 = 0,45 (mol) mA = 0,45 x56 = 25,2g.
= 36: 80 = 0,45 (mol) mA = 0,45 x56 = 25,2g.
Cách giải 2: Phương pháp bảo toàn e
Bảy phương trình phản ứng trên được biểu diễn bằng các quá trình oxi hóa khử sau:
![]()
![]()
N+5 + 3e ® N+2
Do số mol NO = 0,25 (theo giả thiết), số mol Fe là x và số mol nguyên tử oxi là y, theo quy tắc bảo toàn e ta có: 3x = 2y + 0,75 (I)
Mặt khác B chỉ gồm Fe và O nên ta còn có 56x + 16y = 30 (II) giải hệ ta được
x = 0,45 và m = 0,45 x 56 = 25,2 (g).
4.9 Hướng dẫn:
1. Tính % về thể tích của hỗn hợp khí theo phương pháp đường chéo:
Hai khí đều không màu là các oxit của nitơ, trong đó khí bị hóa nâu trong không khí chính là NO (M=30) , M trung bình của hỗn hợp khí là 2,59 : 0,07= 37 Vậy khí thứ hai có M > 37 là N2O có M = 44.
![]() =37
=37
 Ta thiết lập đường chéo N2O M = 44 7
Ta thiết lập đường chéo N2O M = 44 7
NO M = 30 7
![]() : V NO = 1:1 Þ%N2O = 50% % NO = 50%
: V NO = 1:1 Þ%N2O = 50% % NO = 50%
2. Tính số mol HNO3 đã phản ứng theo phương pháp bảo toàn e:
Các quá trình oxi hóa khử:
Mg - 2e ® Mg+2
Al - 3e ® Al+3
2N+5+ 8e ® 2N+1
N+5 + 3e ®N+2
Theo định luật bảo toàn e ta có số mol e nhường = số mol e nhận. Nếu gọi n1, n2 là số mol Mg và Al ta có 2 n1 + 3 n2 = (8 x 0,035 ) + (3 x 0,035) = 11 x 0,035
biểu thức 2 n1 + 3 n2 cũng chính là số mol HNO3 tạo thành muối, ngoài ra, số mol HNO3 chuyển thành N2O và NO là 3 x 0,035.
Vậy tổng số mol HNO3 là : 14 x 0,035 = 0,49 (mol)
3. Tính khối lượng muối theo phương pháp bảo toàn khối lượng
m muối = m kim loại + ![]() = 4,431 + (11 x 0,035x 62) =28,301 (g)
= 4,431 + (11 x 0,035x 62) =28,301 (g)
4.10 Hướng dẫn:
Cách giải 1: Phương pháp thông thường
Các phương trình phản ứng điện phân: 2HCl ® H2 + Cl2 (1)
FeSO4 + H2O ® Fe + 1/2O2 + H2SO4 (2)
![]() = 0,06g =
= 0,06g = ![]() Þ t1 = 1,2 giờ t2 = 2,0 - 1,2 = 0,8 giờ
Þ t1 = 1,2 giờ t2 = 2,0 - 1,2 = 0,8 giờ
mFe = (56 : 2)x(1,34 x 0,8) : 26,8 = 1,12g
![]() = 0,03(mol),
= 0,03(mol),
![]() = 1/2 nFe = 0,01(mol)
= 1/2 nFe = 0,01(mol)
Þ V khí ở anot = 0,04 x22,4 = 0,896 lit.
Cách giải 2: Phương pháp bảo toàn electron
- Điện lượng Q = It = 1,34 x 2 = 2,68A.h
- ne = It/F = 2,68 : 26,8 = 0,1 mol
- Thứ tự điện phân ở katot
H+ + 1e ® 1/2 H2
(mol) 0,06 0,06
Fe+2 + 2e ® Fe
(mol) 0,02 Þ mFe = 0,02 x 56 = 1,12g
- Thứ tự điện phân ở anot
Cl- - 1e ® 1/2 Cl2
(mol) 0,06 0,06 0,03
H2O - 2e ® 1/2O2 + 2H+
(mol) 0,01 Þ n hỗn hợp khí = 0,03 +0,01 = 0,04
Vkhí = 0,04 x 22,4 = 0,896 (lit).
4.11 Hướng dẫn:
Cách giải 1: Phương pháp thông thường
Các phương trình điện phân:
2Cu(NO3)2 + 2H2O ® O2 + 2Cu + 4HNO3 (1)
2AgNO3 + H2O ® 1/2O2 + 2Ag + 2HNO3 (2)
Đặt x, y lần lượt là số mol của Cu và Ag, ta có 64x + 108y = 3,44 (I)
Mặt khác theo phương trình Faraday ta có 64x = ![]() =
= ![]() (II)
(II)
108y =![]() (III)
(III)
![]() Giải ra ta được x = 0,02; y =0,02 Þ
Giải ra ta được x = 0,02; y =0,02 Þ ![]() = 0,1 M
= 0,1 M
![]() = 0,1 M
= 0,1 M
Cách giải 2: Phương pháp bảo toàn electron
- Điện lượng Q = It = 0,402 x 4 = 1,608 (A.h)
- Số mol e nhận là 2x + y = 1,608: 26,8 = 0,06 (I)
Mặt khác, khối lượng hai kim loại 64x + 108y = 3,44 (II)
![]() Giải ra ta được x = 0,02; y = 0,02 Þ
Giải ra ta được x = 0,02; y = 0,02 Þ ![]() = 0,1 M
= 0,1 M
![]() = 0,1 M
= 0,1 M
4.12 Hướng dẫn:
- Quá trình điện ly: Fe2(SO4)3 ® 2Fe3+ + 3SO42-
(mol) x 2x 3x
CuSO4 ® Cu2+ + SO42-
(mol) y y y
HCl ® H+ + Cl-
(mol) z z z
- Quá trình điện phân:
Katot Anot
2Fe3+ + 2e ® 2Fe2+ 2Cl- - 2e ®Cl2
Cu2+ + 2e ® Cu
Cu thoát ra ở katot, chứng tỏ Fe3+ đã bị điện phân hết. nCu= 5,12 : 64 = 0,08 (mol)
![]() = 2,24: 22,4 = 0,1(mol),
= 2,24: 22,4 = 0,1(mol), ![]() = 0,2 x 1,25 = 0,25.
= 0,2 x 1,25 = 0,25.
- Sau khi điện phân xảy ra các phản ứng:
- Ba(OH)2 + SO42- ® BaSO4 ¯ + 2OH- (1)
(mol) (3x +y) (3x +y)
- Ba(OH)2 + 2HCl ® BaCl2 + H2O (2)
(mol) (0,25- 3x- y) 2(0,25- 3x- y)
- Fe2+ + 2OH- ® Fe(OH)2 (3)
(mol) 2x 2x 2x
- Cu2+ + 2OH- ® Cu(OH)2 (4)
(mol) (y - 0,08) (y -0,08)
4Fe(OH)2 + O2 + 2H2O ® 4Fe(OH)3 (5)
(mol) 2x 2x
1. Tính thời gian điện phân theo công thức m = ![]() (m = 7,1g, n = 2)
(m = 7,1g, n = 2)
t = ![]() =
= ![]() = 2500(s)
= 2500(s)
2. Tính CM của các chất trong dung dịch đầu, áp dụng phương pháp bảo toàn e:
- Số mol e thu ở katot = Số mol e nhường ở anot
x + 0,08 = 0,1 (mol) (I)
Theo các phản ứng (1,3, 4, 5): m kết tủa = ![]() +
+ ![]() +
+ ![]() = 56,76 (g)
= 56,76 (g)
233(3x + y) + 98(y - 0,08) + 107 .2x = 56,76 (II)
Giải ra ta được x = 0,02, y = 0,14 Þ nHCl = 0,1.2 + 2(0,25 - 3x -y) = 0,3 (mol)
CM HCl = 0,3 : 0,4 = 0,75 M, ![]() = 0,14 : 0,4 = 0,35 M
= 0,14 : 0,4 = 0,35 M
F. THÔNG TIN BỔ SUNG
A.L.LAVOADIE. Thuyết oxi hóa và sự cải tổ hóa học
A.L.Lavoadie (Antoine Laurent Lavoisier), 1745-1794, là nhà hóa học nổi tiếng của Pháp ở thế kỉ 18. Ông học tập nhiều khoa học tự nhiên, đặc biệt là vật lí và trong nghiên cứu khoa học đi sâu vào hóa học, thể hiện nhiều tài năng ngay khi còn trẻ, năm 21 tuổi được thưởng huy chương vàng của Viện Hàn Lâm khoa học Pari trong một cuộc thi với đề tài "Tìm phương pháp tốt nhất để thắp sáng đường phố của một thành phố lớn". Lavoadie là một ủy viên trong ban thầu thuế của nhà vua, đó là một tổ chức thu thuế gián tiếp. Ông rất giàu, xây dựng một phòng thí nghiệm riêng được trang bị rất đầy đủ. Ông có kế hoạch thời gian nghiêm ngặt từng ngày dành cho khoa học. Ông tổ chức chu đáo các thí nghiệm, cân đo chính xác , ghi số liệu nghiêm chỉnh, có bà Lavoadie làm cộng tác viên và thư kí riêng ghi chép đầy đủ (bà không có con). Vào cuối năm 1774 và đầu năm 1775 sau nhiều thí nghiệm về đốt cháy các chất nung kim loại, về hô hấp, ông làm thí nghiệm tách thủy ngân oxit thành thủy ngân và một khí mới rồi thử các tính chất hóa học đặc trưng của nó.
Tháng 4/1775, ông đọc báo cáo trước Viện Hàn Lâm khoa học Pari "Luận văn về bản chất của chất kết hợp với kim loại khi nung nóng và làm tăng khối lượng của chúng". Trước đây Lavoadie cũng tin thuyết nhiên tố, rồi tự tách dần ra. Ông khẳng định rằng sự tăng khối lượng của kim loại được nung bằng khối lượng của không khí giảm đi, như vậy không phải là chất lửa thay một chất bên ngoài nào khi kết hợp với kim loại mà chính là không khí. Không khí không phải là một vật thể đơn giản mà là một hỗn hợp một số khí có tính chất khác nhau.
Năm 1777, ông cống bố kết quả phân tích không khí bằng thủy ngân nung nóng, kết luận rằng không khí gồm hai khí, một khí thở được sau được gọi là oxi và một khí không thở được - sau được gọi là azot (từ chữ Latinh có nghĩa là không duy trì sự sống). Lavoadiê đặt tên oxi với ý nghĩa là nguyên tố sinh ra oxit vì ông có quan niệm sai lầm là cứ có oxi trong quá trình cháy mà vật thể nào cũng tạo thành oxit. Năm 1783, Lavoadiê xác định được thành phần của nước là hiđro và oxi.
Năm 1785, Lavoadiê đọc một báo cáo công khai công kích kịch liệt thuyết nhiên tố: "Các nhà hóa học đã sử dụng nhiên tố như một nguyên tố mơ hồ..., không được định nghĩa một cách chính xác, do đó có thể sử dụng tùy tiện cho mọi cách giải thích mà họ muốn, ... Quả thực, đó chính là thần Prôtêut luôn luôn thay đổi vẻ mặt của mình".
Rồi ông phát triển thuyết oxi hóa của mình là thuyết về vai trò của oxi trong các quá trình oxi hóa. Căn cứ vào vai trò của nguyên tố oxi trong sự nung kim loại hoặc nung quặng kim loại, thì sự tách với nhiên tố trở thành sự kết hợp với oxi và sự kết hợp nhiên tố trở thành sự tách oxi! Các biểu thức (2) và (3) bây giờ được hiểu đúng như sau:
Sắt + oxi ![]() sắt oxit
sắt oxit
Sắt oxit + cacbon ![]() sắt + cacbon oxit
sắt + cacbon oxit
Các kim loại. lưu huỳnh, photpho và những đơn chất khác đã bị thuyết nhiên tố xem là hợp chất bấy giờ, thật ra là những đơn chất, còn các oxit kim loại, khí sunfurơ SO2, axit sunfuric H2SO4 không còn là đơn chất mà là những hợp chất.
Năm 1787, Lavoadiê cho in sách "Phương pháp về danh pháp hóa học" có sự cộng tác của ba nhà hóa học Pháp có tên tuổi là G.đơMoovô, C.L.Bectolê, A.F.đơ Fuôccroa.
Trong danh pháp hóa học nhóm mấy nhà hóa học trình bày một hệ thống thuật ngữ hóa học đầu tiên hợp lí và khoa học. Trước đó mỗi nhà hóa học thường dùng hệ thống riêng của mình, bây giờ thì có một hệ thống mới, chung, dựa trên những nguyên tắc logic. Thí dụ, theo tên gọi của hợp chất có thể xác định các nguyên tố đã hóa hợp với nhau: canxi oxit được cấu tạo từ Ca và O, natri clorua từ Na và Cl. Một hệ thống tiền tố và hậu tố được đưa ra để biểu diễn tỉ lệ các nguyên tố trong thành phần của chất: cacbon đioxit giàu oxi hơn cacbon monooxit, kaliclorat có nhiều oxi hơn kaliclorit, kalipeclorat có nhiều oxi hơn cả còn kaliclorua thì không có oxi.
Năm 1789, Lavoadiê cho in sách "Khái luận về hóa học" được "trình bày theo một trật tự mới dựa vào những phát minh hiện đại". Trong công trình này ông hệ thống hóa những kiến thức tích lũy được thời bấy giờ về hóa học, trình bày bằng một ngôn ngữ giản dị, dễ hiểu, minh họa bằng nhiều hình vẽ đẹp, chính xác do bà Lavoadiê vẽ.
Trong bảng phân loại các chất, Lavoadiê chia chúng làm hai loại chất đơn giản và phức tạp, bảng các chất đơn giản được chia làm bốn nhóm: các khí đơn giản, các phi kim, các kim loại, các "đất". Ông đã sai lầm coi ánh sáng và nhiệt là hai nguyên tố, là hai thực thể vật chất.
Thuyết oxi hóa và sách khái luận về hóa học dần dần có tiếng vang lớn ở Pháp rồi lan truyền sang các nước ngoài như Đức, Hà Lan, Italia, Thụy Điển, Tây Ban Nha, Ba Lan,...rồi sang đến nước Nga.
Bị chú: Pơrili, cuối đời mình, di cư sang Mỹ sống và tiếp tục nghiên cứu khoa học, có lên tiếng phản đối Lavoadiê không trung thực, khẳng định người phát minh ra oxi là mình, năm 1774. Ông đã nhắc lại rằng tháng 10 ông đã kể cho Lavoadiê nghe là ông đã tách được thủy ngân oxit thành khí mới và thủy ngân,
Trong sách của mình năm 1789, Lavoadiê có viết "lơ lửng" về khí oxi "oxi là khí mà chúng tôi, ông Pơriti, ông Silơ và tôi đã cùng phát hiện ra gần như đồng thời". Chúng ta ngày nay có thể đánh giá như thế này? Lavoadiê không phải là người phát hiện ra oxi đầu tiên, nhưng là người có công lớn trong việc khẳng định được bản chất và ý nghĩa to lớn của oxi.
Chương 5
 NHÓM HALOGEN
NHÓM HALOGEN
A. TÓM TẮT LÍ THUYẾT
I. Cấu tạo nguyên tử, tính chất của đơn chất halogen
- Cấu hình electron nguyên tử
Flo, clo, brom và iot có cấu hình electron như sau:
F:[He]2s22p5; Cl:[Ne]3s23p5; Br :[Ar]4s24p5; I:[Kr]5s25p5
Giống nhau: Lớp electron ngoài cùng của nguyên tử các halogen có 7 electron
và có cấu hình ns2np5 (n là số thứ tự của chu kì).
Khác nhau: Từ flo qua clo đến brom và iot, bán kính nguyên tử tăng dần lớp electron ngoài cùng càng xa hạt nhân hơn, lực hút của hạt nhân đối với lớp electron ngoài cùng càng yếu hơn.
Lớp electron ngoài cùng : ở flo phân lớp 3d có năng lượng quá xa các mức năng lượng 2s và sp cho nên không thể bù đắp được bằng các phản ứng hóa học, do đó flo chỉ có mức oxi hóa +1 , ở các halogen khác có phân lớp d còn trống, như clo có các số oxi hóa +1, +3, + 5, +7.
- Các halogen có độ âm điện lớn
Các giá trị độ âm điện theo thang Paulinh:
F: 3,98 ; Cl: 3,16; Br: 2,96; I: 2,66
Trong nhóm halogen , độ âm điện giảm dần từ flo đến iot
3. Tính chất hóa học
a. Halogen là những phi kim có tính oxi hóa mạnh : halogen oxi hóa hầu hết các kim loại, nhiều phi kim và nhiều hợp chất. Khi đó nguyên tử halogen biến thành ion halogenua với số oxi hóa -1. Thí dụ với clo:
H2 + Cl2 ® 2HCl
2Fe + 3Cl2® 2FeCl3
Cu + Cl2 ® CuCl2
2NaOH + Cl2® NaCl + NaOCl + H2O Nước Gia ven.
b. Tính oxi hóa của halogen giảm dần từ flo đến iot.
c. Flo không thể hiện tính khử, các halogen khác thể hiện tính khử và tính khử tăng dần từ clo đến iot.
II. Hợp chất của halogen
- Hiđro halogenua và axit halogen hiđric
HF, HCl, HBr, HI
Hiđro halogenua là các hợp chất khí dễ tan trong nước tạo ra các dung dịch axit halogen hiđric. Từ HF đến HI tính chất axit tăng dần, HF là một axit yếu.
Từ HF đến HI tính chất khử tăng dần, chỉ có thể oxi hóa F- bằng dòng điện, trong khi đó các ion âm khác như Cl-, Br-, I- đều bị oxi hóa khi tác dụng với chất oxi hóa mạnh
- Hợp chất có oxi của halogen
Trong các hợp chất có oxi, clo, brom, iot thể hiện số oxi hóa dương còn flo thể hiện số oxi hóa âm. Do không phản ứng trực tiếp với oxi, các hợp chất có oxi của halogen được điều chế gián tiếp.
Các hợp chất có oxi quan trọng của clo như:
Nước giaven: NaCl, NaClO, H2O dùng làm chất khử trùng nước, chất tẩy trắng trong công nghiệp dệt, giấy... Nhược điểm quan trọng nhất của nước giaven là không bền, không vận chuyển đi xa được.
Điều chế nước giaven: (điện phân dung dịch muối ăn bão hòa không có màng ngăn)
2NaCl + 2H2O ![]() 2NaOH + Cl2 + H2
2NaOH + Cl2 + H2
Cl2 + 2NaOH ® NaCl + NaClO + H2O nước giaven.
Clorua vôi: CaOCl2 có công dụng tương tự nước giaven. Tuy nhiên, clorua vôi có giá thành rẻ hơn và có thể vận chuyển đi xa, do đó được sử dụng rộng rãi hơn.
Điều chế clorua vôi:
Ca(OH)2 + Cl2 ® CaOCl2 + H2O
Muối Bectole: KClO3 có tên quốc tế là kali clorat. Chất này được dùng làm diêm, điều chế oxi trong phòng thí nghiệm.
Điều chế kali clorat:
6KOH + 3Cl2 ![]() KClO3 + 5KCl + 3H2O
KClO3 + 5KCl + 3H2O
Các axit có oxi của clo:
![]() HClO HClO2 HClO3 HClO4
HClO HClO2 HClO3 HClO4
Chiều tăng tính axit và độ bền, chiều giảm của tính oxi hóa.
B. BÀI TẬP CÓ LỜI GIẢI
5.1 Nguyên tố clo có 2 đồng vị bền ![]() và
và ![]() . Nguyên tử khối trung bình của clo trong bảng tuần hoàn là 35,45. Hãy tính % các đồng vị trên.
. Nguyên tử khối trung bình của clo trong bảng tuần hoàn là 35,45. Hãy tính % các đồng vị trên.
5.2 Viết cấu hình electron nguyên tử của các nguyên tố flo, clo, brom, iot. Dựa vào cấu hình electron hãy giải thích tại sao flo luôn có số oxi hóa âm còn các nguyên tố halogen khác ngoài số oxi hóa âm còn có thể có số oxi hóa dương (+1, +3, +5, +7)?
5.3 Cấu hình ngoài cùng của nguyên tử của một nguyên tố X là 5p5 . Tỉ số nơtron và số điện tích hạt nhân bằng 1,3962 . Số nơtron của X bằng 3,7 lần số nơtron của nguyên tử nguyên tố Y . Khi cho 4,29 gam Y tác dụng với lượng dư X thì thu được 18,26 gam sản phẩm có công thức là YX.
Hãy xác định điện tích hạt nhân Z của X và Y viết cấu hình electron của X và Y.
5.4 Dùng thuốc thử thích hợp để nhận biết các dung dịch sau đây:
a) BaCl2, KBr, HCl, KI, KOH
b) KI, HCl, NaCl, H2SO4
c) HCl, HBr, NaCl, NaOH
d) NaF, CaCl2, KBr, Mgl2.
5.5 Có bốn chất bột màu trắng tương ứng nhau là : NaCl, AlCl3, MgCO3, BaCO3. Chỉ được dùng nước cùng các thiết bị cần thiết (lò nung, bình điện phân v.v...) Hãy trình bày cách nhận biết từng chất trên.
5.6 Không dùng hóa chất nào khác hãy phân biệt 4 dung dịch chứa các hóa chất sau: NaCl, NaOH, HCl, phenoltalein.
5.7 Một loại muối ăn có lẫn tạp chất CaCl2, MgCl2, Na2SO4, MgSO4, CaSO4. Hãy trình bày cách loại các tạp chất để thu được muối ăn tinh khiết.
5.8 Nguyên tố R là phi kim thuộc phân nhóm chính trong bảng tuần hoàn. Tỉ lệ giữa phần trăm nguyên tố R trong oxit cao nhất và phần trăm R trong hợp chất khí với hiđro bằng 0,5955. Cho 4,05 gam một kim loại M chưa rõ hóa trị tác dụng hết với đơn chất R thì thu được 40,05 gam muối. Xác định công thức của muối M.
5.9 Điện phân nóng chảy a gam một muối A tạo bởi kim loại và phi kim hóa trị I (X) thu được 0,896 lit khí nguyên chất (ở đktc). Hòa tan a gam muối A vào 100ml dung dịch HCl 1M cho tác dụng với dung dịch AgNO3 dư thu được 25,83 gam kết tủa. Dung dịch AgNO3 dư cho tác dụng với 100 ml dung dịch HCl 1M.
Xác định tên phi kim công thức tổng quát của muối A.
5.10 Cho 31,84 gam hỗn hợp NaX, NaY (X, Y là hai halogen ở 2 chu kỳ liên tiếp) vào dung dịch AgNO3 dư, thu được 57,34 gam kết tủa.
a) Tìm công thức của NaX, NaY.
b) Tính khối lượng mỗi muối.
5.11 Một muối được tạo bởi kim loại M hóa trị II và phi kim hóa trị I. Hòa tan m gam muối này vào nước và chia dung dịch làm hai phần bằng nhau:
- Phần I: Cho tác dụng với dung dịch AgNO3 có dư thì được 5,74 gam kết tủa trắng.
- Phần II : Nhúng một thanh sắt vào dung dịch muối, sau một thời gian phản ứng kết thúc khối lượng thanh sắt tăng lên 0,16 gam.
a) Tìm công thức phân tử của muối.
b) Xác định trị số của m.
5.12 X, Y là hai nguyên tố halogen thuộc hai chu kì liên tiếp trong hệ thống tuần hoàn. Hỗn hợp A có chứa 2 muối của X, Y với natri.
a) Để kết tủa hoàn toàn 2,2 gam hỗn hợp A, phải dùng 150 ml dung dịch AgNO3 0,2M. Tính khối lượng kết tủa thu được?
b) Xác định hai nguyên tố X, Y.
5.13 Hòa tan một muối kim loại halogenua chưa biết hóa trị vào nước để được dung dịch X. Nếu lấy 250 ml dung dịch X (chứa 27 gam muối) cho vào AgNO3 dư thì thu được 57,4 gam kết tủa. Mặt khác điện phân 125 ml dung dịch X trên thì có 6,4 gam kim loại bám ở catot. Xác định công thức muối.
5.14 Một hỗn hợp ba muối NaF, NaCl, NaBr nặng 4,82 gam hòa tan hoàn toàn trong nước được dung dịch A. Sục khí clo dư vào dung dich A rồi cô cạn hoàn toàn dung dịch sau phản ứng thu được 3,93 gam muối khan. Lấy một nửa lượng muối khan này hòa tan vào nước rồi cho phản ứng với dung dịch AgNO3 dư thì thu được 4,305 gam kết tủa. Viết các phương trình xảy ra và tính thành phần phần trăm khối lượng mỗi muối trong hỗn hợp ban đầu.
5.15 Hỗn hợp A gồm 3 muối NaCl, NaBr và NaI:
* 5,76 gam A tác dụng với lượng dư dung dịch brom, cô cạn thu được 5,29 gam muối khan.
* Hòa tan 5,76 gam A vào nước rồi cho một lượng khí clo sục qua dung dịch. Sau một thời gian, cô cạn thì thu được 3,955 gam muối khan, trong đó có 0,05 mol ion clorua.
a) Viết các phương trình phản ứng.
b) Tính thành phầm phần trăm khối lượng mỗi muối trong A.
5.16 Có hỗn hợp gồm hai muối NaCl và NaBr. Khi cho dung dịch AgNO3 vừa đủ vào hỗn hợp trên người ta thu được lượng kết tủa bằng khối lượng AgNO3 tham gia phản ứng. Tìm % khối lượng mỗi muối trong hỗn hợp ban đầu.
5.17 Hai bình cầu chứa amoniac và hiđroclorua khô. Cho từ từ nước vào đầy mỗi bình khí, thì thấy khí chứa trong hai bình tan hết. Sau đó trộn dung dịch trong hai bình đó lại với nhau. Hãy xác định nồng độ mol/l của các chất trong dung dịch sau khi trộn lẫn, biết rằng bình chứa hiđroclorua có thể tích gấp 3 lần thể tích chứa amoniac, các khí đo ở đktc.
5.18 Hỗn hợp A gồm KClO3, Ca(ClO3)2, Ca(ClO)2, CaCl2 và KCl nặng 83,68 gam. Nhiệt phân hoàn toàn A ta thu được chất rắn B gồm CaCl2, KCl và 17,472lit O2 . Cho chất rắn B tác dụng với 360ml dung dịch K2CO3 0,5M (vừa đủ) thu được kết tủa C và dung dịch D. Lượng KCl trong dung dịch D nhiều gấp ![]() lần lượng KCl có trong A.
lần lượng KCl có trong A.
a) Tính khối lượng kết tủa A.
b) Tính % khối lượng của KClO3 trong A.
5.19 Từ một tấn muối ăn có chứa 10,5% tạp chất, người ta điều chế được 1250 lit dung dịch HCl 37% (D = 1,19 g/ml) bằng cách cho lượng muối ăn trên tác dụng với axit sunfuric đậm đặc và đun nóng. Tính hiệu suất của quá trình điều chế trên.
5.20 Khi đun nóng muối kali clorat, không có xúc tác, thì muối này bị phân hủy đồng thời theo hai phương trình hóa học sau:
a) 2KCIO3 ® 2KCl + 3O2
b) 4KClO3 ® 3KClO4 + KCl
Tính : - Bao nhiêu % khối lượng bị phân hủy theo (a)
- Bao nhiêu % khối lượng bị phân hủy theo (b)
Biết rằng khi phân hủy hoàn toàn 73,5 gam kaliclorat thì thu được 33,5 gam kaliclorua.
5.21 Hòa tan 1,74 gam MnO2 trong 200ml axit clohiđric 2M. Tính nồng độ (mol/l) của HCl và MnCl2 trong dung dịch sau khi phản ứng kết thúc. Giả thiết khí clo thoát hoàn toàn khỏi dung dịch và thể tích của dung dịch không biến đổi.
5.22 Điều chế một dung dịch axit clohiđric bằng cách hòa tan 2 mol hiđroclorua vào nước. Sau đó đun axit thu được với mangan đioxit có dư. Khí clo thu được bằng phản ứng đó có đủ để tác dụng với 28 gam sắt hay không?
5.23 Hòa tan 7,8 gam hỗn hợp bột Al và Mg trong dung dịch HCl dư. Sau phản ứng khối lượng dung dịch tăng thêm 7,0 gam. Khối lượng nhôm và magie trong hỗn hợp đầu là bao nhiêu gam?
5.24 Nung mA gam hỗn hợp A gồm KMnO4 và KClO3 ta thu được chất rắn A1 và khí O2. Biết KClO3 bị phân hủy hoàn toàn theo phản ứng :
2KClO3 ![]() 2KCl + 3O2
2KCl + 3O2
còn KMnO4 bị phân hủy một phần theo phản ứng :
2KMnO4 ![]() K2MnO4 + MnO2 + O2
K2MnO4 + MnO2 + O2
Trong A1 có 0,894 gam KCl chiếm 8,132% khối lượng. Trộn lượng O2 thu được ở trên với không khí theo tỉ lệ thể tích ![]() trong một bình kín ta được hỗn hợp khí A2.
trong một bình kín ta được hỗn hợp khí A2.
Cho vào bình 0,528 gam cacbon rồi đốt cháy hết cacbon thu được hỗn hợp khí A3 gồm 3 khí, trong đó CO2 chiếm 22,92% thể tích.
a) Tính khối lượng mA.
b) Tính % khối lượng của các chất trong hỗn hợp A.
Cho biết: Không khí chứa 80% N2 và 20% O2 về thể tích.
5.25 Cho lượng axit clohiđric, thu được khi chế hóa 200 gam muối ăn công nghiệp (còn chứa một lượng đáng kể tạp chất), tác dụng với MnO2 dư để có một lượng khí clo đủ phản ứng với 22,4 gam sắt kim loại. Xác định hàm lượng % của NaCl trong muối ăn công nghiệp.
C. BÀI TẬP TỰ LUYỆN
5.26 Nêu hiện tượng và viết phương trình phản ứng nếu có khi cho HCl đặc tác dụng với các chất sau: KMnO4, KClO3 .
5.27 Nêu cách tinh chế :
a) Muối ăn có lẫn MgCl2 và NaBr
b) Axit clohiđric có lẫn axit H2SO4.
5.28 Cần bao nhiêu gam KMnO4 và bao nhiêu ml dung dịch axit clohiđric 1M để có đủ khí clo tác dụng với sắt tạo nên 16,25 gam FeCl3 ?
Đáp số: ![]()
5.29 Hòa tan 1,74 gam MnO2 trong 200 ml axit clohiđric 2M. Tính nồng độ (mol/l) của HCl và MnCl2 trong dung dịch sau khi phản ứng kết thúc. Giả thiết khí clo thoát hoàn toàn khỏi dung dịch và thể tích của dung dịch không biến đổi.
Đáp số: ![]()
5.30 Hoàn thành sơ đồ biến hóa sau :

5.31 Điện phân nóng chảy một muối clorua kim loại hóa trị I thu được ở catot 6,24 gam kim loại và ở anot 1,792 lit khí (đktc).
a) Xác định công thức phân tử muối.
b) Cho chất khí sinh ra tác dụng với H2 trong điều kiện ánh sáng được sản phẩm X. Hòa tan X vào nước để có dung dịch 1. Đốt cháy kim loại trên, cho sản phẩm sinh ra hòa tan vào nước để có dung dịch 2. Viết các phương trình phản ứng. Cho 1 mẫu quỳ tím vào dung dịch 1, kế đó thêm vào từ từ dung dịch 2. Quan sát hiện tượng và giải thích.
Đáp số: Công thức muối là KCl.
5.32 Hòa tan 5,37 gam hỗn hợp gồm 0,02 mol AlCl3 và một muối halogenua của kim loại M hóa trị II vào nước, thu được dung dịch A. Cho dung dịch A tác dụng vừa đủ với 200 ml dung dịch AgNO3, thu được 14,35 gam kết tủa. Lọc lấy dung dịch cho tác dụng với NaOH dư, thu được kết tủa B. Nung B đến khối lượng không đổi được 1,6 gam chất rắn.
Xác định công thức phân tử muối halogenua kim loại M.
Đáp số: Công thức phân tử của muối là CuCl2.
5.33 Có hỗn hợp NaI và NaBr. Hòa tan hỗn hợp trong nước. Cho brom dư vào dung dịch. Sau khi phản ứng thực hiện xong, làm bay hơi dung dịch, làm khô sản phẩm thì thấy khối lượng sản phẩm nhỏ hơn khối lượng hỗn hợp 2 muối ban đầu là m gam.
Hòa tan sản phẩm trong nước và cho khí clo đi qua cho đến dư. Làm bay hơi dung dịch và làm khô chất còn lại, người ta thấy khối lượng chất thu được nhỏ hơn khối lượng muối phản ứng là m gam.
Xác định % về khối lượng của NaBr trong hỗn hợp đầu.
Đáp số: % NaBr = 3,7%; %NaI = 96,3%
5.34 Đem điện phân 200 ml dung dịch NaCl 2M (d = 1,1g/ml) với điện cực bằng than có màng ngăn xốp và dung dịch luôn luôn được khuấy đều. Sau một thời gian ở catot thoát ra 22,4 lit khí đo ở điều kiện 200C, 1atm. Hợp chất chứa trong dung dịch sau khi kết thúc điện phân là chất gì? Xác định C% của nó.
Đáp số: C%NaOH = 8,32%
5.35 Điện phân nóng chảy a gam muối A tạo bởi kim loại M và halogen X ta thu được 0,96 gam kim loại M ở catốt và 0,896 lit khí (ở đktc) ở anôt. Mặt khác hòa tan a gam muối A vào nước, sau đó cho tác dụng với AgNO3 dư thì thu được 11,48 gam kết tủa.
Hỏi X là halogen nào ?
Đáp số: X là clo
5.36 Điện phân 200 ml dung dịch KCl 1M (d=1,15g/ml) trong bình điện phân có màng ngăn xốp với cường độ dòng điện I=20A, sau thời gian t khí thoát ra ở catốt là 1,12 lit. Tính nồng độ % của các chất trong dung dịch sau điện phân.
(Coi thể tích dung dịch không thay đổi và nước chưa bị điện phân)
Đáp số: C KOH = 2,474% , CKCl = 3,29% .
5.37 Hỗn hợp A gồm: NaOH, Na2CO3 và Na2SO4. Lấy 1 gam A hòa tan vào nước rồi thêm dung dịch BaCl2 cho đến dư, thu được kết tủa B và dung dịch C. Thêm từ từ dung dịch HCl vào dung dịch C cho đến khi được dung dịch trung tính, cần dùng 24 ml dung dịch HCl 0,25M. Mặt khác, 2 gam A tác dụng với dung dịch HCl dư, sinh ra được 0,224 lit khí (đktc).
a) Xác định thành phần phần trăm từng chất trong hỗn hợp A.
b) Tính thể tích dun dịch HCl 0,5M phản ứng vừa đủ với 0,5 gam A.
c) Tính thể tích dung dịch HCl 0,5M tác dụng với kết tủa B.
Đáp số: a) Thành phần của A: 53% Na2CO3 ; 24% NaOH; 23% Na2SO4.
b) 16ml dung dịch HCl.
c) 20ml dung dịch HCl 0,5M.
5.38 Dung dịch X được tạo thành bằng cách hòa tan 3 muối KCl, FeCl3, BaCl2. Nếu cho 200 ml dung dịch X phản ứng vừa đủ với 100 ml dung dịch Na2SO4 1M , hoặc với 150 ml dung dịch NaOH 2M; hoặc với 300 ml dung dịch AgNO3 2M . Trong mỗi trường hợp đều thu được kết tủa lớn nhất.
a) Tính nồng độ của mỗi muối trong dung dịch X.
b) Tính khối lượng muối khan thu được khi cô cạn 200 ml dung dịch X.
Đáp số: [BaCl2]=[KCl]=[FeCl3]=0,5M; m=44,5g.
5.39 Hòa tan m gam hỗn hợp gồm NaBr và NaI vào nước được dung dịch A. Cho A phản ứng với brom dư sau đó cô cạn dung dịch thu được duy nhất một muối khan B có khối lượng (m - 47) gam. Hòa tan B vào nước và cho tác dụng với clo dư sau đó cô cạn dung dịch thu được duy nhất một muối khan C có khối lượng (m-89) gam. Viết các phương trình phản ứng hóa học và tính % khối lượng của mỗi muối trong hỗn hợp ban đầu.
Đáp số: 40,71% NaBr và 59,29%NaI
5.40 Một khoáng vật có công thức tổng quát là: aKCl.bMgCl2.cH2O. Nung 27,75 gam khoáng vật trên đến khối lượng không đổi thấy khối lượng chất rắn giảm 10,8 gam. Hòa tan chất rắn đó vào trong nước rồi cho tác dụng với AgNO3 dư thì thu được 43,05 gam kết tủa. Lập công thức của khoáng vật trên.
Đáp số: KCl.MgCl2.6H2O.
5.41 Một dung dịch là hỗn hợp các muối NaCl, NaBr, NaI. Sau khi làm khô 20ml dung dịch này thu được 1,732 gam chất rắn. Lấy 20ml dung dịch muối phản ứng với brom rồi làm bay hơi thu được 1,685 gam chất rắn khô. Sau đó cho clo tác dụng với 120ml dung dịch trên, sau khi bay hơi thu được 1,4625 gam kết tủa khô.
a) Tính nồng độ CM của từng muối trong dung dịch.
b) Tính khối lượng brom và iot có thể điều chế được từ 1m3 dung dịch.
Đáp số: NaCl 1M; NaBr 0,2M; NaI 0,05M.
![]()
5.42 Chia 8,84 gam hỗn hợp MCl và BaCl2 thành hai phần bằng nhau. Hòa tan phần 1 vào nước rồi cho phản ứng với AgNO3 dư thu được 8,61 gam kết tủa. Đem điện phân nóng chảy phần 2 đến hoàn toàn thu được V ml khí X ở 27,3oC và 0,88 atm. Nếu số mol MCl chiếm 80% số mol trong hỗn hợp, xác định kim loại M và tính thành phần % khối lượng hỗn hợp đầu. Tính V.
Đáp số: Kim loại là Na

V = 0,84lit
5.43 Từ một tấn muối ăn có chứa 5% tạp chất, người ta điều chế được 1250 lit dung dịch HCl 37% (d = 1,19 g/ml) bằng cách cho lượng muối ăn trên tác dụng với axit sunfuric đậm đặc và đun nóng. Tính hiệu suất của quá trình điều chế trên.
Đáp số: H% = 92,85%
D. BÀI TẬP TRẮC NGHIỆM
5.44 Phản ứng nào sau đây được dùng để điều chế clo trong phòng thí nghiệm ?
B. 2NaCl + 2H2O  H2 + 2NaOH + Cl2
H2 + 2NaOH + Cl2
C. MnO2 + 4HClđặc  MnCl2 + Cl2 + 2H2O
MnCl2 + Cl2 + 2H2O
D. F2 + 2NaCl ® 2NaF + Cl2
5.45 Clorua vôi là muối của kim loại canxi với 2 loại gốc axit là clorua Cl- và hipoclorit ClO-. Vậy clorua vôi gọi là muối gì?
A. Muối trung hoà B. Muối kép
C. Muối của 2 axit D. Muối hỗn tạp
5.46 Khí Cl2 điều chế bằng cách cho MnO2 tác dụng với dd HCl đặc thường bị lẫn tạp chất là khí HCl. Có thể dùng dd nào sau đây để loại tạp chất là tốt nhất?
A. Dd NaOH B. Dd AgNO3 C. Dd NaCl D. Dd KMnO4
5.47 Dùng loại bình nào sau đây để đựng dung dịch HF?
A. Bình thuỷ tinh màu xanh B. Bình thuỷ tinh mầu nâu
C. Bình thuỷ tinh không màu D. Bình nhựa teflon (chất dẻo)
5.48 Chất nào sau đây chỉ có tính oxi hoá, không có tính khử?
A. F2 B. Cl2 C. Br2 D. I2
5.49 Có 4 chất bột màu trắng là vôi bột, bột gạo, bột thạch cao (CaSO4.2H2O) bột đá vôi (CaCO3). Chỉ dùng chất nào dưới đây là nhận biết ngay được bột gạo?
A. Dung dịch HCl B. Dung dịch H2SO4 loãng
C. Dung dịch Br2 D. Dung dịch I2
5.50 Đổ dung dịch chứa 1g HBr vào dd chứa 1g NaOH. Dung dịch thu được làm cho quỳ tím chuyển sang màu nào sau đây?
A. Màu đỏ B. Màu xanh
C. Không đổi màu D. Không xác định được
5.51 Phản ứng nào sau đây được dùng để điều chế khí hiđro clorua trong phòng thí nghiệm?
B. Cl2 + H2O ® HCl + HClO
C. Cl2 + SO2 + 2H2O ® 2HCl + H2SO4
5.52 Trong các phản ứng hoá học, để chuyển thành anion, nguyên tử của các nguyên tố halogen đã nhận hay nhường bao nhiêu electron?
A. Nhận thêm 1 electron B. Nhận thêm 2 electron
C. Nhường đi 1 electron D. Nhường đi 7 electron
5.53 Clo không phản ứng với chất nào sau đây?
A. NaOH B. NaCl C. Ca(OH)2 D. NaBr
5.54 Nhận định nào sau đây sai khi nói về flo?
A. Là phi kim loại hoạt động mạnh nhất
B. Có nhiều đồng vị bền trong tự nhiên
C. Là chất oxi hoá rất mạnh
D. Có độ âm điện lớn nhất
5.55 Những hiđro halogenua có thể thu được khi cho H2SO4 đặc lần lượt tác dụng với các muối NaF, NaCl, NaBr, NaI là
A. HF, HCl, HBr, HI B. HF, HCl, HBr và một phần HI
C. HF, HCl, HBr D. HF, HCl .
5.56 Đốt nóng đỏ một sợi dây đồng rồi đưa vào bình khí Cl2 thì xảy ra hiện tượng nào sau đây?
A. Dây đồng không cháy
B. Dây đồng cháy yếu rồi tắt ngay
C. Dây đồng cháy mạnh, có khói màu nâu và màu trắng.
D. Dây đồng cháy âm ỉ rất lâu
5.57 Hỗn hợp khí nào sau đây có thể tồn tại ở bất kì điều kiện nào?
A. H2 và O2 B. N2 và O2 C. Cl2 và O2 D. SO2 và O2
5.58 Dãy nào sau đây sắp xếp đúng theo thứ tự giảm dần tính axit của các dung dịch hiđro halogenua?
A. HI > HBr > HCl > HF B. HF > HCl > HBr > HI
C. HCl > HBr > HI > HF D. HCl > HBr > HF > HI
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP
5.44. C | 5.45. D | 5.46. C | 5.47. D | 5.48. A |
5.49. D | 5.50. B | 5.51. D | 5.52. A | 5.53. B |
5.54. B | 5.55. D | 5.56. C | 5.57. C | 5.58. A |
5.1 Hướng dẫn:
Áp dụng công thức:
![]()
Trong đó ![]() là nguyên tử khối trung bình
là nguyên tử khối trung bình
a, b là % đồng vị
A, B là nguyên tử khối của đồng vị
Theo đầu bài ta có hệ phương trình sau:

Giải hệ phương trình ta có :
a = 77,5%
b = 22,5%
5.2 Hướng dẫn:
Nguyên tố | Cấu hình electron |
F | 2s22p5 |
Cl | 3s23p5 |
Br | 4s24p5 |
I | 5s25p5 |
Flo luôn có số oxi hóa âm bởi vì: Lớp ngoài cùng của nguyên tử flo không có obitan d, còn mức 2p và mức 3s chênh lệch năng lượng quá cao nên flo không có trạng thái kích thích để hình thành số oxi hóa dương. Mặt khác flo có độ âm điện lớn nhất nên ngay cả số oxi hóa +1 cũng không xuất hiện.
Các nguyên tố halogen khác ngoài số oxi hóa âm còn có thể có số oxi hóa dương(+1, +3, +5, +7) bởi vì: các electron ns và np có khả năng bị kích thích chuyển sang nd,
+1 | ¯ | ¯ | ¯ | | |||||||
s | p | d | |||||||||
+3 | ¯ | ¯ | | | | ||||||
s | p | d | |||||||||
+5 | ¯ | | | | | | |||||
s | p | d | |||||||||
+7 | | | | | | | | ||||
s | p | d |
5.3 Hướng dẫn: Cấu hình electron của nguyên tố X là:
1s22s22p63s23p64s23d104p65s24d105p5
Từ đó rút ra ZX = 53 = pX (số proton)
Theo đầu bài ta có: ![]() (số nơtron)
(số nơtron)
AX = pX + nX = 53 + 74 = 127
mặt khác : ![]()
phản ứng của X và Y:
Y + X ® YX
4,29 18,26
AY MYX
![]()
![]()
Vậy cấu hình electron của nguyên tố Y là:
1s22s22p63s23p64s1
Vậy X là iot và Y là kali.
5.4 Hướng dẫn:
a) Dùng quỳ tím nhận biết HCl, KOH.
Dùng dung dịch H2SO4 nhận biết BaCl2 còn lại KI, KBr.
Dùng khí Cl2 phân biệt các dung dịch KI và KBr.
b) Dùng quỳ tím nhận biết HCl, H2SO4.
Dùng dung dịch BaCl2 phân biệt HCl và H2SO4.
Dùng dung dịch AgNO3 để phân biệt dung dịch KI và NaCl (AgI¯ màu vàng tươi; AgCl¯ màu trắng).
Hoặc đốt : KI ngọn lửa màu tím; NaCl ngọn lửa màu vàng.
c) Dùng quỳ tím nhận biết dung dịch các dung dịch NaOH, HCl, HBr.
Dùng Cl2 phân biệt HCl và HBr hoặc dùng AgNO3 cũng phân biệt được AgBr¯ (màu vàng) và AgCl¯ (màu trắng).
d) Cho bốn mẫu thử tác dụng với dung dịch Na2CO3 có hai mẫu thử có phản ứng tạo kết tủa là CaCl2 và MgI2.
Phân biệt hai mẫu thử CaCl2 và MgI2 bằng Cl2.
Còn lại phân biệt NaF và KBr cũng bằng Cl2.
5.5 Hướng dẫn:
Lấy từng lượng muối nhỏ để làm thí nghiệm:
- Hòa tan vào H2O, tạo thành 2 nhóm:
+ Nhóm I : Tan trong H2O là NaCl và AlCl3
+ Nhóm II : Không tan là MgCO3 và BaCO3
- Điện phân dung dịch các muối nhóm I (có màng ngăn) :
2NaCl + 2H2O ![]() 2NaOH + Cl2 + H2
2NaOH + Cl2 + H2
2AlCl3 +6H2O ![]() 2Al(OH)3¯ + 3Cl2 + 3H2
2Al(OH)3¯ + 3Cl2 + 3H2
Khi kết thúc điện phân, ở vùng catot của bình điện phân nào có kết tủa keo xuất hiện, đó là bình chứa muối AlCl3, bình kia là NaCl.
- Thu khí H2 và Cl2 thực hiện phản ứng :
H2 + Cl2 ® 2HCl
Hòa tan muối nhóm II vào dung dịch HCl :
MgCO3 + 2HCl ® MgCl2 + CO2 + H2O
BaCO3 + 2HCl ® BaCl2 + CO2 + H2O
Điện phân dung dịch NaCl (có màng ngăn) để thu dung dịch NaOH.
Dùng dung dịch NaOH để phân biệt muối MgCl2 và BaCl2. Từ đó tìm được MgCO3 và BaCO3 :
MgCl2 + 2NaOH ® Mg(OH)2¯ + 2NaCl
BaCl2 + 2NaOH ® Ba(OH)2 + 2NaCl
5.6 Hướng dẫn:
- Ta nhỏ lần lượt một mẫu thử vào ba mẫu thử còn lại đến khi nào thấy 2 mẫu thử nhỏ vào nhau biến thành màu hồng thì cặp đó là dung dịch NaOH và phenolphtalein. Còn lại là dung dịch NaCl và dung dịch HCl. Chia ống nghiệm có màu hồng thành hai phần. Lấy hai mẫu thử đựng dung dịch NaCl và dung dịch HCl, mỗi mẫu thử đổ vào một ống nghiệm màu hồng, mẫu nào làm màu hồng mất đi là dung dịch HCl (vì axit trung hòa hết NaOH, nên môi trường trung tính, phenolphtalein không đổi màu). Ta phân biệt được dung dịch HCl và dung dịch NaCl.
- Ống nghiệm từ màu hồng chuyển sang không màu, lúc này chỉ chứa NaCl và phenolphtalein. Ta dùng nó để nhận biết dung dịch NaOH bằng cách nhỏ vào một trong hai ống nghiệm chưa biết, ống nghiệm nào biến thành màu hồng đó là NaOH, ống còn lại là phenolphtalein.
5.7 Hướng dẫn:
- Hòa tan muối ăn vào nước cất.
- Thêm BaCl2 dư để loại ion SO42- ở dạng BaSO4 kết tủa trắng.
Phương trình phản ứng:
BaCl2 + Na2SO4 ® BaSO4¯ + 2NaCl
BaCl2 + MgSO4 ® BaSO4¯ + MgCl2
BaCl2 + CaSO4 ® BaSO4¯ + CaCl2
- Lọc bỏ kết tủa BaSO4.
- Thêm Na2CO3 dư để loại ion Mg2+, Ca2+, Ba2+dư
MgCl2 + Na2CO3 ® 2NaCl + MgCO3¯
CaCl2 + Na2CO3 ® 2NaCl + CaCO3¯
BaCl2 + Na2CO3 ® 2NaCl + BaCO3¯
- Lọc bỏ kết tủa MgCO3, CaCO3, BaCO3.
- Thêm dung dịch HCl để loại bỏ Na2CO3 dư
Na2CO3 + 2HCl ® 2NaCl + CO2 + H2O
- Cô cạn dung dịch ta thu được muối ăn tinh khiết.
5.8 Hướng dẫn:
Đặt hóa trị của R là x và nguyên tử lượng là R
Hợp chất với oxi có công thức R2Ox
Hợp chất với hiđro có công thức RH8-x
Theo đầu bài : 
Þ ![]()
Þ ![]()
X | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
R | -5,53 | 8,72 | 22,97 | 37,22 | 51,47 | 65,72 | 79,97 |
nghiệm | loại | loại | loại | loại | loại | loại | nhận |
Vậy R là brom, viết phương trình M tác dụng với Br2, lập phương trình tìm công thức muối
M + ![]() Br2 ® MBry
Br2 ® MBry
theo ptpư: M gam (M + y.80) gam
theo đầu bài: 4,05 gam 40,05 gam
Þ 40,05.M = 4,05.(M + y.80)
Þ M = 9y
Y | 1 | 2 | 3 |
M | 9 | 18 | 27 |
nghiệm | loại | loại | nhận |
Vậy M là nhôm
Þ Công thức của muối là AlBr3
Hướng dẫn:
Kí hiệu M, X lần lượt là khối lượng nguyên tử của kim loại M và phi kim X, n là hóa trị của kim loại.
![]() (1)
(1)
(mol) x x ![]()
MXn + nAgNO3 ® M(NO3)n + nAgX¯ (2)
(mol) x mol nx mol
HCl + AgNO3 ® AgCl¯ + HNO3
(mol) 0,1´1 = 0,1 0,1
Khối lượng kết tủa AgX là : 25,83 - (0,1 ´ 143,5) = 11,48 (g)
![]() có trong muối A :
có trong muối A : ![]() (mol)
(mol)
nAgX thu được (phương trình 2) = 0,08 (mol)
![]()
X = 143,5 - 108 = 35,5 ; X là Cl
Vậy muối A có công thức tổng quát MCl.
5.10 Hướng dẫn:
a) Phương trình phản ứng của NaX và NaY với AgNO3.
NaX + AgNO3 ® AgX¯ + NaNO3
a a
NaY + AgNO3 ® AgY¯ + NaNO3
b b
- Lập hệ phương trình (gọi số mol NaX: amol; số mol NaY: bmol)

![]()
Vì ![]()
Þ X = 80 < 80,13 nên X là brom và Y = 127 > 83,13 nên Y là iot.
Công thức của 2 muối là: NaBr và NaI.
b) Þ mNaBr = 0,28 ´ 103 = 28,84 (g)
mNaI = 0,02 ´ 150 = 3 (g)
5.11 Hướng dẫn:
a) Gọi công thức phân tử muối của kim loại M hóa trị II và phi kim X hóa trị I là MX2.
MX2 + 2AgNO3 ® 2AgX¯ + M(NO3)2
MX2 + Fe ® M¯ + FeX2
Dựa vào phương trình phản ứng rút ra:
![]()
Vì X là phi kim hóa trị I và muối AgX là kết tủa trắng Þ X là nguyên tố halogen trừ F.
Nguyên tố halogen:
Cl | Br | I | |||||
MX : | 35,5 | 80 | 127 | ||||
MM : | 64 | 66,5 | 69,1 | ||||
Chọn | loại | loại |
Chọn MX = 35,5 Þ X là Cl và MM = 64 Þ M là Cu
Công thức phân tử muối là CuCl2.
b) Số mol của 1/2 lượng muối ban đầu là:
![]()
(a là số mol MgX2 trong 1/2 lượng muối ban đầu)
Khối lượng muối CuCl2 ban đầu:
m = 2 ´ (0,02 ´ 135) = 5,4 (g)
5.12 Hướng dẫn:
a) ![]()
Các phương trình phản ứng:
NaX + AgNO3 ® NaNO3 + AgX¯
NaY + AgNO3 ® NaNO3 + AgY¯
Áp dụng định luật bảo toàn khối lượng ta có:
mA + ![]() =
= ![]() + mkết tủa
+ mkết tủa
2,2 + 0,03.170 = 0,03.85 + mkết tủa
mkết tủa = 4,75 (g)
b) Đặt X > ![]() > Y
> Y
Þ Na![]() + nAgNO3 ® NaNO3 + Ag
+ nAgNO3 ® NaNO3 + Ag![]() ¯
¯
![]()
![]()
Þ ![]() = 158,3 -108 = 50,3
= 158,3 -108 = 50,3
X và Y là các halogen liên tiếp, vậy đó phải là brom (M = 80) và clo (M = 35,5)
5.13 Hướng dẫn:
Đặt kí hiệu kim loại là B.
Đặt kí hiệu halogen là X.
Công thức của muối sẽ là BXn
BXn + AgNO3 ® nAgX¯ + B(NO3)n
27g 57,4g
Þ 13,5g 28,7
BXn ![]() B + nX
B + nX
13,5g 6,4g 7,1g
Trong 13,5 (g) BXn có 7,1 (g) X, vậy trong 28,7 (g) AgX cũng chỉ có 7,1 (g) X
Þ mAg = 28,7 - 7,1 = 21,6 (g) Þ nAg = 0,2 (mol).
Trong AgX tỉ lệ kết hợp theo số mol nAg : nX = 1 : 1 Þ nX = 0,2 (mol).
![]()
Suy ra X là clo
BCln + nAgNO3 ® nAgCl¯ + B(NO3)n
(mol) ![]() 0,2
0,2

Þ MB + 35,5n = 67,5n ; MB = 32n
* Nếu n = 1 MB = 32 (loại)
* Nếu n = 2 MB = 64 Þ B là Cu.
5.14 Hướng dẫn:
Khi sục khí Cl2 vào dung dịch chứa hỗn hợp ở muối NaF, NaCl, NaBr chỉ có NaBr tác dụng.
Đặt số mol hỗn hợp ban đầu: NaF : a (mol) ; NaCl: b (mol); NaBr: c (mol).
Viết các phương trình phản ứng và lập hệ phương trình.

Giải hệ phương trình ta có:
![]() hay 8,7%
hay 8,7%
![]() hay 48,5%
hay 48,5%
![]() hay 42,8%
hay 42,8%
5.15 Hướng dẫn:
Đặt số mol NaCl: a (mol); NaBr: b (mol); NaI: c (mol)
a) Các phản ứng với brom dư:
2NaI + Br2 ® 2NaBr + I2
c mol c mol
Hỗn hợp A: 58,5a + 103b + 150c = 5,76
sau phản ứng với brom: 58,5a + 103 (b + c) = 5,29
Þ 47c = 0,47
* Các phản ứng với Cl2
2NaBr + Cl2 ® 2NaCl + Br2
2NaI + Cl2 ® 2NaCl + I2
(mol) 0,01 0,01
Nếu Cl2 chỉ phản ứng với NaI thì khối lượng hỗn hợp muối sau phản ứng với
Cl2 là
5,76 - 1,5 + 0,585 = 4,845g.
Theo đề bài hỗn hợp sau phản ứng chỉ có 3,955 (g). Vậy Cl2 đã phản ứng với cả NaBr.
mhỗn hợp = 3,955 (g), trong đó có 0,05 (mol) NaCl và còn lại là NaBr.
nNaBr còn lại = ![]() (mol)
(mol)
Tính số mol NaBr tham gia phản ứng.
1 mol NaBr thay thế bằng 1 mol NaCl khối lượng giảm 44,5 g.
x mol NaBr thay thế bằng x mol NaCl khối lượng giảm 4,845 - 3,955 = 0,89 (g)
Þ ![]()
Số mol NaBr có trong 5,76g = 0,02 + 0,01 = 0,03
![]()
% theo khối lượng
NaCl: 20,3%; NaBr: 53,66%; NaI: 26,04%
5.16.Hướng dẫn:
NaCl + AgNO3 ® AgCl + NaNO3
(mol) a a a
NaBr + AgNO3 ® AgBr + NaNO3
(mol) b b b
170a - 143,5a = 188b - 170b
26,5a = 18b
![]()
![]()
%NaCl = ![]()
%NaBr = 100 - 27,84 = 72,16%
5.17 Hướng dẫn: Đặt thể tích của amoniac là V
Bình cầu chứa hiđroclorua là 3V
![]() sau khi trộn = 4V
sau khi trộn = 4V
Phương trình phản ứng:
NH3 + HCl ® NH4Cl
phản ứng theo tỉ lệ 1:1 về số mol Û theo tỉ lệ 1:1 về thể tích
Þ Sau phản ứng lượng HCl còn dư ![]() mol
mol
![]()
![]()
5.18 Hướng dẫn: Các phản ứng khi nhiệt phân:

![]()
![]()
![]()
Tính:

a) Khối lượng kết tủa C = 0,18 . 100 = 18 (g)
b) Gọi x và y là số mol KClO3 và KCl trong A.
Theo định luật bảo toàn khối lượng
tổng số mol KCl trong B = x + y ![]()
(trong đó 32 và 111 là KLPT của O2 và của CaCl2).
Mặt khác :
![]()
Giải hệ phương trình, ta có: x = 0,4
![]()
5.19 Hướng dẫn: Lượng NaCl nguyên chất:
1000kg ´ 89,5% = 895kg
Lượng HCl thu được theo lí thuyết :
2NaCl + H2SO4 ® Na2SO4 + 2HCl
58,5 g 36,5g
895kg x = 558,42kg
Lượng HCl thu được theo thực tế:
1250 lit ´ 1,19kg/lit ´ 37% = 550,375 kg
Hiệu suất của quá trình điều chế:
H% = ![]()
5.20 Hướng dẫn:
2KClO3 ![]() 2KCl + 3O2 (a)
2KCl + 3O2 (a)
(mol) a a
4KClO3 ![]() 3KClO4 + KCl (b)
3KClO4 + KCl (b)
(mol) b ![]()

![]()
![]() và a = 0,4
và a = 0,4
%m phân hủy theo (a) : ![]()
%m phân hủy theo (b) : 33,33%
5.21

Số mol MnO2 đã được hòa tan trong axit clohiđric là :
![]()
![]()
Nhìn vào phương trình phản ứng, ta thấy 1mol MnO2 tác dụng với 4 mol HCl tạo nên 1mol MnCl2. Vậy 0,02mol MnO2 đã tác dụng với 0,08mol HCl tạo nên 0,02mol MnCl2.
Số mol HCl còn lại trong dung dịch là : 0,4 - 0,08 = 0,32 (mol)
Nồng độ của HCl còn lại trong dung dịch là :
CM HCl = ![]()
Nồng độ của MnCl2 trong dung dịch là :
![]() =
= ![]()
5.22 Hướng dẫn:
![]()
Theo (1)

Theo (2) : Nếu Fe phản ứng hết thì cần :
![]()
![]()
Þ Lượng Cl2 thu được sau phản ứng (1) không đủ hòa tan 28 (g) Fe.
5.23 Hướng dẫn:
Các phương trình hóa học
2Al + 6HCl ® 2AlCl3 + 3H2 (1)
(mol) x 1,5x
Mg + 2HCl ® MgCl2 + H2 (2)
(mol) y y
Đặt x, y lần lượt là số mol của Al và Mg trong hỗn hợp, theo bài ra ta có:
27x + 24y = 7,8 (I)
(1,5x + y)2 = 0,8 (II) giải ra ta được x = 0,2, y = 0,1
Vậy ![]() = 0,2 x 27 = 5,4 (g) và
= 0,2 x 27 = 5,4 (g) và ![]() = 0,1x24 = 2,4 (g).
= 0,1x24 = 2,4 (g).
5.24 Hướng dẫn:
a) Các phản ứng nhiệt phân
2KClO3 ![]() 2KCl + 3O2 (1)
2KCl + 3O2 (1)
2KmnO4 ![]() K2MnO4 + MnO2 + O2 (2)
K2MnO4 + MnO2 + O2 (2)
Gọi n là tổng số mol O2 thoát ra từ (1) và (2). Sau khi trộn n mol O2 với 3n mol không khí (trong đó có ![]() ta thấy tổng số mol O2 bằng (1 + 0,6) n = 1,6n. Vì số mol cacbon
ta thấy tổng số mol O2 bằng (1 + 0,6) n = 1,6n. Vì số mol cacbon ![]() và theo điều kiện bài toán, sau khi đốt cháy thu được hỗn hợp 3 khí, nên ta có 2 trường hợp:
và theo điều kiện bài toán, sau khi đốt cháy thu được hỗn hợp 3 khí, nên ta có 2 trường hợp:
Trường hợp 1: Nếu oxi dư, tức 1,6n > 0,044, thì cacbon chỉ cháy theo phản ứng
C + O2 ® CO2 (3)
![]()
Các khí gồm: oxi dư, nitơ, CO2
Þ (1,6 n - 0,044) + 2,4n + 0,044 = 0,192
![]()
Khối lượng mA = khối lượng chất rắn còn lại + khối lượng oxi thoát ra.
![]()
Trường hợp 2: Nếu oxi thiếu, tức 1,6n < 0,044, thì cacbon cháy theo 2 phản ứng:
C + O2 ® CO2 (3)
2C + O2 ® 2CO (4)
Các khí trong hỗn hợp có N2 (2,4n), CO2 (n') và CO (0,044 - n').
Như vậy tổng số mol khí = 2,4n + 0,044. Theo các phản ứng (3), (4) thì
![]() =
= ![]()
![]()
Giải ra có n = 0,0204
![]()
b) Tính % khối lượng các chất trong A.
Theo phản ứng (1): ![]() = 122,5 . 0,012 = 1,47 (g)
= 122,5 . 0,012 = 1,47 (g)
Đối với trường hợp 1:

Đối với trường hợp 2:

5.25 Hướng dẫn: Các phản ứng hóa học:

Số mol Fe cần tác dụng với clo là: ![]()
Theo ba phương trình phản ứng trên ta thấy 2 mol Fe phản ứng với 3 mol Cl2 ; 1 mol Cl2 được tạo nên từ 4 mol HCl và 1 mol HCl được tạo nên từ 1 mol NaCl. Vậy 0,4 mol Fe phản ứng với 0,6 mol Cl2 ; 0,6 mol Cl2 được tạo nên từ 2,4 mol HCl và 2,4 mol HCl được tạo nên từ 2,4 mol NaCl.
Khối lượng NaCl có trong muối ăn công nghiệp là :
58,5 . 2,4 = 140,4 (g)
Hàm lượng phần trăm của NaCl trong muối ăn công nghiệp là :
![]()
F. THÔNG TIN BỔ SUNG
CLO
Muối ăn, NaCl, là hợp chất có chứa clo đã được loài người biết đến từ thửa xa xưa. Thời trung cổ, các nhà giả kim thuật đã biết điều chế các axit clohidric bằng cách cho axit sunfuric tác dụng lên muối ăn
Chúng ta biểu diễn bằng phương trình hóa học tổng quát sau:
H2SO4 + 2NaCl → Na2SO4 + 2HCl
Vào thế kỉ 16, nhà hóa học Đức Glauber đã nhận xét là khi dùng nước cường toan để hòa tan kim loại hay khoáng vật thì thấy có khói màu lục thoát ra. Ngày nay chúng ta hiểu thực chất nước cường toan như sau
HNO3 + 3HCl → 2Cl + NOCl + 2H2O
2Cl → Cl2
Tất cả những điều nói trên mới chỉ là tia sáng để con người lần bước đi tìm clo. Năm 1774, nhà hóa học tài năng Thụy Điển Sile lần đầu tiên tìm ra được nguyên tố clo. Ông đã dùng axit clohidric tác dụng lên khoáng vật piroluzit (MnO2)
4HCl + MnO2 → MnCl2 + 2H2O + Cl2
Ông mô tả chất khí thoát ra có màu vàng lục, và có mùi như mùi nước cường toan đun nóng. Rất có thể trong số những độc giả ham muốn hiểu biết hóa học, có người sẽ hỏi Sile làm sao mà có được khoáng vật trên. Câu hỏi như vậy là rất cần thiết đối với những người nghiên cứu khoa học. Nhà bác học tên tuổi Pháp, Pasteur, người đã tìm ra vacxin chống bệnh chó dại, đã nói rằng biết ngạc nhiên đúng lúc trên bước đường nghiên cứu là bắt đầu của sự phát minh.
Giữa thế kỉ 18, Thụy Điển là một nước nổi tiếng của Châu Âu trong việc cung cấp kim loại đen hảo hạng. Luyện kim và nghề mỏ rất thịnh vượng ở Thụy Điển. Cho nên rất dễ hiểu rằng, các nhà hóa học luôn luôn đi tìm quặng mới.Lại có một em học sinh nào đó thắc mắc: Sile có biết rằng mình đã tìm ra nguyên tố hóa học mới không?
Một câu hỏi thật là thông minh, không dễ gì trả lời ngắn gọn được. Oxi là nguyên tố hóa học cùng ngày sinh với clo, tác giả tìm ra oxi cũng chỉ biết mô tả điều mắt thấy, chứ không biết rằng mình tìm ra nguyên tố mới. Số phận Clo cũng như vậy.
Tìm ra oxi trong lịch sử hóa học, là mở mang cho sự thắng lợi của thuyết oxi về sự cháy và sự sụp đổ của thyết nhiên tố (hay thuyết Phlogittôn)
Tìm ra clo, trong lịch sử hóa học mở màn cho một quan niệm đúng đắn và đầy đủ hơn về axit (Lavodiê nhầm rằng hễ axit là đều chứa oxi)
Độc giả có thể tìm hiểu kĩ vấn đề này trong lịch sử hóa học. Chúng tôi chỉ nói thêm rằng: Nhà hóa học Pháp Lavoadiê cho rằng tính chất của axit là do oxi sinh ra. Vấn đề nêu ra không gặp người tranh cãi, bởi vì phần lớn axit (H2SO4, HNO3, H3PO4 đều có chứa oxi, nhưng khi bắt đầu tìm ra clo và tương ứng với nó là axit clo hiđric, thì người ta vẫn quyết đoán là trong axit phải có oxi(hai nhà hóa học kiên trì nhất quyết ý kiến này là Lavoadiê và Beczeniut). Thế là bao nhiêu nhà bác học bỏ công tìm kiếm oxi trong axit này, nhưng tất thảy đều vô hiệu. Phải chờ cho đến khi tìm ra hai nguyên tố điển hình nữa trong nhóm Halogen là brom và iot (nửa đầu thế kỉ 19), ứng với chúng là axit HBr, HI thì thuyết oxi sinh axit mới chịu thua hoàn toàn (1870).
Vấn đề lí thú kéo theo sau việc tìm ra clo là: Trong phản ứng điều chế khí clo từ khoáng vật MnO2, khi cô muối còn lại, người ta thấy còn lại những tinh thể màu hồng. Màu sắc lạ lùng này, gây sự chú ý của các nhà khoa học. Sự tìm ra clo đã dẫn đến sự tìm ra nguyên tố mới Mangan. Dùng quặng MnO2 để điều chế clo là một phản ứng đắt tiền chỉ được dùng trong các phòng thí nghiệm hiện nay, không thể dùng cho công nghiệp được.
Clo có nhu cầu lớn trong việc tẩy trắng vải sợi, cho nên các nhà hóa học tìm cách điều chế clo công nghiệp cho rẻ hơn.
Người ta tìm cách thay Piroluzit bằng vôi tôi, còn oxi thì lấy ở không khí, tức là lầy của công!
Phương pháp điều chế đầu tiên là của Veldon, phương trình có dạng tổng quát
12HCl + 4Ca(OH)2 + O2 → 4CaCl2 + 2Cl2 + 10H2O
Phương pháp thứ hai là phương pháp Dicon, có phần ưu điểm hơn
4HCl + O2 → 2Cl2 + 2H2O, chất xúc tác trung gian là muối đồng clorua. Với sự phát triển của công nghiệp điện hóa, ngày nay người ta sản xuất NaOH từ muối ăn và thu được sản phẩm phụ là khí clo. Ở nước ta, nhà máy hóa chất Việt Trì thực hiện phản ứng này bằng phương pháp điện phân
2NaCl + 2H2O → 2NaCl + H2 + Cl2
Sản phẩm phụ ở hai điện cực là khí clo và khí hiđro, chúng ta vẫn nghe nói axit clohidric của nhà máy. Chính vì họ đã tận dụng sản phẩm phụ để thực hiện phản ứng tổng hợp sau đây:
H2 + Cl2 → 2HCl
Đầu chiến tranh thế giới lần thứ nhất, khí clo đã bị giới quân sự Đức sử dụng làm chất độc hóa học. Hàng nghìn binh lính Pháp đã chết vì hít phải khí clo.
Tên gọi clo là là lấy từ tiếng Hi Lạp "Cloros" có nghĩa là "vàng _ lục".
Năm 1811, nhà hóa học Đức I. Shweiger đề nghị gọi là "Halogen", theo tiếng Hi Lạp có nghĩa "tạo muối". Thật vậy, clo (cũng như những nguyên tố cùng nhóm) rất dễ dàng hóa hợp với kim loại để tạo thành muối.
Clo ở dạng lỏng được nhà vật lí kiêm hóa học Anh Faraday tìm ra năm 1823
Chương 6
A. TÓM TẮT LÍ THUYẾT
I. Tính chất của oxi và lưu huỳnh
Cấu hình electron
Nguyên tử oxi có cấu hình electron 1s22s22p4, có 2 electron độc thân.
 Nguyên tử S có cấu hình electron: 1s22s22p63s23p4, có hai electron độc thân. Nguyên tử S có phân lớp 3d trống, khi bị kích thích có thể 1 electron từ phân lớp 3p sang 3d khi đó có 4 electron độc thân:
Nguyên tử S có cấu hình electron: 1s22s22p63s23p4, có hai electron độc thân. Nguyên tử S có phân lớp 3d trống, khi bị kích thích có thể 1 electron từ phân lớp 3p sang 3d khi đó có 4 electron độc thân:
¯ ¯ ¯ ¯ ¯ ¯
1s2 2s2 2p6 3s2 3p3 3d1
Hoặc thêm 1 electron nữa từ phân lớp 3s sang 3d, lúc này S* có 6 electron độc thân.
¯ ¯ ¯ ¯ ¯
1s2 2s2 2p6 3s1 3p3 3d2
2.Tính chất vật lí
Oxi là một chất khí không màu, không mùi, hơi nặng hơn không khí. Oxi ít tan trong nước, oxi hóa lỏng khi bị nén ở áp suất cao và nhiệt độ thấp. Oxi lỏng là một chất lỏng màu xanh nhạt, sôi ở -183oC.
Oxi có dạng thù hình là ozon (O3). Tầng khí ozon là tấm áo giáp che chở Trái đất khỏi các tia cực tím, bảo vệ sự sống trên hành tinh xanh.
Lưu huỳnh là chất rắn màu vàng, nhiệt độ nóng chảy tương đối thấp (113oC). Lưu huỳnh không tan trong nước, nhưng tan được trong các dung môi hữu cơ. Khi bị đun nóng lưu huỳnh thành dẻo, màu hơi nâu, sau đó nếu tiếp tục đun nóng mạnh sẽ tạo ra hơi lưu huỳnh có màu nâu sẫm.
3. Tính chất hóa học
Oxi và lưu huỳnh là các phi kim có tính oxi hóa mạnh. Nguyên tố oxi có độ âm điện lớn thứ hai, chỉ sau flo. Oxi có thể oxi hóa hầu hết các kim loại (trừ vàng và bạch kim) và một số phi kim, trong các phản ứng đó số oxi hóa của oxi giảm từ 0 xuống -2.Lưu huỳnh tác dụng với nhiều kim loại và một số phi kim. Trong các phản ứng số oxi hóa của lưu huỳnh biến đổi từ 0 xuống -2 (hợp chất với kim loại và hiđro) và từ 0 lên +4 hay +6 (hợp chất với oxi, axit, muối).
II. Tính chất các hợp chất của oxi, lưu huỳnh
Nước (H2O) là hợp chất quan trọng nhất của oxi, có vai trò vô cùng quan trọng đối với toàn bộ sự sống trên Trái đất. Phân tử nước có liên kết cộng hóa trị phân cực, là dung môi tốt cho nhiều chất. Giữa các phân tử nước có các liên kết hiđro, với năng lượng liên kết nhỏ hơn nhiều so với liên kết cộng hóa trị nhưng có ảnh hưởng quan trọng đến các tính chất vật lí của nước như nhiệt độ nóng chảy, nhiệt độ sôi cao. Loài người đang đứng trước nguy cơ cạn kiệt nguồn nước sạch, do các hoạt động sản xuất thải các chất độc hại làm ô nhiễm nguồn nước sông ngòi, ao hồ và đại dương.
Hiđro peoxit (nước oxi già, H2O2) vừa có tính chất oxi hóa vừa có tính khử.
Chất này có nhiều ứng dụng trong công nghiệp, làm chất tẩy trắng, bảo vệ môi trường, khử trùng trong y tế...
3. Hợp chất quan trọng nhất của S là axit sunfuric H2SO4 trong đó lưu huỳnh có số oxi hóa +6. Axit sunfuric H2SO4 là một trong những hóa chất cơ bản, ứng dụng rộng rãi trong sản xuất phân bón hóa học, chất tẩy rửa, sơn, chất dẻo, luyện kim, phẩm nhuộm, dược phẩm, hóa dầu...
Tính chất axit
H2SO4 + 2NaOH ® Na2SO4 + 2H2O
H2SO4 + CuO ® CuSO4 + H2O
H2SO4 loãng + Fe ® FeSO4 + H2
H2SO4 + Na2CO3 ® Na2SO4 + H2O + CO2
Tính chất oxi hóa mạnh của H2SO4 đặc, nóng.
 2H2SO4 đặc + Cu ® CuSO4 + SO2 + 2H2O
2H2SO4 đặc + Cu ® CuSO4 + SO2 + 2H2O
4H2SO4 đặc + 3Mg ® 3MgSO4 + S¯ + 4H2O
H2SO4 đặc là một chất rất háo nước, có thể làm khô được nhiều chất khí ẩm.
Oleum là dung dịch H2SO4 hấp thụ SO3, có công thức H2SO4.nSO3 (n có thể nhận giá trị nguyên hoặc thập phân).
4. Lưu huỳnh còn có các hợp chất như H2S (có trong thành phần một số suối nước khoáng nóng như Mỹ Lâm - Tuyên Quang), SO2 và axit H2SO3, các muối sunfua, sunfit, sunfat.
Dung dịch H2S trong nước gọi là axit sunfuhiđric. Đây là một axit yếu, hai nấc.
B. BÀI TẬP CÓ LỜI GIẢI
6.1 Trong tự nhiên oxi có 3 đồng vị bền ![]() ;
; ![]() và
và ![]() . Nguyên tử khối của oxi trong bảng tuần hoàn là 15,999. Tại sao có sự mâu thuẫn này.
. Nguyên tử khối của oxi trong bảng tuần hoàn là 15,999. Tại sao có sự mâu thuẫn này.
6.2 Có 5 lọ đựng khí riêng biệt các khí sau: O2, Cl2, HCl, O3, SO2. Làm thế nào để nhận ra từng khí?.
6.3 Một hợp chất được tạo thành từ các ion M+ và X22-. Trong phân tử của M2X2 có tổng số hạt proton, nơtron và electron là 164. Trong đó số hạt mang điện nhiều hơn hạt không mang điện là 52. Số khối của M lớn hơn số khối của X là 23 đơn vị.
Tổng số hạt electron trong M+ nhiều hơn trong X22- là 7 hạt.
- Xác định các nguyên tố M, X và viết công thức của phân tử M2X.
- Viết cấu hình electron (dạng chữ và dạng obitan) của nguyên tố X
6.4 Cho 100 lit hỗn hợp A gồm H2, O2, N2. Đem đốt hỗn hợp rồi đưa về nhiệt độ và áp suất ban đầu, sau khi cho H2O ngưng tụ thu được hỗn hợp B có thể tích 64 lit. Trộn vào B 100 lit không khí (20% thể tích O2) rồi đốt và tiến hành tương tự trên thì thu được hỗn hợp C có thể tích 128 lít. Hãy xác định thể tích các chất trong hỗn hợp A, B, C. Biết các thể tích đo cùng điều kiện.
6.5 Có 4 lọ mất nhãn đựng 4 dung dịch : HCl, H2SO4, BaCl2, Na2CO3, hãy nhận biết lọ nào đựng dung dịch gì mà không được dùng bất cứ thuốc thử nào.
6.6 Một loại muối ăn có lẫn tạp chất CaCl2, MgCl2, Na2SO4, MgSO4, CaSO4. Hãy trình bày cách loại các tạp chất để thu được muối ăn tinh khiết.
6.7 Chỉ dùng quỳ tím làm thế nào để phân biệt được dung dịch các chất sau đây: Na2SO4, Na2CO3, NH4Cl.
6.8 Có 6 lọ không nhãn đựng riêng biệt từng dung dịch sau: K2CO3, (NH4)2SO4, MgSO4, Al2(SO4)3, FeSO4 và Fe2(SO4)3. Dùng dung dịch xút hãy nhận biết dung dịch trong mỗi lọ?
6.9 Dung dịch A chứa các ion : SO42-, SO32-, CO32-. Bằng những phản ứng hóa học nào có thể nhận biết từng loại anion có trong dung dịch.
6.10 Cho một lượng Cu2S tác dụng hoàn toàn với dung dịch HNO3 đun nóng. Phản ứng tạo thành dung dịch A1 và làm giải phóng ra khí A2 không màu, bị hóa nâu trong không khí. Chia A1 thành 2 phần. Thêm dung dịch BaCl2 vào phần 1, thấy tạo thành kết tủa trắng A3 không tan trong axit dư. Thêm lượng dư dung dịch NH3 vào phần 2, đồng thời khuấy đều hỗn hợp, thu được dung dịch A4 có màu xanh lam đậm.
a) Hãy chỉ ra A1, A2, A3, A4 là gì?
b) Viết các phương trình phản ứng trong các quá trình hóa học vừa nêu trên.
6.11 Cho biết tổng số electron trong anion AB32- là 42. Trong các hạt nhân A cũng như B số proton bằng số nơtron.
a) Tính số khối của A, B
b) Viết cấu hình và sự phân bố electron trong các obitan của các nguyên tử A, B.
6.12 Hai nguyên tố A, B có các oxit ở thể khí tương ứng là AOn, AOm, Bm và BOi. Hỗn hợp (I) gồm x phân tử gam AOn và y phân tử gam AOm có khối lượng phân tử trung bình là 37,6. Hỗn hợp (II) gồm y phân tử gam AOn và x phân tử gam AOm có khối lượng phân tử trung bình là 34,4. Biết tỉ khối hơi của Bm so với BOi là 0,8 và x < y.
a) Xác định các chỉ số n, m, i và tỉ số x/y.
b) Xác định các nguyên tố A, B và các oxit của chúng.
c) Cho biết tính tan của các chất trên trong nước và tính chất hóa học cơ bản của các dung dịch của chúng.
6.13 Đốt cháy chất X bằng O2 vừa đủ ta thu được hỗn hợp khí duy nhất là CO2 và SO2 có tỉ khối so với hiđro bằng 28,667 và tỉ khối hơi của X so với không khí nhỏ hơn 3. Xác định công thức phân tử của X.
6.14 Cho một lượng chất A tác dụng hết với một lượng dung dịch H2SO4 vừa đủ, tạo ra chất B, C và 7,458 lit khí D ở 300C, 1 atm. Ở cùng nhiệt độ, áp suất, tỉ khối hơi của D so với hiđro bằng 2,286 lần tỉ khối hơi của nitơ so với hiđro.
a) A, B, C là chất nào? Viết phương trình phản ứng cụ thể cho quá trình trên. Biết rằng trong các phản ứng đó các chất đều có hệ số như nhau trong các phương trình; A có thể là một trong các chất K2CO3, K2SO3, KHCO3, KHSO3.
b) Tính khối lượng các chất: A, B, C và H2SO4 nguyên chất.
6.15 Trong một bình kín dung tích không đổi chứa a mol SO2 , a mol O2 và một ít bột xúc tác V2O5; áp suất và nhiệt độ trong bình là P atm và t0C. Nung nóng bình một thời gian, sau đó đưa nhiệt độ bình về t0C, áp suất trong bình lúc này là P'. Lập biểu thức P theo P và h (hiệu suất phản ứng). Hỏi P' có giá trị trong khoảng nào, biết rằng ở t0C các chất đều ở thể khí.
6.16 Cho m gam hỗn hợp bột Fe và S với tỉ lệ số mol sắt bằng 2 lần số mol lưu huỳnh, rồi đem nung (không có oxi), thu được hỗn hợp A. Hòa tan A bằng dung dịch HCl dư thu được 0,4 gam chất rắn B, dung dịch C và khí D. Sục khí D từ từ qua dung dịch CuCl2 dư thấy tạo ra 4,8 gam kết tủa đen.
a) Tính hiệu suất phản ứng tạo thành hỗn hợp A (theo S). Tính m.
b) Cho dung dịch C tác dụng với H2SO4 đặc, nóng dư. Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn.
6.17 Cho a gam hỗn hợp gồm FeS2 và FeCO3 với số mol bằng nhau vào một bình kín chứa lượng dư oxi. Áp suất trong bình là p1 atm. Đun nóng bình để phản ứng xảy ra hoàn toàn rồi đưa bình về nhiệt độ ban đầu, áp suất khí trong bình lúc này là p2 atm, khối lượng chất rắn thu được là b gam. Biết rằng thể tích chất rắn trong bình trước và sau phản ứng là không đáng kể. Hãy xác định các tỉ số p1/p2 và a/b.
6.18 Hỗn hợp ban đầu SO2 và O2 có tỉ khối hơi đối với H2 bằng 24. Cần thêm bao nhiêu lit O2 vào 20 lit hỗn hợp ban đầu để hỗn hợp mới có tỉ khối hơi so với H2 bằng 22,4. Thực hiện phản ứng với hỗn hợp mới và xúc tác V2O5. Hỏi sau phản ứng hỗn hợp có khí gì và thể tích hỗn hợp là bao nhiêu?
(Biết rằng thể tích các khí đo trong điều kiện tiêu chuẩn, hiệu suất phản ứng 100%).
6.19 Từ 800 tấn quặng pirit sắt (FeS2) chứa 25% tạp chất không cháy, có thể sản xuất được bao nhiêu m3 dung dịch H2SO4 93% (D = 1,83 g/ml) ? Giả thiết tỉ lệ hao hụt là 5%.
6.20 Hòa tan 0,4 gam SO3 vào a gam dung dịch H2SO4 10% thu được dung dịch H2SO4 12,25%.
a) Tính a.
b) Thêm 10 ml dung dịch Ba(OH)2 0,5 M vào dung dịch thu được ở trên lọc kết tủa thêm tiếp 50 ml dung dịch NaOH 0,8 M vào nước lọc rồi cho bay hơi thu được 6,44 gam chất rắn X. Xác định công thức của X.
c) Lấy 48,3 gam X hòa tan trong V ml H2O thu được dung dịch 8%. Tính V. (![]() = 1g/ml).
= 1g/ml).
C. BÀI TẬP TỰ LUYỆN
6.21 X, Y là hai nguyên tố liên tiếp nhau trong một nhóm A. Cấu hình e ngoài cùng của X là 2p4.
a) Viết cấu hình e và xác định vị trí X, Y trong bảng tuần hoàn.
b) Viết công thức e và công thức cấu tạo của phân tử tạo nên từ X và Y
6.22 Dung dịch hiđropeoxit có nồng độ 30% và khối lượng riêng 1,51g/cm3. Dung dịch hiđropeoxit bị phân hủy theo phản ứng sau:
![]()
Tính thể tích khí oxi thu được (đktc) khi cho 100ml hiđropeoxit trên phân hủy.
Đáp số: 14,92 lít oxi
6.23 Hỗn hợp khí ozon và oxi có tỉ khối hơi so với hiđro bằng 20. Hãy xác định thành phần phần trăm theo thể tích của các khí trong hỗn hợp. Dẫn 2,24 lit hỗn hợp khí trên đi qua dung dịch KI dư. Tính khối lượng iot tạo thành.
Đáp số: 
6.24 Người ta có thể điều chế oxi từ các chất sau: KMnO4, KClO3, H2O2, H2O. Hãy viết các phương trình phản ứng minh họa và so sánh thể tích khí oxi thu được (trong cùng điều kiện) khi phân hủy cùng một khối lượng chất ban đầu.
6.25 Nêu hiện tượng và viết phương trình phản ứng nếu có khi cho H2SO4 đặc tác dụng với các chất sau: KMnO4, KClO3, H2O2, H2O..
6.26 Mỗi ống nghiệm chứa một trong các dung dịch sau: KI, BaCl2, Na2CO3, Na2SO4, NaOH, (NH4)2SO4, nước clo. Không dùng thêm chất khác, hãy trình bày cách nhận biết mỗi chất trên.
6.27 Cho hỗn hợp gồm FeS và CuS với tỉ lệ mol 1 : 1 tác dụng với dung dịch HNO3 thu được dung dịch A và khi B. A tạo thành kết tủa trắng với BaCl2; để trong không khí B chuyển thành màu nâu B1. Cho dung dịch A tác dụng với dung dịch amoniac tạo ra dung dịch A1 và kết tủa A2. Nung A2 ở nhiệt độ cao được chất rắn A3. Viết các phương trình phản ứng dạng phân tử.
6.28 Tính lượng FeS2 cần dùng để điều chế một lượng SO3 đủ để tan vào 100 gam H2 SO4 91% thành oleum chứa 12,5% SO3 . Giả thiết các phản ứng được thực hiện hoàn toàn.
Đáp số: mFeS2 = 45gam
6.29 Trộn 400ml HCl với 100ml H2SO4 được dung dịch A. Để trung hòa 10ml dung dịch A cần 40ml dung dịch NaOH 0,4M. Cô cạn dung dịch sau khi trung hòa được 1,036 gam muối khan.
Tính nồng độ mol/l của dung dịch HCl, H2SO4 và của các muối trong dung dịch sau trung hòa.
Đáp số: [HCl] = 0,875M; [H2SO4] = 2,25M;
[NaCl] = 0,14M; [Na2SO4] = 0,09M;
6.30 Hỗn hợp A gồm FeCO3 và FeS2. A tác dụng với dung dịch axit HNO3 63% (khối lượng riêng 1,44 g/ml) theo các phản ứng sau:
![]()
được hỗn hợp khí B và dung dịch C. Tỉ khối của B đối với oxi bằng 1,425. Để phản ứng vừa hết với các chất trong dung dịch C cần dùng 540 ml dung dịch Ba(OH)2 0,2M. Lọc lấy kết tủa, đem nung đến khối lượng không đổi, được 7,568 gam chất rắn (BaSO4 coi như không bị nhiệt phân). Các phản ứng xảy ra hoàn toàn.
a) X là muối gì ? Hoàn thành các phương trình phản ứng (1) và (2).
b) Tính khối lượng từng chất trong hỗn hợp A.
c) Xác định thể tích dung dịch HNO3 đã dùng (giả thiết HNO3 không bị bay hơi trong quá trình phản ứng).
![]() Đáp số:
Đáp số: 
6.31 Đun nóng hỗn hợp gồm 5,6 gam bột sắt và 3,2 gam bột lưu huỳnh sau phản ứng thu được hỗn hợp A. Cho A tác dụng với dung dịch HCl dư thu được 2,24 lit hỗn hợp khí B và m gam chất rắn C. Cho biết tỉ khối hơi của B so với hiđro là 13.
a) Xác định thành phần phần trăm theo thể tích của các khí trong B.
b) Tính hiệu suất của phản ứng sắt và lưu huỳnh; tính giá trị của m.
![]() Đáp số:
Đáp số: 
6.32 Từ 100 tấn quặng pirit sắt (FeS2) chứa 15% tạp chất không cháy, có thể sản xuất được bao nhiêu m3 dung dịch H2SO4 98% (d = 1,84) ? Giả thiết tỉ lệ hao hụt là 10%.
Đáp số: ![]()
6.33 Cho 9,52 gam hỗn hợp Na2SO4, Na2SO3 và NaHSO3 tác dụng với dung dịch H2SO4 loãng dư, thu được 1,008 lit khí A (đktc). Mặt khác 9,52 gam hỗn hợp trên phản ứng vừa đủ với 72 ml dung dịch NaOH 0,5M.
1- Tính khối lượng mỗi chất trong 9,52 gam hỗn hợp trên.
2- Khí A làm mất màu vừa đủ 200 ml dung dịch nước brom. Tính nồng độ mol/l của dung dịch nước Br2 đã dùng?
Đáp số: 
D. BÀI TẬP TRẮC NGHIỆM
6.34. Khi cho 20 lít khí oxi đi qua máy tạo ozon, có 9% thể tích oxi chuyển thành ozon. Hỏi thể tích khí bị giảm bao nhiêu lít? (các điều kiện khác không thay đổi)
A. 2 lít B. 0,9 lít C. 0,18 lít D. 0,6 lít
6.35. Trong phản ứng
Phát biểu nào sau đây đúng khi nói về phân tử H2O2?
A. Là chất oxi hoá
B. Là chất khử
C. Vừa là chất oxi hoá, vừa là chất khử.
D. Không là chất oxi hoá, không là chất khử
6.36. Ở phản ứng nào sau đây H2O2 vừa đóng vai trò chất oxi hoá, vừa đóng vai trò chất khử?
A. H2O2 + 2KI ® I2 + 2KOH
B. Ag2O + H2O2 ® 2Ag + H2O + O2
C. 2H2O2 ® 2H2O + O2
D. H2O2 + KNO2 ® H2O + KNO3
6.37. Cho nổ hỗn hợp gồm 2ml hiđro và 6ml oxi trong bình kín. Hỏi sau khi nổ, đưa bình về nhiệt độ phòng, nếu giữ nguyên áp suất ban đầu, trong bình còn khí nào với thể tích bằng bao nhiêu?
A. 4ml O2 B. 2ml O2 C. 1ml H2 D. 5ml O2
6.38. Nếu 1gam oxi có thể tích 1 lít ở áp suất 1atm thì nhiệt độ bằng bao nhiêu?
A. 35oC B. 48oC
C. 117oC D. 120oC
6.39. Cặp chất nào sau đây có phần trăm khối lượng đồng như nhau?
A. Cu2S và Cu2O B. CuS và CuO
C. Cu2S và CuO D. Không có cặp nào.
6.40. Dùng 300 tấn quặng pirit (FeS2) có lẫn 20% tạp chất để sản xuất axit H2SO4 có nồng độ 98%. Biết rằng hiệu suất phản ứng là 90%. Khối lượng axit H2SO4 98% thu được là
A. 320 tấn B. 335 tấn C. 350 tấn D. 360 tấn
6.41. Đốt cháy hoàn toàn 8,96 lít H2S (đktc) trong oxi dư, rồi dẫn tất cả sản phẩm vào 50 ml dung dịch NaOH 25% (D= 1,28). Nồng độ % muối trong dung dịch là
A. 47, 92% B. 42, 96% C. 42,69% D. 24,97%
6.42. Cho sơ đồ của phản ứng
H2S + KMnO4 + H2SO4 ® H2O + S + MnSO4 + K2SO4
Hệ số của các chất tham gia phản ứng là dãy số nào trong các dãy sau?
A. 3, 2, 5 B. 5, 2, 3 C. 2, 2, 5 D. 5, 2, 4
6.43. Cho các chất và ion sau Cl-, Na2S, NO2, Fe2+, SO2, Fe3+,  ,
,  ,
,  , Na, Cu. Dãy chất và ion nào sau đây vừa có tính khử, vừa có tính oxi hoá?
, Na, Cu. Dãy chất và ion nào sau đây vừa có tính khử, vừa có tính oxi hoá?
A. Cl-, Na2S, NO2, Fe2+ B. NO2, Fe2+, SO2, Fe3+, 
C. Na2S, Na2S,  , NO2 D. Cl-, Na2S, Na, Cu
, NO2 D. Cl-, Na2S, Na, Cu
6.44. Dãy chất và ion nào sau đây chỉ thể hiện tính khử trong các phản ứng hóa học?
A. H2S và Cl- B. NH3 và I-
C. Na và S2- D. Fe2+ và Cl-
6.45. Tính chất đặc biệt của dd H2SO4 đặc, nóng là tác dụng được với các chất trong dãy nào sau đây mà dd H2SO4 loãng không tác dụng?
A. BaCl2, NaOH, Zn B. NH3, MgO, Ba(OH)2
C. Fe, Al, Ni D. Cu, S, C12H22O11 (đường saccarozơ)
6.46. Cho 21 gam hỗn hợp Zn và CuO vào 600 ml dung dịch H2SO4 0,5mol/L, phản ứng vừa đủ. % khối lượng của Zn có trong hỗn hợp ban đầu là
A. 57% B. 62% C. 69% D. 73%
6.47. Hai bình cầu có thể tích bằng nhau. Nạp oxi vào bình thứ nhất. Nạp oxi đã được ozon hóa vào bình thứ hai. Nhiệt độ và áp suất ở hai bình như nhau. Đặt hai bình trên hai đĩa cân thấy khối lượng của hai bình khác nhau 0,21 gam. Số gam ozon có trong bình oxi đã được ozon hóa là
A. 0,63 B. 0,65 C. 0,67 D. 0,69
6.48 Để trừ nấm thực vật, người ta dùng dung dịch CuSO4 0,8%. Lượng dung dịch CuSO4 0,8% pha chế được từ 60 gam CuSO4.5H2O là:
A. 4800 gam B. 4700 gam C. 4600 gam D. 4500 gam
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP
7.34. D | 7.35. C | 7.36. C | 7.37. D | 7.38. C |
7.39. C | 7.40. D | 7.41. B | 7.42. B | 7.43. B |
7.44. C | 7.45. D | 7.46. D | 7.47. A | 7.48. A |
6.1 Hướng dẫn:
Trong tự nhiên oxi có 3 đồng vị bền ![]() ,
, ![]() và
và ![]() . Nguyên tử khối của oxi trong bảng hệ thống tuần hoàn là 15,999. Điều mâu thuẫn này xảy ra do sự hụt khối. Khi hình thành hạt nhân nguyên tử, một phần khối lượng của các hạt proton và nơtron đã chuyển thành năng lượng. Theo công thức của Anhxtanh:
. Nguyên tử khối của oxi trong bảng hệ thống tuần hoàn là 15,999. Điều mâu thuẫn này xảy ra do sự hụt khối. Khi hình thành hạt nhân nguyên tử, một phần khối lượng của các hạt proton và nơtron đã chuyển thành năng lượng. Theo công thức của Anhxtanh:
E = mc2, trong đó E là năng lượng, m là khối lượng và c là tốc độ của ánh sáng.
6.2 Hướng dẫn:
Khí Cl2 có màu vàng lục nhạt.
Dùng giấy tẩm hồ tinh bột và dung dịch KI nhận biết được O3:
O3 + 2KI + H2O ® O2 + I2 + 2KOH
I2 làm hồ tinh bột chuyển màu xanh.
Dùng quỳ tím ẩm nhận biết được HCl và SO2. Còn lại là khí O2.
- Phân biệt lọ khí HCl và SO2 bằng dung dịch nước brom. SO2 làm mất màu dung dịch brom.
SO2 + Br2 + 2H2O ® 2HBr + H2SO4
6.3 Hướng dẫn:
Gọi p, z, n là số proton, số electron và số nơtron trong một nguyên tử M.
p', z', n' là số proton, số electron và số nơtron trong một nguyên tử X.
Theo điều kiện bài toán ta có phương trình:
2(2z + n) + 2(2z' + n') = 164 (1)
(4z + 4z') - 2(n + n') = 52 (2)
(z + n) - (z' + n') = 23 (3)
(2z + n - 1) - 2(2z' + n') + 2 = 7 (4)
Giải hệ (1), (2), (3), (4) ta được z = 19 Þ M là kali: z' = 8 Þ X là oxi.
Công thức phân tử của hợp chất là K2O2
Cấu hình electron của nguyên tố X
O | ¯ | ¯ | ¯ | | | ||
1s2 | 2s2 | 2p4 |
6.4 Hướng dẫn:
Phản ứng : 2H2 + O2 ® 2H2O lỏng (1)
Sau lần phản ứng (I) hỗn hợp có thể tích giảm : 100 - 64 = 36 (lit)
Suy ra ![]() (đã phản ứng) + 2
(đã phản ứng) + 2![]() (đã phản ứng) = 36 (lit)
(đã phản ứng) = 36 (lit)
Trong đó ![]() (đã phản ứng) = 2
(đã phản ứng) = 2![]() = 24 (lit)
= 24 (lit)
Sau lần phản ứng (II) hỗn hợp có thể tích tiếp tục giảm:
100 + 64 - 128 = 36 (lit)
Chứng tỏ trong B còn H2 dư, suy ra O2 trong hỗn hợp A có 12 (lit) và đã phản ứng hết.
Ở lần phản ứng (II):
![]() (cũng phản ứng) = 24(lit)
(cũng phản ứng) = 24(lit)
![]() phản ứng = 12(lit)
phản ứng = 12(lit)
Mà ![]() trong 100 (lit) không khí =
trong 100 (lit) không khí = ![]() (lit) > 12 (lit) O2 phản ứng, chứng tỏ sau phản ứng (II) H2 đã hết, vì O2 dư.
(lit) > 12 (lit) O2 phản ứng, chứng tỏ sau phản ứng (II) H2 đã hết, vì O2 dư.
![]() dư = 8(lit)
dư = 8(lit)
vậy sau 2 lần phản ứng ![]() : 24 + 24 = 48 (lit)
: 24 + 24 = 48 (lit)
Kết luận : hh A có : 48 (lit) H2 ; 12 (lit) O2; 40 (lit) N2
hh B có : 24 (lit) H2 ; 40 (lit) N2
hh C có : 8 (lit) O2 dư; 120 (lit) N2
6.5 Hướng dẫn:
Lần lượt cho mẫu thử tác dụng với ba mẫu thử còn lại ta có kết quả :
HCl | H2SO4 | BaCl2 | Na2CO3 | ||
1 | HCl | CO2 | |||
2 | H2SO4 | BaSO4¯ | CO2 | ||
3 | BaCl2 | BaSO4¯ | BaCO3¯ | ||
4 | Na2CO3 | CO2 | CO2 | BaCO3¯ |
Dựa vào bảng trên ta thấy khi cho một mẫu thử nhỏ vào 3 mẫu thử kia sẽ xảy ra một trong bốn trường hợp. Trong các trường hợp trên, duy nhất chỉ có Na2CO3 hai lần thử có khí và một lần có kết tủa. BaCl2 có hai lần thử có kết tủa. H2SO4 vào 3 mẫu thử còn lại, một lần có kết tủa và một lần có khí bay ra. HCl vào 3 mẫu thử còn lại, chỉ có một lần có khí bay ra.
H2SO4 + HCl ® dung dịch trong suốt.
H2SO4 + BaCl2 ® BaSO4¯ + 2HCl
H2SO4 + Na2CO3 ® Na2SO4 + CO2 + H2O
6.6 Hướng dẫn:
- Hòa tan muối ăn vào nước cất.
- Thêm BaCl2 dư để loại ion SO42- ở dạng BaSO4 kết tủa trắng.
Phương trình phản ứng:
BaCl2 + Na2SO4 ® BaSO4¯ + 2NaCl
BaCl2 + MgSO4 ® BaSO4¯ + MgCl2
BaCl2 + CaSO4 ® BaSO4¯ + CaCl2
- Lọc bỏ kết tủa BaSO4.
- Thêm Na2CO3 dư để loại ion Mg2+, Ca2+
MgCl2 + Na2CO3 ® 2NaCl + MgCO3¯
CaCl2 + Na2CO3 ® 2NaCl + CaCO3¯
- Lọc bỏ kết tủa MgCO3, CaCO3.
- Thêm dung dịch HCl để loại bỏ Na2CO3 dư
Na2CO3 + 2HCl ® 2NaCl + CO2 + H2O
- Cô cạn dung dịch ta thu được muối ăn tinh khiết.
6.7 Hướng dẫn:
Cho một mẫu quỳ tím vào các mẫu thử, mẫu thử nào làm quỳ tím hóa xanh là dung dịch Na2CO3, quỳ tím hóa đỏ là dung dịch NH4Cl, quỳ tím không đổi màu là Na2SO4 vì:
Na2CO3 là muối của bazơ mạnh (NaOH) axit yếu nên thủy phân tạo ra dung dịch có tính bazơ.
Na2CO3 + H2O ![]() NaHCO3 + NaOH
NaHCO3 + NaOH
NH4Cl là muối của axit mạnh (HCl) và bazơ yếu nên thủy phân tạo ra dung dịch có tính axit.
NH4Cl + H2O ![]() NH3 + H2O + HCl
NH3 + H2O + HCl
Na2SO4 là muối của axit mạnh (H2SO4) và bazơ mạnh (NaOH) nên không bị thủy phân.
6.8 Hướng dẫn:
Lấy từ mỗi dung dịch một ít để làm thí nghiệm.
- Nhỏ dung dịch NaOH vào từng dung dịch:
+ Dung dịch nào không có hiện tượng gì là K2CO3.
+ Dung dịch nào thấy phản ứng xảy ra có khí mùi khai bay ra. Đó là (NH4)2SO4
(NH4)2SO4 + 2NaOH ® 2NH3 + Na2SO4 + 2H2O
+ Dung dịch nào thấy có kết tủa xuất hiện, để lâu ngoài không khí kết tủa không đổi màu. Đó là MgSO4:
MgSO4 + 2NaOH ® Mg(OH)2¯ + Na2SO4
+ Dung dịch nào thấy có kết tủa keo trắng xuất hiện, nhỏ tiếp NaOH đến dư, kết tủa tan . Đó là Al2(SO4)3.
Al2(SO4)3 + 6NaOH ® 2Al(OH)3¯ + 3Na2SO4
Al(OH)3 + NaOH dư ® NaAlO2 + 2H2O
+ Dung dịch nào thấy xuất hiện kết tủa trắng và kết tủa dần dần chuyển sang màu nâu đỏ khi để ngoài không khí. Đó là FeSO4.
FeSO4 + 2NaOH ® Fe(OH)2¯ + Na2SO4
4Fe(OH)2 + O2 + 2H2O ® 4Fe(OH)3¯(màu nâu đỏ)
+ Dung dịch nào thấy xuất hiện kết tủa màu nâu. Đó là Fe2(SO4)3.
Fe2(SO4)3 + 6NaOH ® 2Fe(OH)3¯(màu nâu đỏ) + 3Na2SO4
6.9 Nhận biết từng loại anion trong dung dịch A: Ta có thể tiến hành theo nhiều cách khác nhau. Sau đây giới thiệu 2 cách.
Cách 1 :
- Cho dung dịch A tác dụng với dung dịch axit HCl:
Dung dịch A + HCl ® hỗn hợp khí + dung dịch B
SO32- + 2H+ ® SO2 + H2O
CO32- + 2H+ ® CO2 + H2O
- Cho hỗn hợp khí lần lượt qua dung dịch KMnO4 và sau đó là dung dịch Ca(OH)2. Ta thấy:
+ Dung dịch KMnO4 bị nhạt màu do phản ứng:
5SO2 + 2KMnO4 +2H2O ® K2SO4 + 2MnSO4 + 2H2SO4
Chứng tỏ trong hỗn hợp khí có SO2, suy ra dung dịch A có SO32-.
+ Dung dịch Ca(OH)2 bị vẩn đục hoặc vẩn đục rồi trở nên trong suốt do các phản ứng:
CO2 + Ca(OH)2 ® CaCO3¯ + H2O
CO2 + CaCO3 + H2O ® Ca(HCO3)2
Chứng tỏ trong hỗn hợp có khí CO2, suy ra trong dung dịch A có CO32-.
- Dung dịch B tác dụng với BaCl2 thấy có kết tủa:
SO42- + BaCl2 ® BaSO4¯ + 2Cl-
Chứng tỏ trong dung dịch A có ion SO42-.
Cách 2:
- Dung dịch A + BaCl2 ® hỗn hợp kết tủa C:
SO42 + Ba2+ ® BaSO4¯
SO32- + Ba2+ ® BaSO3¯
CO32- + Ba2+ ® BaCO3¯
- Cho kết tủa C tác dụng với axit HCl:
+ Chất không tan là BaSO4, suy ra dung dịch A có ion SO42-.
+ Chất tan là BaSO3 và BaCO3:
BaSO3 + 2HCl ® BaCl2 + SO2 + H2O
BaCO3 + 2HCl ® BaCl2 + CO2 + H2O
Nhận biết khí SO2, CO2 để suy ra có ion SO32- và CO32- như cách 1.
6. 10 Hướng dẫn :
a) Chỉ ra các chất
A1 là dung dịch gồm Cu(NO3)2, H2SO4 và HNO3 dư.
A2 là khí NO
A3 là kết tủa BaSO4
A4 là dung dịch chứa ion phức [Cu(NH3)4]2+
b) Các phương trình phản ứng:
3Cu2S + 22HNO3 ® 6Cu(NO3)2 + 3H2SO4 + 10NO + 8H2O
2NO + O2 ® 2NO2
H2SO4 + BaCl2 ® BaSO4¯ + 2HCl
NH3 + H+ ® NH4+
Cu2+ + 4NH3 ® Cu(NH3)4)2+
6.11 Hướng dẫn :
a) Gọi x, y: số proton trong các hạt nhân của A, B ta có:
x + 3y = 42 - 2 = 40
Do đó y < ![]() B phải thuộc chu kỳ 2. Vì là phi kim (tạo anion) nên B chỉ có thể là F, O hoặc N.
B phải thuộc chu kỳ 2. Vì là phi kim (tạo anion) nên B chỉ có thể là F, O hoặc N.
+ Nếu là F: (y = 9) thì x = 40 - (3 ´ 9) = 13 Þ Al (loại)
+ Nếu là O:(y = 8) thì x = 40 - (3 ´ 8) = 16 đó là S (đúng)
+ Nếu là N: (y = 7) thì x = 40 - (3 ´ 7) = 19 ứng với K (loại)
Vậy: A là S có số khối: 16 + 16 = 32
B là O có số khối : 8 + 8 = 16
b) Cấu hình electron và sự phân bố electron của:
S | ¯ | ¯ | ¯ | ¯ | ¯ | ¯ | ¯ | | | ||||
1s2 | 2s2 | 2p6 | 3s2 | 3p4 |
O | ¯ | ¯ | ¯ | | | ||
1s2 | 2s2 | 2p4 |
6.12 Hướng dẫn :
a) Xác định các chỉ số n, m, i và tỷ số x/y.
Đặt khối lượng mol nguyên tử của 2 nguyên tố A, B lần lượt là A, B.
* Hỗn hợp : x mol AOn và y mol AOm có khối lượng mol phân tử trung bình ![]() .
.
![]()
Þ ![]() (1)
(1)
* Hỗn hợp II: x mol AOm và y mol AOn có khối lượng mol phân tử trung bình ![]()
![]()
Þ ![]() (2)
(2)
Þ (1) - (2)
![]()
Þ ![]() (3)
(3)
Vì x + y > 0 và x < y (theo đề bài)
Nên m - n > 0 Þ m > n (4)
* Tỉ khối hơi của BOm so với BOi :
![]() (5)
(5)
Þ ![]() (6)
(6)
So sánh (4); (6) ta có : n < m < i
Các oxit ở thể khí thường có dạng tổng quát
XOK trong đó 1 £ K £ 3
Þ 1 £ n < m < i £ 3 Þ n = 1; m = 2 và i = 3
(2) Tỷ số x/y
Thay n = 1; m = 2 vào (2) ta có :
![]()
b) Xác định A, B và các oxit của chúng.
* Thay n = 1; m = 2 và ![]() vào (1) thì được:
vào (1) thì được:
A = 12. Vậy A là cacbon
* Thay m = 2 và i = 3 vào (5) thì được :
B = 32. Vậy B là lưu huỳnh.
Vậy các oxit tương ứng của A là: CO và CO2.
Các oxit tương ứng của B là : SO2 và SO3.
c) Tính tan của các oxit và tính chất hóa học cơ bản của các dung dịch.
CO : rất ít tan trong nước.
Có tính khử :
Fe2O3 + 3CO ![]() 2Fe + 3CO2
2Fe + 3CO2
CO2 : ít tan trong nước:
Dung dịch có tính axit yếu, không bền:
CO2 + H2O ![]() H2CO3
H2CO3
SO2 : tan nhiều trong nước.
Dung dịch có tính axit, không bền
SO2 + H2O ![]() H2SO3
H2SO3
Dung dịch có tính khử hoặc có tính oxi hóa
H2SO3 + Br2 (dd) + H2O ® H2SO4 + 2HBr (tính khử)
H2SO3 + 2H2S ® 3S + 3H2O (tính oxi hóa )
SO3: tan nhiều trong nước tạo thành axit mạnh
SO3 + H2O ® H2SO4
Dung dịch H2SO4 loãng có tính axit mạnh
H2SO4 + Zn ® ZnSO4 + H2
Dung dịch H2SO4 đậm đặc nóng có tính oxi hóa mạnh.
6.13 Hướng dẫn:
![]() hỗn hợp khí CO2 và SO2 : 28,667 ´ 2 = 57,334
hỗn hợp khí CO2 và SO2 : 28,667 ´ 2 = 57,334
Trong hỗn hợp khí : Gọi số mol CO2 là x, số mol SO2 là y
![]()
 .
.
Suy ra trong hợp chất X số mol nguyên tử C là 1 và số mol nguyên tử S là 2.
Công thức đơn giản (CS2)nOz.
n chỉ có thể = 1 vì nếu n = 2; z = 0 thì MX = 152
So với không khí ![]() . Trái với giả thiết
. Trái với giả thiết
n = 1 và z = 1 thì MX = 92 so với không khí ![]() cũng trái với giả thiết.
cũng trái với giả thiết.
Vậy công thức CS2 (cacbon đisunfua)là công thức của X.
CS2 + 3O2 ® CO2 + 2SO2
6.14 Hướng dẫn:
a) Theo giả thiết : 
A là một trong các chất K2CO3, K2SO3, KHCO3, KHSO3. Vậy khi tác dụng H2SO4 khí được giải phóng sẽ là CO2 hoặc SO2 với M = 64 thì D là SO2 vậy A là một trong hai chất K2SO3 hoặc KHSO3.
b) Tính khối lượng các chất A, B, C và H2SO4 nguyên chất.
* A là K2SO3
![]()
Số mol khí D : ![]()
K2SO3 + H2SO4 ® K2SO4 + H2O + SO2
0,3 mol 0,3 mol 0,3 mol 0,3 mol 0,3 mol
![]() gam
gam
![]() gam
gam
![]() gam
gam
![]() gam
gam
* A là KHSO3
KHSO3 + H2SO4 ® KHSO4 + H2O + SO2
0,3 mol 0,3 mol 0,3 mol 0,3 mol 0,3 mol
![]() (g)
(g)
![]() (g)
(g)
![]() (g)
(g)
![]() (g)
(g)
6.15 Hướng dẫn:
Biểu thức tính P' theo P và h (hiệu suất phản ứng)
2SO2 + O2 ![]() 2SO3
2SO3
Ban đầu : a mol a mol 0
Phản ứng với: ah mol ah/2 mol ah mol
Hiệu suất h%
Cân bằng (a - ah) mol ![]() mol ah mol
mol ah mol
- Tổng số mol ban đầu nt = a + a = 2a (mol)
- Tổng số mol sau phản ứng: ns = a - ah + a - ![]()
![]()
Ta có :
![]()
![]()
* Nếu h = 0 (không phản ứng): P' = P
* Nếu h = 1 (hiệu suất 100%):
![]()
Vậy P' phải có giá trị trong khoảng:
![]()
6.16 Hướng dẫn :
a) Gọi x là số mol S có trong m gam hỗn hợp. Suy ra số mol Fe sẽ là 2x.
Gọi x1 là số mol S tham gia phản ứng khi nung:
Ta có :
Fe + S ![]() FeS (1)
FeS (1)
(mol) x1 x1 x1
Sau khi nung, trong hỗn hợp A có :
(x - x1) mol S
(2x - x1) mol Fe
và x1 mol FeS
- Hòa tan A trong axit HCl dư:
Fe + 2HCl ® FeCl2 + H2 (2)
FeS + 2HCl ® FeCl2 + H2S (3)
Còn lại 0,4 gam chất rắn B là lưu huỳnh dư
nS = x - x1 = ![]() (mol) (I)
(mol) (I)
Dung dịch C gồm HCl dư và FeCl2 với số mol là 2x. Khí D gồm H2 và H2S
Sục khí D từ từ vào dung dịch CuCl2 dư, chỉ có H2S phản ứng:
CuCl2 + H2S ® CuS¯ + 2HCl (4)
Kết tủa đen tạo thành là CuS.
Theo (1), (2), (4):
nCuS = x1 = ![]() mol (II)
mol (II)
Kết hợp (I) và (II) ta có : x - x1 = 0,0125
x = 0,0125 + 0,05 = 0,0625
- Hiệu suất phản ứng tạo thành hỗn hợp A:
Theo S : h% = ![]()
b) Dung dịch C gồm HCl dư và FeCl2 với số mol là 0,125 . Cho dung dịch C tác dụng với H2SO4 đặc, nóng dư chỉ có FeCl2 phản ứng.
2FeCl2 + 4H2SO4 ® Fe2(SO4)3 + SO2 + 4HCl + 2H2O
2mol 1mol
0,125 ![]()
Þ ![]()
6.17 Trong a gam hỗn hợp gồm x mol FeCO3 và x mol FeS2
Các phương trình phản ứng đốt cháy:
4FeCO3 + O2 ![]() 2Fe2O3 + 4CO2 (1)
2Fe2O3 + 4CO2 (1)
x ![]()
![]() x
x
4FeS2 + 11O2 ![]() 2Fe2O3 + 8SO2 (2)
2Fe2O3 + 8SO2 (2)
x ![]()
![]() 2x
2x
Như vậy sau phản ứng (1), (2) đã dùng hết ![]() mol O2, nhưng lại tạo ra 3x mol khí CO2 và SO2. Do đó, số mol khí trong bình trước và sau phản ứng không thay đổi. Như vậy, tại cùng một nhiệt độ thì p1 = p2 hay
mol O2, nhưng lại tạo ra 3x mol khí CO2 và SO2. Do đó, số mol khí trong bình trước và sau phản ứng không thay đổi. Như vậy, tại cùng một nhiệt độ thì p1 = p2 hay ![]() .
.
Theo (1), (2) : a = 116x + 120x = 236x (g)
b = 0,5x ´ 160 + 0,5x . 160 = 160x (g)
![]()
6.18 Hướng dẫn :
Trong hỗn hợp SO2, O2 có ![]() = 24 ´ 2 = 48
= 24 ´ 2 = 48
gọi ![]() là x và
là x và ![]() là y
là y
![]()
![]() chiếm 50% hỗn hợp.
chiếm 50% hỗn hợp.
![]() chiếm 50% hỗn hợp
chiếm 50% hỗn hợp
Trong 20 lít hỗn hợp ![]() lít hay
lít hay
![]() mol.
mol.
Gọi thể tích O2 thêm vào là a
hỗn hợp sau khi thêm O2 có ![]() Þ
Þ ![]() = 22,4 ´ 2 = 44,8
= 22,4 ´ 2 = 44,8
Þ 
Þ a = 5 lit
Phương trình phản ứng:
![]()
(mol) ![]()
![]()
![]()
theo trên ta có oxi dư
sau phản ứng hỗn hợp có khí SO3 , O2 .
Þ số mol khí bị giảm ![]() mol Þ thể tích bị giảm 5 lit.
mol Þ thể tích bị giảm 5 lit.
Thể tích hỗn hợp sau phản ứng 20 + 5 - 5 = 20 (lit)
6.19 Hướng dẫn:Phản ứng đốt cháy pirit sắt:
4FeS2 + 11O2 ![]() 2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
4 mol 8 mol
Các phản ứng chuyển SO2 thành H2SO4

Lượng FeS2 có trong 800 tấn quặng: 800 - (800. 0,25) = 600 tấn = 600000000g
Số mol FeS2 = ![]()
Số mol FeS2 thực tế chuyển thành SO2:
5000000 - (5000000 . 0,05) = 4750000 mol
theo các phương trình phản ứng ta có số mol SO2 bằng số mol H2SO4 và bằng 2 lần số mol FeS2 đã phản ứng: 4750000 . 2 = 9500000 mol
Lượng H2SO4 được tạo thành : 98 . 9500000 = 931000000g = 931000 kg
![]()
6.20 Hướng dẫn :
a. Khi hòa tan SO3 vào dung dịch xảy ra phản ứng:
SO3 + H2O ® H2SO4
Khối lượng của H2SO4:
![]()
Khối lượng dung dịch: mdd = 0,4 + a. Ta có:
![]() Þ a = 19,6 gam
Þ a = 19,6 gam
b. Số mol H2SO4 là
![]()
Số mol Ba(OH)2 là x = 0,01.0,5 = 0,005 mol; Số mol NaOH là z = 0,05.0,8 = 0,04 mol.
Khi thêm các dung dịch trên ta có phản ứng:
Ba(OH)2 + H2SO4 ® BaSO4¯ + 2H2O (1)
2NaOH + H2SO4 ® Na2SO4 + 2H2O (2)
Theo phương trình phản ứng (1) và (2) x + z/2 = 0,025 = y do đó H2SO4 phản ứng hoàn toàn, lọc bỏ kết tủa BaSO4 thì trong dung dịch chỉ còn Na2SO4 với số mol là: 0,02 mol. Khi cho bay hơi dung dịch thu được Na2SO4.nH2O (X). Vậy MX = 6,44/0,02 = 322 (g).
MX = (2.23 + 96 + 18n) = 322 ị n = 10
Vậy X là Na2SO4 .10H2O
c. Khi hòa tan 48,3 gam X (Na2SO4 .10H2O) nX = 48,3/322 = 0,15 mol
ị mct = 0,15.142 = 21,3 gam.
Ta có:
![]()
Vậy khối lượng của nước cần lấy là: m = 266,25 - 48,3 = 217,95 (g)
V = m/D = 217,95 ml.
F. THÔNG TIN BỔ SUNG
Nguyên tố lưu huỳnh
Là nguyên tố phi kim thứ hai được biết đến từ thời rất xa xưa. Trong thiên nhiên, nhiều nơi đã có mỏ lưu huỳnh. Đó cũng là lí do để con người sớm biết lưu huỳnh
Vào thời Hôme (Khoảng thế kỉ 12-9, TCN), những người cổ Hi Lạp đã biết đốt lưu huỳnh để tẩy uế nhà cửa, dùng khí thoát ra (SO2) để tẩy trắng sợi vải. Người xưa tin rằng, cái mùi và màu xanh của ngọn lửa lưu huỳnh có thể xua đuổi được ma quỷ.....
Lưu huỳnh tự sinh được thấy ở những nơi gần các núi lửa họat động. Các khí thoát ra từ miệng núi lửa thường là hợp chất của lưu huỳnh, nên có giả thuyết cho rằng lưu huỳnh tự sinh là kết quả của phản ứng của các chất khí đó
2H2S + SO2 → 3S + 2H2O
Ngoài ra sự hoạt động lâu bền của các vi sinh vật trong đất cũng là nguyên nhân tạo thành lưu huỳnh tự sinh. Những mỏ lưu huỳnh này thường ở xa núi lửa và không có chứa tạp chất asen. Lí do đáng tin cậy ở chỗ, trong quá trình hoạt động để chuyển các hợp chất sunfua thành lưu huỳnh, các vi sinh vật đã tránh không đụng đến asen, một chất độc với chúng.
Vào thời Home (khoảng thế kỉ 12- 9, TCN), những người cổ Hi Lạp đã biết đốt lưu huỳnh để tẩy uế nhà cửa, dùng khí thoát ra (SO2) để tẩy trắng sợi vải. Người xưa tin rằng, cái mùi và màu xanh của ngọn lửu lưu huỳnh có thể xua đuổi được ma quỷ
Thời trung cổ đã biêt dùng lưu huỳnh và hợp chất của lưu huỳnh để điều chế mĩ phẩm và chữa bệnh ngoài da. Thuốc súng có tên "Hi Lạp" mà người Hi Lạp năm 670 đã dùng để đốt cháy chiến thuyền của Ai cập, có thành phần (Lưu huỳnh, than, diêm tiêu) và tỉ lệ gần như thuôc súng ngày nay
Tính chất cháy được và khả năng hóa hợp dễ dàng với nhiều kim loại cho lưu huỳnh có vị trí ưu đãi đối với các nhà giả kim thuât thời trung cổ.
Thời trung cổ các nhà giả kim thuật tin tưởng mù quáng rằng: Các kim loại được cấu tạo từ sự kết hợp của Thủy Ngân và Lưu huỳnh. Sự kết hợp theo những tỉ lệ khác nhau thì tạo thành các kim loại khác nhau và đặc biệt là để tạo thành kim loại vàng thì phải pha trộn thủy ngân và lưu huỳnh theo một tỉ lệ "hoàn hảo nhất". Hơn 1000 năm, các nhà giả kim thuật đã tìm kiếm trong vô vọng các tỉ lệ hoàn hảo đó nhằm điều chế được Vàng.
Chương 7
A. TÓM TẮT LÍ THUYẾT
I. Tốc độ phản ứng hóa học
1. Khái niệm về tốc độ phản ứng hóa học
- Tốc độ phản ứng là độ biến thiên nồng độ của một trong các chất phản ứng hoặc sản phẩm trong một đơn vị thời gian.
Thí dụ: Nồng độ ban đầu của N2O5 là 2,33M, sau 184 giây nồng độ là 2,08M.
Tốc độ trung bình của phản ứng trong khoảng thời gian 184 giây tính theo N2O5 là:
N2O5 ![]() N2O4 +
N2O4 + ![]()
![]()
![]() + Công thức tổng quát tính tốc độ phản ứng :
+ Công thức tổng quát tính tốc độ phản ứng : ![]() hay
hay ![]()
![]() : tốc độ trung bình
: tốc độ trung bình
Trong đó: DC: biến thiên nồng độ
Dt: biến thiên thời gian
- Tổng quát:
+ Nếu: A + B ![]() C + D Þ V = K. [A]. [B]
C + D Þ V = K. [A]. [B]
+ Nếu : nA + mB ![]() pC + qD Þ V = K. [A]n. [B]m
pC + qD Þ V = K. [A]n. [B]m
(trong đó K là hằng số tốc độ phản ứng)
- Theo qui ước: nồng độ tính bằng mol/l, thời gian có thể là giây, phút, giờ.
- Tốc độ phản ứng được tính bằng thực nghiệm.
2. Các yếu tố ảnh hưởng đến tốc độ phản ứng
a. Ảnh hưởng của nồng độ
Khi tăng nồng độ chất phản ứng, tốc độ phản ứng tăng.
b. Ảnh hưởng của áp suất
Đối với phản ứng có chất khí tham gia, khi tăng áp suất, tốc độ phản ứng tăng.
c. Ảnh hưởng của nhiệt độ
Khi tăng nhiệt độ, tốc độ phản ứng tăng.
d. Ảnh hưởng của diện tích bề mặt
Đối với phản ứng có chất rắn tham gia, khi tăng diện tích bề mặt, tốc độ phản ứng tăng.
e. Ảnh hưởng của chất xúc tác
Chất xúc tác là chất làm tăng tốc độ phản ứng, nhưng không bị tiêu hao trong phản ứng.
3. Ý nghĩa thực tiễn của tốc độ phản ứng:
Các yếu tố ảnh hưởng đến tốc độ phản ứng được vận dụng nhiều trong đời sống sản xuất như:
+ Nhiệt độ ngọn lửa axetilen cháy trong oxi cao hơn rất nhiều so với cháy trong không khí, nên tạo nhiệt độ hàn cao hơn.
+ Nấu thực phẩm trong nồi áp suất nhanh chín hơn so với nấu ở áp suất thường.
+ Than, củi có kích thước nhỏ sẽ cháy nhanh hơn than, củi có kích thước lớn.
+ Dùng chất xúc tác, chọn nhiệt độ thích hợp, tăng áp suất chung của hệ khi tổng hợp NH3 từ N2 và H2.
II. Cân bằng hóa học
1. Phản ứng một chiều, phản ứng thuận nghịch và cân bằng hóa học
a. Phản ứng một chiều
- Thí dụ: Phân hủy KClO3 có xúc tác MnO2, phản ứng xảy ra như sau:
2KClO3 ![]() 2KCl + 3O2
2KCl + 3O2
Phản ứng này chỉ xảy ra theo một chiều từ trái sang phải. Phản ứng như thế được gọi là phản ứng một chiều. Dùng mũi tên chỉ chiều phản ứng.
b. Phản ứng thuận nghịch
- Trong cùng điều kiện phản ứng xảy ra theo hai chiều trái ngược nhau gọi là phản ứng thuận nghịch.
Phản ứng thuận Phản ứng nghịch![]()
![]() Thí dụ: Cl2 + H2O HCl + HClO
Thí dụ: Cl2 + H2O HCl + HClO
- Nhận xét: Cl2 phản ứng với H2O tạo HCl va HClO, đồng thời HCl và HClO sinh ra cũng tác dụng lại với nhau tạo lại Cl2 và H2O.
c. Cân bằng hóa học
- Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch (Vthuận =Vnghịch).
![]()
![]() Thí dụ: H2(k) + I2(k) 2HI(k)
Thí dụ: H2(k) + I2(k) 2HI(k)
d. Hằng số cân bằng (tính theo nồng độ) của phản ứng thuận nghịch:
![]() Nếu : A + B C + D Þ
Nếu : A + B C + D Þ 
![]() Tổng quát: nA + mB pC + qD
Tổng quát: nA + mB pC + qD

2. Sự chuyển dịch cân bằng hóa học
- Sự chuyển dịch cân bằng hóa học là sự di chuyển từ trạng thái cân bằng này sang trạng thái cân bằng khác do tác động của các yếu tố từ bên ngoài lên cân bằng.
![]() 2NO2 (khí màu nâu đỏ) N2O4(khí không màu)
2NO2 (khí màu nâu đỏ) N2O4(khí không màu)
3. Các yếu tố ảnh hưởng đến cân bằng hóa học
a. Ảnh hưởng của nồng độ
- Khi tăng hoặc giảm nồng độ một chất trong cân bằng, thì cân bằng bao giờ cũng dịch chuyển theo chiều làm giảm tác dụng của việc tăng hoặc giảm nồng độ chất đó.
b. Ảnh hưởng của áp suất
- Khi tăng hoặc giảm áp suất chung của hệ cân bằng, thì cân bằng bao giờ cũng dịch chuyển theo chiều làm giảm tác dụng của việc tăng hoặc giảm áp suất đó.
c. Ảnh hưởng của nhiệt độ
- Phản ứng tỏa nhiệt (![]() < 0 ): là phản ứng xảy ra có tỏa năng lượng dưới dạng ánh sáng hoặc sức nóng.
< 0 ): là phản ứng xảy ra có tỏa năng lượng dưới dạng ánh sáng hoặc sức nóng.
- Phản ứng thu nhiệt (![]() > 0 ): là phản ứng xảy ra có hấp thụ năng lượng.
> 0 ): là phản ứng xảy ra có hấp thụ năng lượng.
- Phương trình nhiệt hóa học: là phương trình hóa học có ghi cả hiệu ứng nhiệt.
- Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều phản ứng thu nhiệt, nghĩa là chiều làm giảm tác dụng của việc tăng nhiệt độ và khi giảm nhiệt độ, cân bằng chuyển dịch theo chiều phản ứng tỏa nhiệt, chiều làm giảm tác dụng của việc giảm nhiệt độ.
Kết luận (nguyên lý Lơ-Sa-tơ-liê):
Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu một tác động từ bên ngoài như biến đổi nồng độ, áp suất, nhiệt độ, sẽ chuyển dịch cân bằng theo chiều làm giảm tác động bên ngoài đó.
d. Vai trò của chất xúc tác
- Chất xúc tác làm tăng tốc độ phản ứng thuận và nghịch với số lần như nhau, cho nên không làm ảnh hưởng đến cân bằng hóa học.
4. Ý nghĩa của tốc độ phản ứng và cân bằng hóa học trong sản xuất hóa học.
- Quá trình sản xuất axit H2SO4, dùng lượng dư không khí (tăng nồng độ oxi) để phản ứng: 2SO2 + O2 ![]() 2SO3 ,
2SO3 , ![]() < 0 chuyển dịch theo chiều thuận.
< 0 chuyển dịch theo chiều thuận.
- Tổng hợp NH3 trong công nghiệp theo phản ứng:
N2(k) +3H2(k) ![]() 2NH3(k),
2NH3(k), ![]() < 0
< 0
Người ta phải thực hiện phản ứng này ở nhiệt độ thích hợp, áp suất cao và dùng chất xúc tác.
B. BÀI TẬP CÓ LỜI GIẢI
7.1 Trong quá trình đốt cháy các nhiên liệu như than đá, dầu mỏ và khí thiên nhiên, làm thế nào để nâng cao hiệu suất cung cấp nhiệt ?
7.2 Các yếu tố như nhiệt độ, áp suất chất khí, chất xúc tác và diện tích bề mặt chất rắn có ảnh hưởng lớn đến tốc độ phản ứng hóa học. Tùy theo phản ứng hóa học cụ thể mà vận dụng một, một số hay tất cả các yếu tố trên để tăng hay giảm tốc độ phản ứng. Trong những trường hợp dưới đây, yếu tố nào trong số các yếu tố trên ảnh hưởng đến tốc độ phản ứng?
a. Sự cháy diễn ra nhanh và mạnh hơn khi các viên than tổ ong được ép với các hàng lỗ rỗng .
b. Khi cần ủ bếp than, người ta đậy nắp bếp lò làm cho phản ứng cháy của than chậm lại.
c. Phản ứng oxi hóa lưu huỳnh đioxit tạo thành lưu huỳnh trioxit diễn ra nhanh hơn khi có mặt vanađi (V) oxit (V2O5).
d. Đá vôi được đập nhỏ, chín nhanh và đều hơn khi nung đá vôi ở dạng cục lớn.
e. Thức ăn sẽ nhanh chín hơn nếu được nấu trong nồi áp suất.
7.3 Nghiên cứu sự phụ thuộc của tốc độ phản ứng tổng hợp hiđro iotua vào nhiệt độ, trong một khoảng nhiệt độ xác định, người ta biết rằng khi nhiệt độ tăng lên 250C thì tốc độ của phản ứng hóa học này tăng lên 3 lần. Hỏi:
a. Tốc độ phản ứng hóa học trên tăng lên bao nhiêu lần khi nhiệt độ tăng từ 250C lên 750C ?
b. Tốc độ phản ứng hóa học trên giảm bao nhiêu lần khi nhiệt độ giảm từ 1700C xuống 950C ?
7.4 Bảng số liệu sau đây cho biết thể tích khí hiđro thu được theo thời gian phản ứng giữa kẽm dư với axit clohiđric. Hãy vẽ đồ thị biểu diễn sự phụ thuộc thể tích khí hiđro theo thời gian.
a. Từ đồ thị hãy cho biết khoảng thời gian nào phản ứng xảy ra nhanh nhất? Ở thời điểm phản ứng kết thúc, hình dạng đồ thị như thế nào?
Thời gian (s) | 0 | 20 | 40 | 60 | 80 | 100 | 120 | 140 |
Thể tích H2(ml) | 0 | 20 | 30 | 35 | 38 | 40 | 40 | 40 |
b. Nếu xác định được nồng độ của axit clohiđric theo thời gian phản ứng, thì đồ thị biểu diễn sự phụ thuộc đó có dạng như thế nào?
7.5 Khi bắt đầu phản ứng, nồng độ của một chất là 0,024 mol/l. Sau 20 giây phản ứng, nồng độ của chất đó là 0,020 mol/l. Hãy tính tốc độ trung bình của phản ứng này trong thời gian đã cho.
7.6 Cho phản ứng hóa học:
Công thức tính tốc độ của phản ứng trên là v = k [H2] [I2]. Tốc độ của phản ứng hóa học trên sẽ tăng bao nhiêu lần khi tăng áp suất chung của hệ lên 3 lần?
7.7 Hãy cho biết người ta đã sử dụng biện pháp nào để tăng tốc độ phản ứng hóa học trong các trường hợp sau đây:
a. Rắc men vào tinh bột đã được nấu chín (cơm, ngô, khoai, sắn...) để ủ rượu.
b. Dùng quạt thông gió trong bễ lò rèn.
c. Nén hỗn hợp khí nitơ và hiđro ở áp suất cao để tổng hợp amoniac.
d. Nung hỗn hợp bột đá vôi, đất sét và thạch cao ở nhiệt độ cao để sản xuất clinke, trong công nghiệp sản xuất xi măng.
e. Dùng phương pháp ngược dòng, trong sản xuất axit sunfuric. Hơi SO3 đi từ dưới lên, dung dịch axit H2SO4 đặc đi từ trên đỉnh tháp hấp thụ xuống.
7.8 Trong mỗi cặp phản ứng sau, phản ứng nào có tốc độ lớn hơn?
a. Fe + ddHCl 0,1M và Fe + ddHCl 2M ở cùng một nhiệt độ.
b. Al + ddNaOH 2M ở 250C và Al + ddNaOH 2M ở 500C.
c. Zn (hạt) + ddHCl 1M ở 250C và Zn (bột) + HCl1M ở 250C.
d. Nhiệt phân KClO3 và nhiệt phân hỗn hợp KClO3 với MnO2.
7.9 Cho phản ứng hóa học:
Tốc độ của phản ứng trên được xác định bởi biểu thức: v = k . [A2].[B]2.
Hỏi tốc độ phản ứng trên sẽ thay đổi như thế nào khi:
a. tăng áp suất chung của hệ lên 10 lần.
b. tăng nồng độ của B lên 3 lần.
c. giảm nồng độ A2 xuống 4 lần.
7.10 Cho phản ứng hóa học đang ở trạng thái cân bằng:
Hãy cho biết sự chuyển dịch cân bằng hóa học trên khi tăng nhiệt độ?
7.11 Từ thế kỷ XIX, người ta đã nhận ra rằng trong thành phần khí lò cao (lò luyện gang) vẫn còn khí cacbon monoxit (CO). Người ta đã tìm đủ mọi cách để phản ứng hóa học xảy ra hoàn toàn, tuy nhiên khí lò cao vẫn còn CO. Hãy cho biết nguyên nhân của hiện tượng trên?
A. Lò xây chưa đủ độ cao.
B. Nhiệt độ của lò còn thấp.
C. Phản ứng luyện quặng thành gang không hoàn toàn.
D. Một nguyên nhân khác.
7.12 Cho phương trình hóa học
2SO2 (k) + O2(k)  2SO3 (k); DH = -192kJ
2SO3 (k); DH = -192kJ
Cân bằng hóa học của phản ứng sẽ chuyển dịch về phía nào khi:
a. Tăng nhiệt độ của bình phản ứng?
b. Tăng áp suất chung của hỗn hợp?
c. Tăng nồng độ khí oxi ?
d. Giảm nồng độ khí sunfurơ ?
7.13 Sản xuất amoniac trong công nghiệp dựa trên phương trình hóa học sau :
2N2(k) + 3H2(k)  2NH3(k) ; DH = -92kJ
2NH3(k) ; DH = -92kJ
Cân bằng hóa học sẽ chuyển dịch về phía tạo ra amoniac nhiều hơn khi thực hiện những biện pháp kĩ thuật nào? Giải thích.
7.14 Phản ứng hóa học sau đã đạt trạng thái cân bằng:
Cân bằng hóa học sẽ chuyển dịch theo chiều nào khi:
A. Tăng nhiệt độ?
B. Tăng áp suất chung ?
C. Thêm khí trơ agon và giữ áp suất không đổi ?
D. Thêm chất xúc tác?
Hãy giải thích sự lựa chọn đó.
7.15 Sự tăng áp suất ảnh hưởng như thế nào đến trạng thái cân bằng của các phản ứng hóa học sau:
7.16 Phản ứng hóa học sau, diễn ra trong tự nhiên đang ở trạng thái cân bằng:
Khi tăng lượng CO2 cân bằng hóa học sẽ chuyển dịch sang chiều nào?
7.17 Trong công nghiệp, để điều chế khí than ướt, người ta thổi hơi nước qua than đá đang nóng đỏ. Phản ứng hóa học xảy ra như sau :
C (r) + H2O (k)  CO(k) + H2(k); DH = 131kJ
CO(k) + H2(k); DH = 131kJ
Điều khẳng định nào sau đây là đúng?
A. Tăng áp suất chung của hệ làm cân bằng không thay đỏi.
B. Tăng nhiệt độ của hệ làm cân bằng chuyển sang chiều thuận.
C. Dùng chất xúc tác làm cân bằng chuyển sang chiều thuận.
D. Tăng nồng độ hiđro làm cân bằng chuyển sang chiều thuận.
7.18 Clo tác dụng với nước một phần nhỏ theo phương trình hóa học sau:
Hai sản phẩm tạo ra đều tan tốt trong nước tạo thành dung dịch. Ngoài ra một phần lớn khí clo tan trong nước tạo thành dung dịch có màu vàng lục nhạt gọi là nước clo. Nước clo, đựng trong bình kín, dần dần bị mất màu theo thời gian, không bảo quản được lâu, vận dụng những hiểu biết về chuyển dịch cân bằng hóa học hãy giải thích hiện tượng trên.
7.19 Sản xuất vôi trong công nghiệp và thủ công nghiệp đều dựa trên phản ứng hóa học: CaCO3(r)  CaO(r) + CO2(k), DH = 178kJ
CaO(r) + CO2(k), DH = 178kJ
a. Hãy phân tích các đặc điểm của phản ứng hóa học nung vôi.
b. Từ những đặc điểm đó, hãy cho biết những biện pháp kĩ thuật nào được sử dụng để nâng cao hiệu suất của quá trình nung vôi.
7.20 Một phản ứng hóa học có dạng:
Hãy cho biết các biện pháp cần tiến hành để chuyển dịch cân bằng hóa học sang chiều thuận?
7.21 Cho các phản ứng hóa học
C(r) + H2O (k)  CO(k) + H2(k); DH = 131kJ (1)
CO(k) + H2(k); DH = 131kJ (1)
2SO2(k) + O2(k)  2SO3(k); DH = -192kJ (2)
2SO3(k); DH = -192kJ (2)
a. Hãy so sánh các đặc điểm của hai phản ứng hóa học trên.
b. Nêu các biện pháp kĩ thuật để làm tăng hiệu suất sản xuất.
7.22 Cho phản ứng hóa học:
2NO(k) + O2(k) ® 2NO2(k)
Tốc độ phản ứng hóa học trên được tính theo công thức v = k [NO]2[O2]. Hỏi ở nhiệt độ không đổi, áp suất chung của hệ đã tăng bao nhiêu lần khi tốc độ của phản ứng tăng 64 lần?
7.23 Người ta đã sử dụng nhiệt của phản ứng đốt cháy than đá để nung vôi:
C(r) + O2 (k) ® CO2(k); DH = - 393,5kJ (1)
CaCO3(r)  CaO(r) + CO2(k) ; DH = 178kJ (2)
CaO(r) + CO2(k) ; DH = 178kJ (2)
Biện pháp kĩ thuật nào sau đây không được sử dụng để tăng tốc độ phản ứng nung vôi?
A. Đập nhỏ đá vôi với kích thước thích hợp.
B. Duy trì nhiệt độ phản ứng thích hợp.
C. Tăng nhiệt độ phản ứng càng cao càng tốt.
D. Thổi không khí nén vào lò nung vôi.
 7.24 Đồ thị nào sau đây biểu diễn sự biển đổi tốc độ phản ứng thuận theo thời gian? Sự biển đổi tốc độ phản ứng nghịch theo thời gian? Trạng thái cân bằng hóa học?
7.24 Đồ thị nào sau đây biểu diễn sự biển đổi tốc độ phản ứng thuận theo thời gian? Sự biển đổi tốc độ phản ứng nghịch theo thời gian? Trạng thái cân bằng hóa học?
v v
a. b.
t (thời gian) t (thời gian)
v
c.
t (thời gian)
7.25 Trong nước ngầm thường có ion Fe2+ dưới dạng muối sắt II hiđrocacbonat và sắt II hiđroxit. Nước sinh hoạt có chứa Fe2+ ảnh hưởng xấu đến sức khoẻ của con người. Để loại bỏ Fe2+, trong một phương pháp đơn giản, rẻ tiền, nguời ta dùng oxi không khí oxi hóa Fe2+ thành hợp chất Fe3+ (có độ tan trong nước nhỏ) rồi lọc để thu nước sạch. Để tăng tốc độ của phản ứng oxi hóa Fe2+ người ta sử dụng biện pháp kĩ thuật nào? Giải thích.
7.26 Gần đây, khi thám hiểm Nam cực, các nhà khoa học đã tìm thấy những đồ hộp do các đoàn thám hiểm trước để lại. Mặc dù đã qua hàng trăm năm, nhưng các thức ăn trong những đồ hộp đó vẫn trong tình trạng tốt, có thể ăn được. Hãy giải thích và liên hệ với việc bảo quản thực phẩm bằng cách ướp đá hay dùng tủ lạnh.
7.27 Trong phòng thí nghiệm, để tăng tốc độ của một số phản ứng hóa học, ngoài các biện pháp như tăng nồng độ, nhiệt độ, người ta còn dùng máy khuấy. Tác dụng của máy khuấy là gì?
7.28 Hãy trình bày thí nghiệm đốt cháy dây sắt mảnh trong bình khí oxi. Vận dụng lí thuyết phản ứng hóa học để giải thích cách tiến hành thí nghiệm trên.
7.29 Làm thế nào để điều khiển các phản ứng hóa học theo hướng có lợi nhất cho con người?
7.30 Tốc độ của phản ứng tăng bao nhiêu lần nếu tăng nhiệt độ từ 2000C đến 2400C, biết rằng khi tăng 100C thì tốc độ phản ứng trên tăng hai lần.
7.31 Hãy chọn từ hoặc cụm từ cho sẵn trong bảng dưới đây vào chỗ trống trong
câu sau :
Tốc độ phản ứng là độ biến thiên ...(1)... của một trong...(2)... hoặc sản phẩm phản ứng trong ...(3)... thời gian.
A. | B. | C. | D. | |
(1) | khối lượng | nồng độ | thể tích | phân tử khối |
(2) | các chất phản ứng | các chất tạo thành | các chất bay hơi | các chất kết tủa |
(3) | một khoảng | một đơn vị | một | mọi khoảng |
7.32 Chọn các từ, cụm từ cho dưới đây điền vào chỗ trống (1), (2),... cho thích hợp.
Tốc độ phản ứng là ...(1)...của một ...(2)....phản ứng hoặc ...(3)... trong một ...(4).... thời gian. Tốc độ phản ứng hóa học phụ thuộc vào nhiệt độ, nồng độ và áp suất đối với ...(5)...
A. | B. | C. | D. | |
(1) | sự thay đổi | độ biến thiên | độ tăng | độ giảm |
(2) | trong các chất | giai đoạn | số chất | loại hợp chất |
(3) | chất xúc tác | chất trung gian | chất ban đầu | sản phẩm phản ứng |
(4) | chu kì | khoảng | đơn vị | biến thiên |
(5) | chất lỏng | chất rắn | chất khí | chất tan |
Thứ tự điền từ: 1... 2.... 3... 4..... 5.....
7.33 Chọn các từ, cụm từ cho dưới đây điền vào chỗ trống (1), (2),... cho thích hợp.
Khi tăng nồng độ chất phản ứng, tốc độ phản ứng ...(1)... Đối với phản ứng có chất khí tham gia, khi tăng áp suất, ...(2)... phản ứng tăng. Đối với phản ứng có chất rắn tham gia, khi tăng ....(3)... bề mặt, tốc độ phản ứng ...(4).... Lưu ý đối với phản ứng hóa học có chất ...(5)....tham gia, nồng độ của chúng không ảnh hưởng đên tốc độ của phản ứng.
A | B. | C. | D. | |
(1) | giảm | không đổi | biến đổi | tăng |
(2) | khối lượng | tốc độ | hiệu suất | thể tích |
(3) | diện tích | kích thước | hình dạng | độ dày |
(4) | biến đổi | tăng | giảm | không đổi |
(5) | Lỏng | khí | Rắn | tan |
Thứ tự ghép nối: 1... 2.... 3... 4..... 5......
7.34 Hãy ghép mệnh đề ở cột A với cột B sao cho phù hợp.
Cột 1 | Cột 2 | ||
1 | Đối với phản ứng có chất khí tham gia, khi tăng áp suất | a | tốc độ phản ứng giảm. |
2 | Đối với phản ứng có chất khí tham gia, khi giảm áp suất | b | cân bằng hóa học chuyển dịch theo chiều thuận. |
3 | Đối với phản ứng tỏa nhiệt, khi tăng nhiệt độ | c | tốc độ phản ứng tăng. |
4 | Đối với phản ứng tỏa nhiệt, khi giảm nhiệt độ | d | cân bằng hóa học chuyển dịch theo chiều nghịch. |
e | cân bằng hóa học không bị chuyển dịch. |
Thứ tự ghép nối: 1. .............. 2. .............. 3. .............. 4. ...............
7.35 Khi đốt 19,4 gam muối sunfua của một kim loại hóa trị II thì cần vừa đủ 6,72 lít khí oxi (đktc) thì thu được khí A. Khí A sinh ra được oxi hóa tiếp bằng khí oxi có xúc tác V2O5 tạo thành chất lỏng B ở điều kiện thường. Hòa tan B vào nước thu được dung dịch làm đỏ giấy quỳ tím.
a. Xác định kim loại trong muối sunfua.
b. Tính số ml dung dịch KOH 33,6% (d = 1,33g/ml) cần dùng để trung hòa lượng axit thu được ở trên.
c. Cho biết các biện pháp kĩ thuật cần thiết để tăng hiệu quả quá trình oxi khí A trong công nghiệp?
![]() Đáp số: a. Kim loại hóa trị II là Zn
Đáp số: a. Kim loại hóa trị II là Zn
b. 50,12 9(ml).
c. Dùng xúc tác, tăng nồng độ oxi, duy trì nhiệt độ thích hợp.
7.36 Nén 2,0 mol N2 và 8,0 mol H2 vào một bình kín có thể tích 2,0 lít (chỉ chứa sẵn chất xúc tác với thể tích không đáng kể) đã được giữ ở nhiệt độ không đổi. Khi phản ứng đạt tới cân bằng, áp suất các khí trong bình bằng 0,8 lần áp suất ban đầu (khi mới cho các chất vào bình chưa xảy ra phản ứng). Tính nồng độ các chất ở trạng thái cân bằng.
Đáp số:  (mol/l);
(mol/l);  (mol/l);
(mol/l);  (mol/l).
(mol/l).
7.37 Hỏi tốc độ một phản ứng hóa học tăng bao nhiêu lần khi nhiệt độ tăng từ 250C đến 850C. Biết khi tăng nhiệt độ lên 100C, tốc độ của phản ứng trên tăng lên 3 lần. Người ta nói rằng hệ số nhiệt độ của phản ứng đã cho bằng 3.
Đáp số: Tốc độ phản ứng tăng 36 lần = 729 lần.
7.38 Trong các cân bằng sau, cân bằng nào sẽ chuyển dịch và chuyển dịch theo chiều nào khi giảm dung tích của bình phản ứng xuống ở nhiệt độ không đổi.
a) CH4(k) + H2O(k) ![]() CO(k) + 3H2(k)
CO(k) + 3H2(k)
b) CO2(k) + H2(k) ![]() CO(k) + H2O(k)
CO(k) + H2O(k)
c) SO2(k) + O2(k) ![]() 2SO3(k)
2SO3(k)
d) N2O4(k) ![]() 2NO2(k)
2NO2(k)
7.39 Hãy cho biết người ta lợi dụng yếu tố nào để tăng tốc độ phản ứng trong các trường hợp sau:
a) Dùng không khí nén, nóng thổi vào lò cao để đốt cháy than cốc (sản xuất gang).
b) Nung đá vôi ở nhiệt độ cao để sản xuất vôi sống.
c) Nghiền nguyên liệu trước khi đưa vào lò nung để sản xuất clanhke (sản xuất xi măng)
7.40 Nồng độ ban đầu của SO2 và O2 trong hệ: 2SO2 + O2 ![]() 2SO3 tương ứng là 4 mol/l và 2 mol/l. ở nhiệt độ không đổi, nếu tăng áp suất hỗn hợp phản ứng lên hai lần thì cân bằng chuyển dịch theo chiều nào? (trả lời theo kết quả tính toán).
2SO3 tương ứng là 4 mol/l và 2 mol/l. ở nhiệt độ không đổi, nếu tăng áp suất hỗn hợp phản ứng lên hai lần thì cân bằng chuyển dịch theo chiều nào? (trả lời theo kết quả tính toán).
7.41 Khí NO2 nhị hợp theo phản ứng thuận nghịch: 2NO2 ![]() N2O4. Trong đó: NO2 là khí màu nâu; N2O4 là khí không màu.
N2O4. Trong đó: NO2 là khí màu nâu; N2O4 là khí không màu.
a) Khi giảm áp suất của hệ phản ứng, cân bằng chuyển dịch theo chiều nào?
Giải thích.
b) Khi ngâm bình chứa NO2 vào nước đá, thấy mầu nâu của bình nhạt dần. Hãy cho biết phản ứng tỏa nhiệt hay thu nhiệt? Giải thích.
7.42 Cho 15 gam axit CH3COOH tác dụng với 9,6 gam rượu CH3OH có xúc tác là H2SO4 đặc. Chia hỗn hợp sau phản ứng thành hai phần bằng nhau:
Phần 1: Cho tác dụng với lượng dư BaCl2 thu được 23,3 gam kết tủa.
Phần 2: Cho tác dụng với KHCO3 thu được 5,6 lít khí CO2(ở đktc).
Tính hằng số cân bằng của phản ứng.
7.43 Cho khí HI vào một bình kín có dung tích là 5 lít, rồi đun nóng đến nhiệt độ xác định thì xảy ra phản ứng: 2HI(khí) ![]() H2 (khí) + I2(khí); DH =- 52kJ. Nếu nồng độ ban đầu của HI là 0,5 mol, khi ở trạng thái cân bằng nồng độ mol/l của các chất trong phản ứng [HI], [H2] và [I2] lần lượt là bao nhiêu?
H2 (khí) + I2(khí); DH =- 52kJ. Nếu nồng độ ban đầu của HI là 0,5 mol, khi ở trạng thái cân bằng nồng độ mol/l của các chất trong phản ứng [HI], [H2] và [I2] lần lượt là bao nhiêu?
7.44 Cho năng lượng liên kết của H2O là 971 kJ/mol; của H2 là 435,9 kJ/ mol. của O2 là 498,7 kJ/mol. Nhiệt của phản ứng: 2H2O ![]() 2H2 + O2 là bao nhiêu?
2H2 + O2 là bao nhiêu?
7.45 Khi đốt cháy 2,0 mol hiđro photphua (PH3) thì tạo thành điphotphopentoxit (P2O5), nước và giải phóng 2440 kJ. Hãy tính nhiệt tạo thành PH3, biết nhiệt tạo thành P2O5 là 1548 kJ/mol và nhiệt tạo thành H2O là 286 kJ/mol.
7.46 Trong một bình kín chứa khí propan được đóng kín bằng pittong. Đốt nóng bình lên tới 5270C , phản ứng xảy ra trong bình: C3H8 ![]() C3H6 + H2
C3H6 + H2
Với hằng số cân bằng là 1,3 . 10-3. Tại thời điểm cân bằng C3H8 chiếm 80% thể tích.
a) Tính thành phần % thể tích của C3H6 và H2.
b) Tính nồng độ các chất lúc cân bằng và áp suất của hệ tại nhiệt độ đã cho.
c) Nếu sử dụng pittong để nén thể tích bình còn một nửa thể tích ban đầu tại nhiệt độ không đổi. Tính áp suất cân bằng trong bình.
D. BÀI TẬP TRẮC NGHIỆM
Fe, P
7.47 Cho phản ứng hóa học:
Trong phản ứng tổng hợp amoniac, yếu tố nào sau đây không làm thay đổi trạng thái cân bằng hóa học?
A. Nồng độ của N2 và H2.
B. Áp suất chung của hệ.
C. Chất xúc tác Fe.
D. Nhiệt độ của hệ.
7.48 Sự tăng áp suất có ảnh hưởng như thế nào đến trạng thái cân bằng hóa học của phản ứng:
A. Cân bằng chuyển dịch sang chiều thuận.
B. Cân bằng dịch chuyển theo chiều nghịch.
C. Cân bằng không thay đổi.
D. Phản ứng trở thành một chiều.
7.49 Cho phản ứng : X ® Y
Tại thời điểm t1 nồng độ của chất X bằng C1, tại thời điểm t2 (với t2> t1), nồng độ của chất X bằng C2. Tốc độ trung bình của phản ứng trong khoảng thời gian trên được tính theo biểu thức nào sau đây ?
7.50 Khi cho cùng một lượng dung dịch axit sunfuric vào hai cốc đựng cùng một thể tích dung dịch Na2S2O3 với nồng độ khác nhau, ở cốc đựng dung dịch Na2S2O3 có nồng độ lớn hơn thấy kết tủa xuất hiện trước.
Điều đó chứng tỏ ở cùng điều kiện về nhiệt độ, tốc độ phản ứng:
A. Không phụ thuộc vào nồng độ của chất phản ứng.
B. Tỉ lệ thuận với nồng độ của chất phản ứng.
C. Tỉ lệ nghịch với nồng độ của chất phản ứng.
D. Không thay đổi khi thay đổi nồng độ của chất phản ứng.
Hãy chọn đáp án đúng.
7.51 Đối với các phản ứng có chất khí tham gia, khi tăng áp suất, tốc độ phản ứng tăng là do
A. Nồng độ của các chất khí tăng lên.
B. Nồng độ của các chất khí giảm xuống.
C. Chuyển động của các chất khí tăng lên.
D. Nồng độ của các chất khí không thay đổi.
Hãy chọn đáp án đúng.
7.52 Đồ thị dưới đây biểu diễn sự phụ thuộc của tốc độ phản ứng vào nhiệt độ.
Từ đồ thị trên, ta thấy tốc độ phản ứng:
A. Giảm khi nhiệt độ của phản ứng tăng.
B. Không phụ thuộc vào nhiệt độ của phản ứng.
C. Tỉ lệ thuận với nhiệt độ của phản ứng.
D. Tỉ lệ nghịch với nhiệt độ của phản ứng.
7.53 Đồ thị dưới đây biểu diễn sự phụ thuộc của tốc độ phản ứng vào nồng độ chất phản ứng.
Từ đồ thị trên, ta thấy tốc độ phản ứng
A. Giảm khi nồng độ của chất phản ứng tăng.
B. Không phụ thuộc vào nồng độ của chất phản ứng.
C. Tỉ lệ thuận với nồng độ của chất phản ứng.
D. Tỉ lệ nghịch với nồng độ của chất phản ứng.
· Cho các phương trình hóa học sử dung cho các bài tập 7.54, 7.55, 7.56 sau :
c) CaCO3 (r)  CaO (r) + CO2 (k)
CaO (r) + CO2 (k)
d) 2Fe2O3 (r) + 3C (r)  4Fe (r) + 3CO2 (k)
4Fe (r) + 3CO2 (k)
e) Fe (r) + H2O (h)  FeO (r) + H2 (k)
FeO (r) + H2 (k)
g) Cl2 (k) + H2S (k)  2HCl (k) + S (r)
2HCl (k) + S (r)
h) Fe2O3 (r) + 3CO (k)  2Fe (r) + 3CO2 (k)
2Fe (r) + 3CO2 (k)
7.54 Các phản ứng có tốc độ phản ứng tăng khi tăng áp suất chung của hệ là:
A. a, f. C. a, c, d, e, f, g.
B. a, g. D. a, b, g.
7.55. Các phản ứng có tốc độ phản ứng giảm khi tăng áp suất của hệ là
A. a, b, e, f, h. C. b, e, h.
B. a, b, c, d, e. D. c, d.
7.56. Các phản ứng có tốc độ phản ứng không thay đổi khi tăng áp suất của hệ là
A. a, b, e, f. C. b, e, g, h.
B. a, b, c, d, e. D. d, e, f, g.
Hãy chọn đáp án đúng.
7.57 Định nghĩa nào sau đây là đúng ?
A. Chất xúc tác là chất làm thay đổi tốc độ phản ứng, nhưng không bị tiêu hao trong phản ứng.
B. Chất xúc tác là chất làm tăng tốc độ phản ứng, nhưng không bị tiêu hao trong phản ứng.
C. Chất xúc tác là chất làm tăng tốc độ phản ứng, nhưng không bị thay đổi trong phản ứng.
D. Chất xúc tác là chất làm thay đổi tốc độ phản ứng, nhưng bị tiêu hao không nhiều trong phản ứng.
7.58 Khi cho cùng một lượng nhôm vào cốc đựng dung dịch axit HCl 0,1M, tốc độ phản ứng sẽ lớn nhất khi dùng nhôm ở dạng nào sau đây?
A. Dạng viên nhỏ.
B. Dạng bột mịn, khuấy đều.
C. Dạng tấm mỏng.
D. Dạng nhôm dây.
Hãy chọn đáp án đúng.
7.59 Khi cho axit clohiđric tác dụng với kali pemanganat (rắn) để điều chế clo, khí clo sẽ thoát ra nhanh hơn khi:
A. Dùng axit clohiđric đặc và đun nhẹ hỗn hợp.
B. Dùng axit clohiđric đặc và làm lạnh hỗn hợp.
C. Dùng axit clohiđric loãng và đun nhẹ hỗn hợp.
D. Dùng axit clohiđric loãng và làm lạnh hỗn hợp.
7.60 Trong một bình kín chứa 10 lít nitơ và 10 lít hiđro ở nhiệt độ 00C và 10 atm. Sau phản ứng tổng hợp NH3, lại đưa bình về 00C. Biết rằng có 60% hiđro tham gia phản ứng, áp suất trong bình sau phản ứng là:
A. 10 atm B. 8 atm C. 9 atm D. 8,5 atm
7.61 Tốc độ của phản ứng sẽ tăng lên bao nhiêu lần khi tăng nhiệt độ từ 20oC đến 100oC, nếu hệ số nhiệt độ của phản ứng đã cho bằng 2?
A. 256 lần B. 265 lần C. 275 lần D. 257 lần
7.62 Hằng số cân bằng Kc của phản ứng chỉ phụ thuộc vào yếu tố nào sau đây? A. Nồng độ B. Áp suất C. Nhiệt độ D. Chất xúc tác.
7.63 Biết nhiệt tạo thành của Ca(OH)2, H2O, CaO tương ứng là -985,64;-286;
- 635,36 (kJ). Nhiệt phản ứng toả ra khi tôi 56 gam vôi là
A.- 46,28 kJ B.-64,82kJ C.- 64,28 kJ D.- 46,82 kJ
7.64 Một phản ứng thuận nghịch đạt đến trạng thái cân bằng khi nào?
A. Phản ứng thuận đã kết thúc
B. Phản ứng nghịch đã kết thúc
C. Tồc độ của phản ứng thuận và nghịch bằng nhau.
D. Nồng độ của các chất tham gia phản ứng và của các chất sản phẩm
phản ứng bằng nhau
7.65 Xét phản ứng thuận nghịch sau:
H2 (k) + I2 (k) ![]() 2HI (k)
2HI (k)
Đồ thị biểu diễn sự biến thiên tốc độ phản ứng thuận và phản ứng nghịch theo thời gian:
Tại thời điểm nào phản ứng đạt trạng thái cân bằng?
A. 0 giây B. 5 giây C. 10 giây D. 15 giây
7.66 Cho hình vẽ về cách thu khí trong phòng thí nghiệm bằng cách dời nước. Hình vẽ bên có thể áp dụng để thu được những khí nào trong các khí sau đây?
A)H2, N2, O2, CO2, HCl, H2S B)O2, N2, H2, CO2, SO2, C)NH3, HCl, CO2, SO2, Cl2 D)NH3, O2, N2, HCl, CO2 |
|
7.67 Nhận định nào sau đây đúng?
A. Hằng số cân bằng KC của mọi phản ứng đều tăng khi tăng nhiệt độ
B. Phản ứng một chiều không có hằng số cân bằng KC.
C. Hằng số cân bằng KC càng lớn, hiệu suất phản ứng càng nhỏ.
D. Khi một phản ứng thuận nghịch ở trạng thái cân bằng cũ chuyển sang một trạng thái cân bằng mới ở nhiệt độ không đổi, hằng số cân bằng KC biến đổi.
7.68 Cho phản ứng nung vôi CaCO3 ® CaO + CO2
Để tăng hiệu suất của phản ứng thì biện pháp nào sau đây không phù hợp?
A. Tăng nhiệt độ trong lò B. Tăng áp suất trong lò
C. Đập nhỏ đá vôi D. Giảm áp suất trong lò
7.69 Cho phản ứng 2SO2 + O2  2SO3
2SO3
Nồng độ ban đầu của SO2 và O2 tương ứng là 4 mol/L và 2 mol/L. Khi cân bằng, có 80% SO2 đã phản ứng, hằng số cân bằng của phản ứng là
A. 40 B. 30 C. 20 D. 10
7.70 Phản ứng giữa hai chất A và B được biểu thị bằng phương trình hóa học sau
A + B ® 2C
Tốc độ phản ứng này là V = K.[A].[B]. Thực hiện phản ứng này với sự khác nhau về nồng độ ban đầu của các chất:
Trường hợp 1 Nồng độ của mỗi chất là 0,01 mol/l.
Trường hợp 2 Nồng độ của mỗi chất là 0,04 mol/l
Trường hợp 3 Nồng độ của chất A là 0,04 mol/l, của chất B là 0,01 mol/l.
Tốc độ phản ứng ở trường hợp 2 và 3 lớn hơn so với trường 1 số lần là
A. 12 và 8 B. 13 và 7 C. 16 và 4 D 15 và 5
7.71 Biết nhiệt tạo thành CH4 là -75kJ/ mol; của CO2 là -393 kJ/mol và của H2O là -286 kJ/ mol. Nhiệt của phản ứng CH4 + O2  CO2 + 2H2O là
CO2 + 2H2O là
A. -900 kJ B. -890 kJ. C. -880 kJ D. -870 kJ
7.72 Cho phương trình hoá học
Hãy cho biết cặp yếu tố nào sau đây đều ảnh hưởng đến sự chuyển dịch cân bằng hoá học trên?
A. Nhiệt độ và nồng độ B. Áp suất và nồng độ
C. Nồng độ và chất xúc tác D. Chất xúc tác và nhiệt độ
 7.73 Cho hình vẽ mô tả sự điều chế clo trong phòng thí nghiệm như sau:
7.73 Cho hình vẽ mô tả sự điều chế clo trong phòng thí nghiệm như sau:
Vai trò của dung dịch NaCl là:
A.Hòa tan khí clo. B.Giữ lại khí hiđroclorua.
C.Giữ lại hơi nước D.Cả 3 đáp án trên đều đúng.
7.74 Khí hiđroclorua là chất khí tan rất nhiều trong nước tạo thành dung dịch axit clohdric.Trong thí nghiệm thử tính tan của khí hidroclorua trong nước, có hiện tượng nước phun mạnh vào bình chứa khí như hình vẽ mô tả dưới đây.
 Nguyên nhân gây nên hiện tượng đó là do:
Nguyên nhân gây nên hiện tượng đó là do:
A. khí HCl tác dụng với nước kéo nước vào bình.
B. HCl tan mạnh làm giảm áp suất trong bình.
C. trong bình chứa khí HCl ban đầu không có nước.
D.Tất cả các nguyên nhân trên đều đúng
 7.75 Cho dung dịch HCl đặc vào ống nghiệm đựng MnO2. Dụng cụ thí nghiệm được lắp như hình vẽ bên.
7.75 Cho dung dịch HCl đặc vào ống nghiệm đựng MnO2. Dụng cụ thí nghiệm được lắp như hình vẽ bên.
Hiện tượng xảy ra trong thí nghiệm bên là:
A.Có khí màu vàng sinh ra, đồng thời có kết tủa
B.Chỉ có khí màu vàng thoát ra
C.Chất rắn MnO2 tan dần
D.Cả B và C
7.76 Cho thí nghiệm được lắp như như hình vẽ sau:
 Ống nghiệm 1 đựng HCl và Zn, ống nghiệm nằm ngang chứa bột S, ống nghiệm 2 chứa dung dịch Pb(NO3)2 . Phản ứng xảy ra trong
Ống nghiệm 1 đựng HCl và Zn, ống nghiệm nằm ngang chứa bột S, ống nghiệm 2 chứa dung dịch Pb(NO3)2 . Phản ứng xảy ra trong
ống nghiệm nằm ngang là:
A.Zn + 2HCl → ZnCl2 + H2
B.H2 + S → H2S
C.H2S + Pb(NO3)2 → PbS↓ + 2HNO3
D.2HCl + Pb(NO3)2 → PbCl2↓ + 2HNO3
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP
7.47. C | 7.48. C | 7.49. C | 7.50. B | 7.51. A |
7.52. C | 7.53. C | 7.54. A | 7.55. D | 7.56. C |
7.57. B | 7.58. B | 7.59. A | 7.60. B | 7.61. A |
7.62. C | 7.63. C | 7.64. C | 7.65. C | 7.66. B |
7.67. A | 7.68. B | 7.69. A | 7.70. C | 7.71. B |
7.72. A | 7.73. B | 7.74. B | 7.75. D | 7.76. B |
7.1 Để nâng cao hiệu suất cung cấp năng lượng cần đốt các nhiên liệu với các biện pháp kĩ thuật sau:
- Dùng dư không khí để cung cấp oxi cho phản ứng cháy hoàn toàn.
- Đập nhỏ than đá đến kích thức thích hợp để tăng diện tích tiếp xúc giữa than và khí oxi.
- Sử dụng các động cơ đieden và các động cơ đốt trong để nâng cao hiệu suất sử dụng dầu mỏ và khí thiên nhiên.
7.2 Các yếu tố ảnh hưởng đến tốc độ phản ứng trong mỗi trường hợp đã cho là:
a. Tăng diện tích bề mặt của chất rắn tham gia phản ứng (than đá) làm tăng tốc độ phản ứng.
b. Giảm nồng độ chất tham gia phản ứng (khí oxi) làm giảm tốc độ phản ứng.
c. V2O5 là chất xúc tác, làm tăng tốc độ phản ứng.
d. Giảm kích thước hạt để tăng tốc độ phản ứng.
e. Thức ăn sẽ nhanh chín hơn nếu được nấu trong nồi áp suất, người ta đã sử dụng yếu tố nhiệt độ và áp suất cao để tăng tốc độ của phản ứng hóa học.
7.3 a. Từ 250C lên 750C, nhiệt độ của phản ứng hóa học đã tăng thêm là:
75 0C - 250C = 500C. Do đó, tốc độ phản ứng tăng thêm = 32 = 9 (lần).
b. Từ 1700C xuống 950C, nhiệt độ của phản ứng hóa học đã giảm đi là: 1700C - 950C = 750C. Do đó, tốc độ phản ứng giảm = 33 = 27 (lần)
7.4 a. ![]() (ml)
(ml)
Từ 0 đến 20 giây là đoạn đồ thị dốc nhất, khoảng thời gian có tốc độ phản ứng cao nhất.
Đoạn đồ thị nằm ngang, khi thể tích hiđro đạt cực đại (40ml) là khi phản ứng hóa học kết thúc, axit clohiđric đã phản ứng hết.
b. CM HCl

0
thời gian t (s)
Dạng đồ thị biểu diễn sự phụ thuộc của nồng độ axit HCl theo thời gian.
7.5 Tốc độ phản ứng trung bình:
![]() =
= ![]() = 0,0002 (mol/L.s)
= 0,0002 (mol/L.s)
7.6 Giải: v = k [3H2] [3I2] = 9.k. [H2] [I2]
Như vậy tốc độ phản ứng tăng 9 lần.
7.7 a. Men rượu là một loại xúc tác sinh học. Chất xúc tác đã được sử dụng để tăng tốc độ của phản ứng hóa học.
b. Bễ lò rèn có mục đích tăng nồng độ của oxi không khí, do đó làm tăng tốc độ của phản ứng cháy của than đá.
c. Nén hỗn hợp khí nitơ và hiđro ở áp suất cao để tăng nồng độ của hai chất khí, làm tăng tốc độ của phản ứng hóa học.
d. Dùng biện pháp tăng nhiệt độ để tăng tốc độ của phản ứng hóa học.
e. Dùng phương pháp ngược dòng, anhiđrit sunfuric đi từ dưới lên, axit sunfuric 98% đi từ trên đỉnh tháp hấp thụ xuống để tăng diện tích tiếp xúc giữa các chất, do đó, làm tăng tốc độ của phản ứng hóa học.
7.8 a. Ở cùng một nhiệt độ, cặp chất Fe + ddHCl 0,1M có tốc độ phản ứng xảy ra chậm hơn so với cặp chất Fe + ddHCl 2M, do nồng độ HCl nhỏ hơn..
b. Hai cặp chất Al + ddNaOH 2M ở 250C và Al + ddNaOH 2M ở 500C chỉ khác nhau về nhiệt độ. Cặp chất thứ hai có nhiệt độ cao hơn nên có tốc độ phản ứng cao hơn.
c. Hai cặp chất Zn (hạt) + ddHCl 1M ở 250C và Zn (bột) + HCl1M ở 250C chỉ khác nhau về kích thước hạt. Cặp chất thứ hai có kích thước hạt nhỏ hơn, do đó có tốc độ phản ứng cao hơn.
d. Nhiệt phân KClO3 và nhiệt phân hỗn hợp KClO3 với MnO2. Trường hợp thứ hai có xúc tác nên có tốc độ phản ứng cao hơn.
7.9 Khi tăng áp suất chung của hệ lên 10 lần thì nồng độ của mỗi chất cũng tăng 10 lần, do đó v2 = k[10A2][10B]2
Þ ![]() = 10 x 102 = 1000 (lần).
= 10 x 102 = 1000 (lần).
b. Tăng nồng độ của B lên 3 lần, tương tự ta có ![]() = 32 = 9 (lần).
= 32 = 9 (lần).
c. Giảm nồng độ A2 xuống 4 lần, tương tự ta có ![]() =
= ![]() tốc độ phản ứng giảm 4 lần.
tốc độ phản ứng giảm 4 lần.
7.10 Xét phương trình hóa học:
N2 (k) + O2(k) ![]() 2NO (k); DH > 0
2NO (k); DH > 0
Đặc điểm của phản ứng hóa học trên là thuận nghịch, phản ứng thuận thu nhiệt và tất cả các chất tham gia và tạo thành đều là chất khí. Tuy nhiên, tổng số mol khí trước và sau phản ứng không thay đổi, do đó áp suất không ảnh hưởng gì đến sự chuyển dịch cân bằng.
Khi tăng nhiệt độ phản ứng đã cho chuyển sang chiều nghịch.
7.11 Đáp án C.
Phản ứng hóa học khử sắt oxit bằng cacbon monoxit là không hoàn toàn. Do đó, dù có tăng chiều cao của lò đến bao nhiêu đi nữa thì chỉ gây lãng phí, trong thành phần của khí lò cao vẫn có khí CO.
7.12 Xét phương trình hóa học
2SO2 (k) + O2(k) ![]() 2SO3 (k) DH = -192kJ
2SO3 (k) DH = -192kJ
a. Khi tăng nhiệt độ của bình phản ứng cân bằng hóa học của phản ứng sẽ chuyển dịch về phía nghịch, vì phản ứng thuận tỏa nhiệt.
b. Khi tăng áp suất chung của hỗn hợp cân bằng hóa học của phản ứng sẽ chuyển dịch về chiều thuận vì sau phản ứng có sự giảm thể tích.
c. Khi tăng nồng độ khí oxi cân bằng hóa học của phản ứng sẽ chuyển dịch về phía thuận.
d. Khi giảm nồng độ khí sunfurơ cân bằng hóa học của phản ứng sẽ chuyển dịch về chiều nghịch.
7.13 Để thu được nhiều amoniac, hiệu quả kinh tế cao có thể dùng các biện pháp kĩ thuật sau đây:
- Tăng nồng độ N2 và H2.
- Tăng áp suất chung của hệ lên khoảng 100 atm, vì phản ứng thuận có sự giảm thể tích khí.
- Dùng nhiệt độ phản ứng thích hợp khoảng 400 -4500C và chất xúc tác để tăng tốc độ phản ứng tạo thành NH3. Chú ý rằng chất xúc tác không làm chuyển dịch cân bằng.
- Tận dụng nhiệt của phản ứng sinh ra đề sấy nóng hỗn hợp N2 và H2
- Tách NH3 ra khỏi hỗn hợp cân bằng và sử dụng lại N2 và H2 còn dư.
7.14 a. Khi tăng nhiệt độ cân bằng hóa học của phản ứng sẽ chuyển sang chiều nghịch. Bởi vì phản ứng thuận tỏa nhiệt.
b. Khi tăng áp suất chung cân bằng hóa học của phản ứng sẽ chuyển sang chiều thuận. Bởi vì sau phản ứng thuận có sự giảm thể tích khí.
c. Khi thêm khí trơ agon và giữ áp suât không đổi thì nồng độ của hai khí đều giảm, tuy nhiên tốc độ phản ứng thuận sẽ giảm nhanh hơn và do đó cân bằng hóa học của phản ứng sẽ chuyển sang chiều nghịch.
d. Khi thêm chất xúc tác không làm chuyển dịch cân bằng hóa học.
7.15 Để đánh giá tác động của áp suất cần so sánh sự biến đổi của thể tích khí trước và sau phản ứng. Nếu sau phản ứng có sự giảm thể tích thì áp suất tăng làm cân bằng chuyển dịch theo chiều thuận và ngược lại, áp suất không có ảnh hương tới cân bằng của các phản ứng không thay đổi thể tích khí.
a) 3O2(k) ![]() O3(k)
O3(k)
Phản ứng (a) có sự giảm thể tích, cân bằng chuyển theo chiều thuận khi áp suất tăng.
b) H2(k) + Br2(k) ![]() 2HBr(k)
2HBr(k)
Phản ứng (b) không có sự thay đổi thể tích, cân bằng không phụ thuộc vào áp suất.
c) N2O4(k) ![]() 2NO2(k)
2NO2(k)
Phản ứng (c) có sự tăng thể tích, cân bằng chuyển theo chiều nghịch khi áp suất tăng.
7.16 Các hoạt động của con người đang làm tăng hàm lượng CO2 trong khí quyển. Nhờ cân bằng này trong tự nhiên điều tiết, chuyển sang chiều thuận cho nên đã làm chậm quá trình nóng lên toàn cầu.
7.17 Đáp án B.
Tăng nhiệt độ của hệ làm cân bằng chuyển sang chiều thuận.
7.18 Nước clo dần dần bị mất màu theo thời gian, không bảo quản được lâu là do quá trình phân hủy HClO
Cl2(k) + H2O(l) ![]() HOCl + HCl (1)
HOCl + HCl (1)
2HClO ![]() 2HCl + O2 (2)
2HCl + O2 (2)
Phản ứng (2) làm cho [HClO] giảm, cân bằng hóa học của phản ứng (1) chuyển dịch theo chiều thuận, clo sẽ phản ứng với nước cho đến hết, do đó nước clo không bền.
7.19 Sản xuất vôi trong công nghiệp và thủ công đều dựa trên phản ứng hóa học:
CaCO3(r) ![]() CaO(r) + CO2(k), DH = 178kJ
CaO(r) + CO2(k), DH = 178kJ
a. Các đặc điểm của phản ứng hóa học nung vôi:
- Phản ứng thuận nghịch.
- Phản ứng thuận thu nhiệt.
- Phản ứng thuận của chất rắn có tạo ra một chất khí.
b. Những biện pháp kĩ thuật để nâng cao hiệu suất nung vôi:
- Chọn nhiệt độ thích hợp.
- Tăng diện tích tiếp xúc của chất rắn (CaCO3) bằng cách đập nhỏ đá vôi đến kích thước thích hợp.
- Thổi không khí nén (trong công nghiệp) hay chọn hướng gió thích hợp để tăng nồng độ khí oxi cung cấp cho phản ứng đốt cháy than, đồng thời làm giảm nồng độ khí cacbon đioxit.
7.20 A(x) + B(x) ![]() 2C(x) DH > 0
2C(x) DH > 0
- Phản ứng trên không có sự thay đổi về số mol khí trước và sau phản ứng, do đó áp suất không có ảnh hưởng đến sự chuyển dịch cân bằng.
- Phản ứng thuận thu nhiệt, do đó tăng nhiệt độ làm cân bằng chuyển sang chiều thuận.
- Tăng nồng độ các chất A và B hay giảm nồng độ C cũng làm chuyển dịch cân bằng sang chiều thuận.
7.21
a. So sánh các đặc điểm của hai phản ứng hóa học:
Phương trình hóa học | Giống nhau | Khác nhau |
C(r)+H2O (k) | Phản ứng thuận nghịch | - Phản ứng thuận thu nhiệt. - Sau phản ứng thuận tăng thể tích khí. |
2SO2(k)+O2(k) | Phản ứng thuận nghịch | - Phản ứng thuận tỏa nhiệt. - Sau phản ứng thuận giảm thể tích. - Cần chất xúc tác. |
b. Các biện pháp kĩ thuật để làm tăng hiệu suất sản xuất.
- Đối với phản ứng (1) : Tăng nhiệt độ, tăng nồng độ của hơi nước.
- Đối với phản ứng(2) : Nếu giảm nhiệt độ cân bằng chuyển sang chiều thuận, tuy nhiên ở nhiệt độ thấp tốc độ của phản ứng thấp làm cho quá trình sản xuất không kinh tế. Người ta chọn nhiệt độ thích hợp, dùng chất xúc tác V2O5 và tăng áp suất chung của phản ứng.
7. 22 Đặt x là số lần tăng của áp suất. Theo bài ra ta có ![]() = 64 = x3 Þ x = 4.
= 64 = x3 Þ x = 4.
7.23 Chọn đáp án C.
7.24 Đồ thị a biểu diễn sự biển đổi tốc độ phản ứng thuận theo thời gian.
 Đồ thị b biểu diễn sự biển đổi tốc độ phản ứng nghịch theo thời gian.
Đồ thị b biểu diễn sự biển đổi tốc độ phản ứng nghịch theo thời gian.
v v
a. b.
t(thời gian) t(thời gian)
Đồ thị c biểu diễn trạng thái cân bằng hóa học.
v
c,
t(thời gian)
7.25 Để loại bỏ Fe2+, trong một phương pháp đơn giản, rẻ tiền, nguời ta dùng oxi không khí oxi hóa Fe2+ thành hợp chất Fe3+ (có độ tan trong nước nhỏ) rồi lọc để thu nước sạch. Để tăng tốc độ của phản ứng oxi hóa Fe2+ người ta sử dụng giàn mưa. Nước ngầm sau khi hút lên bể chứa được qua giàn mưa với mục đích tăng diện tích tiếp xúc của nước với oxi không khí.
7.26 Nam cực là nơi lạnh nhất Trái đất. Nhiệt độ ở vùng này có thể xuống hàng chục độ dưới không. Ở nhiệt độ đó, các phản ứng hóa học phân hủy thức ăn hầu như không xảy ra. Điều này giải thích vì sao đã qua hàng trăm năm, nhưng các thức ăn trong những đồ hộp đó vẫn trong tình trạng tốt, có thể ăn được. Để giảm tốc độ phản ứng phân hủy thức ăn, người ta bảo quản thực phẩm bằng cách ướp đá hay dùng tủ lạnh.
7.27 Trong phòng thí nghiệm, để tăng tốc độ của một số phản ứng hóa học, ngoài các biện pháp như tăng nồng độ, nhiệt độ, sử dụng chất xúc tác..., người ta còn dùng máy khuấy. Máy khuấy là một thiết bị cho phép tăng tốc độ khuếch tán của các chất tham gia phản ứng, do đó tăng khả năng tiếp xúc của các chất và tăng tốc độ phản ứng hóa học. Người ta thường dùng máy khuấy trong trường hợp các chất phản ứng cần được trộn là các chất lỏng khác nhau, hay chất lỏng và chất rắn.
7.28 Dây thép được quấn thành hình lò xo để tăng bề mặt tiếp xúc của dây thép với oxi. Mẫu than nóng đỏ có tác dụng khơi mào phản ứng. Than cháy cung cấp nhiệt, nâng nhiệt độ của dây thép đến nhiệt độ cháy. Dây thép cháy trong oxi kèm theo hiện tượng tỏa nhiệt mạnh, các hạt sắt từ oxit (Fe3O4) nóng đỏ bắn tung tóe. Do đó, đáy bình cần có một lớp nước mỏng nhằm bảo vệ bình thủy tinh tránh bị nứt, vỡ.
7.29 Để điều khiển các phản ứng hóa học theo hướng có lợi nhất cho con người, trước hết cần biết rõ đặc điểm của phản ứng hóa học:
§ Phản ứng một chiều hay thuận nghịch?
§ Phản ứng thu hay tỏa nhiệt?
§ Phản ứng có sự tăng hay giảm thể tích khí?
§ Phản ứng cần chất xúc tác?
§ Phản ứng đồng thể (cùng trạng thái rắn, lỏng, khí) hay dị thể?
Căn cứ vào đặc điểm của phản ứng để tác động theo hướng tăng tốc độ phản ứng, chuyển dịch cân bằng theo chiều có lợi nhất.
7.30 Giải
Gọi V200 là tốc độ phản ứng ở 2000C
Vậy ở V210 = 2V200
V220 = 2V210 = 2.2V200 = 22.V200
V230 = 2V220 = 2.2V210 = 2 x 2 x 2V200 = 23.V200
V240 = 2V230 = 2.2V220 = 2 x 2 x2 V210 = .2.2.2.2V200 = 24.V200
Vậy tốc độ phản ứng tăng 24 = 16 lần.
F. THÔNG TIN BỔ SUNG
1. Liệu lượng oxi trên trái đất có hết không?
Hàng ngày, người, vật, cây cỏ... đều hút vào một lượng oxi và thải CO2. Hãy cứ lấy một người trưởng thành làm thí dụ, mỗi ngày anh ta thở ra trên dưới 400 lít CO2. Liệu lâu dài, có lúc nào đó lượng oxi trong không khí dùng hết và thế giới chỉ còn lại CO2 hay không?
Vào năm 1898, nhà vật lý học người Anh là Kenvin đã tỏ ra lo lắng: "Do sự phát triển của công nghiệp và dân số gia tăng, 500 năm sau, lượng oxi trên mặt đất sẽ bị sử dụng hết và loài người sẽ diệt vong?". Lúc đó, Kenvin đã chỉ xem xét vấn đề từ một phía: tiêu hao oxi và sản sinh CO2, nhưng còn phía khác là tiêu hao CO2 và sinh ra O2.
Nhà khoa học Thụy Sỹ Cheniba đã làm thí nghiệm sau: Cho lá cây xanh vào nước rồi để dưới ánh mặt trời. Không lâu sau, từ các lá cây thoát ra nhiều bóng khí nhỏ. Khi Cheniba dùng ống nghiệm nhỏ thu khí thoát ra rồi cho một que diêm đã tắt vào, que diêm bùng cháy mãnh liệt. Căn cứ vào đó ông cho rằng đó chính là oxi và chỉ có oxi mới duy trì sự cháy.
Sau đó Cheniba liền thổi khí CO2 vào nước. Ông nhận thấy, khi lượng CO2 thổi qua càng nhiều thì các bóng khí từ lá cây xanh thoát ra càng mạnh. Từ đó, Cheniba kết luận: "Dưới tác dụng của ánh sáng mặt trời, lá cây xanh hấp thụ CO2 và thải ra khí oxi".
Như vậy, đồng cỏ, rừng biển mênh mông có ẩn dấu một bí mật sau đây: "Dưới tác dụng của ánh sáng mặt trời, chất diệp lục của cây cỏ hấp thụ CO2 trong không khi, CO2 sẽ cùng với nước do rễ cây hút lên hóa hợp thành tinh bột, đường, đồng thời để thoát ra O2, người ta gọi quá trình này là quang hợp". Theo tính toán, cứ 3 cây lớn mỗi ngày hấp thụ vừa hết khí CO2 do người lớn thở ra. Mỗi năm, các loại cây xanh trên toàn thế giới hấp thụ đến hàng vạn tấn CO2.
Còn có một tác nhân khác khó thấy hơn, đó là đất đá. Chú ý đến cân bằng hóa học:
CaCO3 + H2O + CO2 ![]() Ca(HCO3)2
Ca(HCO3)2
Các loại đất đá bị gió mưa mài mòn, lâu ngày bị phong hóa như người ta thường nói: Nước chảy đá mòn. Như CaCO3 trong đá vôi dưới tác dụng của CO2 và nước sẽ hòa tan CaCO3, sau đó được nước mưa cuốn đi vào sông rồi ra biển. Dưới tác dụng của nhiệt lại tạo thành CaCO3 và lắng xuống đáy biển tạo thành lớp nham thạch mới. Hàng năm do sự phong hóa có thể tiêu tốn từ 40 đến 70 triệu tấn CO2. Người ta đã tính toán và thấy rằng khả năng điều chỉnh lượng CO2 trong khí quyển của biển và các đại dương là rất lớn, có thể lên đến hàng trăm triệu tấn CO2 trong một năm.
Như vậy, thế giới nhất định sẽ không biến thành một thế giới đầy CO2. Theo kết quả đo đạc của mấy trăm năm trở lại đây, hàm lượng CO2 trong bầu khí quyển có tăng lên, nhưng tăng chậm. Việc tăng hàm lượng CO2 là một nguy cơ làm cho Trái đất nóng lên, gây ra những biến đổi bất thường về khí hậu. Các kết quả quan sát cho biết trong 100 năm vừa qua, nhiệt độ trung bình của Trái Đất đã tăng 0,60C. Sắp tới lúc các cư dân Bắc Cực phải sử dụng tủ lạnh và điều hòa nhiệt độ, nếu như tình hình không được cải thiện.
Vì vậy nếu ta không chú ý coi trọng việc bảo vệ môi trường, hàm lượng CO2 trong khí quyển cao vượt quá giới hạn nhất định, điều đó sẽ tổn hại lớn cho con người. Những trận bão lớn gần đây như Katrina ở Mỹ, bão Sao Mai ở Trung Quôc là một sự cảnh báo nghiêm khắc của thiên nhiên đối với sự phá hủy môi trường của con người. Công ước Kyoto quy định duy trì mức thải CO2 ngang với năm 1997. Tuy nhiên để thực hiện được điều đó không phải dễ dàng, nguời ta ước tính chi phí cho nước Mỹ duy trì lượng CO2 thải ra khí quyển như 1997 là bằng khoảng 2% GDP năm, tức là trên 200 tỷ USD, điều này đồng nghĩa với việc phải đóng cửa nhiều nhà máy gây ô nhiễm, hàng loạt công nhân thất nghiệp, lợi nhuận của nhà đầu tư sụt giảm... . Đó chính là lí do lớn nhất mà nước Mỹ, cho đến thời điểm hiện tại (2006) vẫn chưa phê chuẩn công ước Kyoto.
2. Chất xúc tác là gì ?
1. Xúc tác
Chất xúc tác là những chất làm tăng tốc độ phản ứng hóa học, nhưng không bị tiêu hao sau phản ứng.
Có nhiều cách phân loại xúc tác, dựa trên các tiêu chí khác nhau.
Nếu dựa vào chức năng xúc tác, có thể chia xúc tác thành những loại sau:
- Xúc tác axit - bazơ.
- Xúc tác oxi hóa - khử
- Xúc tác lưỡng chức...
Còn nếu dựa vào trạng thái phân tán của xúc tác, có thể chia xúc tác thành
- Xúc tác đồng thể (chất phản ứng và chất xúc tác cùng pha)
- Xúc tác dị thể (chất phản ứng và chất xúc tác khác pha)
Các chất xúc tác trên thế giới có giá trị thương mại khoảng 5 tỷ USD/năm (1997), tạo ra một lượng hàng hóa khoảng 5000 tỷ USD, tức là bằng khoảng 1/2 tổng thu nhập quốc dân của nước giàu nhất thế giới là Hoa Kỳ.
2. Xúc tác - trong công nghiệp hóa học vô cơ
Trong công nghiệp Hóa học vô cơ có ba quy trình xúc tác được áp dụng ở quy mô lớn, đó là:
- Tổng hợp amoniac (NH3).
- Oxi hóa amoniac thành các oxit của nitơ để sản xuất axit nitric (HNO3).
- Oxi hóa khí sunfurơ thành anhiđric sunfuric để sản xuất axit sunfuric (H2SO4).
a. Tổng hợp amoniac (NH3).
N2 + 3H2 ![]() 2NH3; DH = - 92kJ
2NH3; DH = - 92kJ
Người ta tìm kiếm một chất xúc tác hoạt động tốt và ổn định để chuyển hệ đến trạng thái cân bằng ở nhiệt độ thấp nhất có thể. Trong khoảng những năm 1905 - 1910, các nhà hóa học như Haber, Bosch và Miltasch tại phòng thí nghiệm BASF đã có những cố gắng bền bỉ để tìm chất xúc tác thích hợp. Các kết quả nghiên cứu cho thấy một số kim loại có hoạt tính xúc tác như wonfam, urani, sắt, ruteni và osimi. Tuy nhiên độ bền của các chất xúc tác kể trên không cao. Sau nhiều năm nghiên cứu với các quặng sắt, người ta đã đạt được tiến bộ vượt bậc với một loại quặng sắt đến từ vùng Gallivare ở Thụy Điển. Phân tích thành phần của loại xúc tác này, thấy rằng có một ít oxit nhôm và oxit kali. Từ đó người ta cho rằng Al2O3 và K2O là những chất trợ xúc tác cho sắt. Bắt đầu từ năm 1914, loại xúc tác Fe/ Al2O3 và K2O được sử dụng ở quy mô lớn ở nước Đức. Loại xúc tác này cho đến nay vẫn còn được sử dụng.
b. Oxi hóa amoniac
4NH3 + 5O2 ® 4NO + 6H2O
Bằng phát minh đầu tiên về xúc tác cho phản ứng oxi hóa NH3 là do Kuhlman năm 1938. Chất xúc tác được sử dụng là muội bạch kim (Pt). ứng dụng công nghiệp đầu tiên của xúc tác này phải chờ đến khi người ta sản xuất được amoniac có độ sạch cao. Để bảo vệ xúc tác ở nhiệt độ cao, người ta đã sử dụng hợp kim của Pt với 10% Rh, vật liệu này tốt hơn nhiều so với Pt nguyên chất. Người ta dệt xúc tác thành lưới, đường kính sợi là 0,06mm, với 1050 lỗ /cm2.
c. Xúc tác oxi hóa lưu huỳnh đioxit.
2SO2 + O2 ® 2SO3
Phản ứng oxi hóa SO2 là một công đoạn trong quá trình sản xuất axit H2SO4. Trước đây người ta dùng xúc tác Pt trên chất mang. Tuy nhiên loại xúc tác này rất dễ bị ngộ độc bởi các hợp chất của asen. Ngày nay, xúc tác cho phản ứng oxi hóa SO2 được điều chế bằng cách làm nóng chảy V2O5 trong oxit của kim loại kiềm.
Mục lục
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP.. 16
F. MỘT SỐ THÔNG TIN BỔ SUNG.. 26
BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC.. 28
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP.. 43
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP.. 78
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP.. 123
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP.. 149
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP.. 180
TỐC ĐỘ PHẢN ỨNG VÀ CÂN BẰNG HÓA HỌC.. 198
E. ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI BÀI TẬP.. 220


































































































































 Trang Trước
Trang Trước



No comments: