ĐỀ CƯƠNG ÔN TẬP KIỂM TRA HỌC KÌ 1 Hóa 10 CB
ĐỀ CƯƠNG ÔN TẬP KIỂM TRA HỌC KÌ 1
MÔN: HÓA HỌC KHỐI 10 - CB
NĂM HỌC: 2012 - 2013
I. TRẮC NGHIỆM
Chương I
Hãy chọn đáp án đúng A, B, C hoặc D.
1. Các hạt cấu tạo nên hạt nhân của hầu hết các nguyên tử là
A. electron và proton. B. proton và nơtron. C. nơtron và electron. D. electron, proton và nơtron.
2. Các hạt cấu tạo nên hầu hết các nguyên tử là
A. electron và proton. B. proton và nơtron. C. nơtron và electron. D. electron, proton và nơtron.
3. Nguyên tố hóa học là những nguyên tử có cùng
A. số khối. B. số nơtron. C. số proton. D. số proton và số nơtron.
4. Kí hiệu nguyên tử  cho ta biết những gì về nguyên tố hóa học X?
cho ta biết những gì về nguyên tố hóa học X?
A. Nguyên tử khối của nguyên tử. B. Chỉ biết số hiệu nguyên tử.
C. Chỉ biết số khối của nguyên tử. D. Số hiệu nguyên tử và số khối.
5. Nguyên tố kali có 3 đồng vị bền  chiếm 93,258%;
chiếm 93,258%;  chiếm 0,012% và
chiếm 0,012% và  chiếm 6,730%. Nguyên tử khối trung bình của nguyên tố kali là
chiếm 6,730%. Nguyên tử khối trung bình của nguyên tố kali là
A. 39,31. B. 39,13. C. 39,34. D. 39,43.
6. Nguyên tử nhôm được kí hiệu  .Tổng số hạt proton, nơtron và electron của nguyên tử nhôm lần lượt là
.Tổng số hạt proton, nơtron và electron của nguyên tử nhôm lần lượt là
A. 13, 13, 14. B. 14, 14, 13. C. 13, 14, 13. D. 13, 27, 13.
7. Nguyên tử natri được kí hiệu  . Tổng số hạt cấu tạo nên nguyên tử natri là
. Tổng số hạt cấu tạo nên nguyên tử natri là
A. 23. B. 11. C. 12. D. 34.
8. Nguyên tử magiê có 12 electron, 12 proton, 12 nơtron. Khối lượng của nguyên tử magiê (u) là
A. 24,0066 u. B. 24,0606 u. C. 24,0660 u. D. 24,6600 u.
9. Đồng có hai đồng vị bền  và
và  . Nguyên tử khối trung bình của đồng là 63,54. Thành phần phần trăm số nguyên tử của
. Nguyên tử khối trung bình của đồng là 63,54. Thành phần phần trăm số nguyên tử của  ,
,  lần lượt là
lần lượt là
A. 73%, 27%. B. 27%, 73%. C. 37%, 63%. D. 63%, 37%.
10. Photpho có Z = 15 và N = 16. Nguyên tử khối của photpho là
A. 15. B. 16. C. 31. D. 13.
11. Lớp electron có mức năng lượng nhỏ nhất là
A. lớp L. B. lớp K. C. lớp M. D. lớp N.
12. Các electron trên cùng một phân lớp có mức năng lượng
A. bằng nhau. B. gần bằng nhau.
C. khác nhau rất nhiều. D. không xác định được.
A. 1. B. 2. C. 3. D. 4.
14. Số đơn vị điện tích hạt nhân của natri là 11. Trong nguyên tử natri số electron ở phân mức năng lượng cao nhất là
A. 1. B. 2. C. 3. D. 4.
15. Các electron của nguyên tố X được phân bố trên 2 lớp, lớp thứ 2 có 7 electron. Số hiệu nguyên tử của nguyên tố X là
A. 7. B. 8. C. 9. D.10.
16. Nguyên tố có Z = 29 thuộc loại nguyên tố A. s. B. p. C. d. D. f.
17. Cấu hình electron của nguyên tử Fe (Z = 26) là
A. 1s22s22p63s23p64s23d6. B. 1s22s22p63s23p6 3d64s2. C. 1s22s22p63s23p64s23d5. D. 1s22s22p63s23p6 3d54s2.
18. Tổng các hạt cơ bản (p, n, e) của một nguyên tử X là 28. Số hạt mang điện nhiều hơn số hạt không mang điện là 8. Kí hiệu nguyên tử X là
19. Cho biết cấu hình electron của nguyên tố A là 1s22s22p63s23p1 và cấu hình electron của nguyên tố B là 1s22s22p4. Phát biểu đúng là
A. Nguyên tố A là phi kim, nguyên tố B là kim loại.
B. Nguyên tố A là kim loại, nguyên tố B là phi kim.
C. Nguyên tố A, nguyên tố B đều là phi kim.
D. Nguyên tố A, nguyên tố B đều là kim loại.
20. Các ion và nguyên tử Ne, Na+, F- có
A. số khối bằng nhau. B. số electron bằng nhau.
C. số proton bằng nhau. D. số nơtron bằng nhau.
21. Số electron tối đa trên phân lớp s, p, d, f lần lượt là
A. 2, 10, 6, 14. B. 2, 6, 14, 10. C. 2, 6, 10, 14. D. 6, 2, 10, 14.
22. Số electron tối đa của lớp thứ n là
A. n2. B. 2n2. C. 2n. D. 3n2.
23. Nguyên tố có cấu hình: 1s22s22p63s23p5 thuộc loại nguyên tố
A. s. B. p. C. d. D. f.
24. Cấu hình electron của nguyên tử Flo (Z = 9) là
A. 1s22s22p6. B. 1s22s22p5. C. 1s22s62p2. D. 1s22s22p7.
25. Nhôm có cấu hình electron nguyên tử 1s22s22p63s23p1. Số electron lớp ngoài cùng của nhôm là
A. 1. B. 2. C. 3. D. 4.
26. Cấu hình electron của các nguyên tử có số hiệu Z=3, Z=11 và Z=19 có đặc điểm chung là:
A. có 1 electron lớp ngoài cùng. B. có 2 electron lớp ngoài cùng. C. có 3 electron lớp ngoài cùng. D. đáp án khác.
27. Một nguyên tử R có tổng số hạt mang điện và không mang điện là 34. Trong đó có số hạt mang điện nhiều hơn số hạt không mang điện là 1,833 lần. nguyên tố R là:
28. Nguyên tố natri có điện tích hạt nhân là 11+. Số hiệu nguyên tử, tổng số proton, tổng số electron lần lượt là
A. 11, 12, 13. B. 11, 13, 12. C. 11, 11, 11. D. 13, 12, 11.
29. Các electron trên cùng một lớp có mức năng lượng
A. bằng nhau. B. gần bằng nhau. C. khác nhau rất nhiều. D. không xác định được.
30. Tổng các hạt cơ bản trong nguyên tửX (proton,nơtron và electron) là 58. Biết các hạt mang điện gấp các hạt không mang điện là 1,8 lần. Tìm số khối của X?
A. 19 B. 39 C. 58 D. 38.
31. Các đồng vị của cùng một nguyên tố hóa học là những nguyên tử có
A. cùng số proton, cùng số electron. B. cùng số proton, cùng số hiệu nguyên tử.
C. cùng số proton, khác số nơtron. D. cùng số nơtron, khác số proton.
32. Nguyên tố cacbon có 2 đồng vị bền  chiếm 98,89% và
chiếm 98,89% và  chiếm 1,11%. Nguyên tử khối trung bình của nguyên tố cacbon là
chiếm 1,11%. Nguyên tử khối trung bình của nguyên tố cacbon là
A. 12,500. B. 12,022. C. 12,011. D. 12,055.
33. Nguyên tố X có cấu hình electron: 1s22s22p63s2. Số electron lớp ngoài cùng của nguyên tố X là
A. 1. B. 2. C. 3. D. 4.
34. Cacbon có 2 đồng vị 12C và 13C, Oxi có 3 đồng vị là16O, 17O và 18O. Có bao nhiêu công thức phân tử Cacbon monooxit (CO) khác nhau?
A. 2. B. 6. C. 3. D. 8.
35. Số đơn vị điện tích hạt nhân của magiê là 12. Trong nguyên tử magiê số electron ở phân mức năng lượng cao nhất là
A. 1. B. 2. C. 3. D. 4.
36. Cấu hình electron nguyên tử của oxi (Z = 8) là
A. 1s22s22p6. B. 1s22s22p4. C. 1s22s62p2. D. 1s22s22p7.
37. Ion có 18 electron và 16 proton, mang điện tích là
A. 18+. B. 2-. C. 18-. D. 2+.
38. Nguyên tử magiê được kí hiệu  . Tổng số hạt cấu tạo nên nguyên tử magiê là
. Tổng số hạt cấu tạo nên nguyên tử magiê là
A. 24. B. 11. C. 12. D. 34.
39. Nguyên tử X không có nơtron trong hạt nhân nguyên tử là
40. Ion có 16 electron và 18 proton, mang điện tích là
A. 18+. B. 2-. C. 18-. D. 2+.
41. Nguyên tố clo có 2 đồng vị bền  chiếm 75,77% và 37Cl chiếm 24,23%. Nguyên tử khối trung bình của nguyên tố cacbon là
chiếm 75,77% và 37Cl chiếm 24,23%. Nguyên tử khối trung bình của nguyên tố cacbon là
A. 53,5. B. 35,5. C. 55,3. D. 35,7.
42. Clo có 2 đồng vị bền 35Cl và 37Cl, Hidro có 2 đồng vị bền la ø1H và 2H. Có bao nhiêu công thức phân tử HCl khác nhau?
A. 5. B. 2. C. 3. D. 4.
43. Ba nguyên tử X, Y, Z có số proton và số nơtron như sau:
X: 20 proton và 20 nơtron; Y: 18 proton và 22 nơtron; Z: 20 proton và 22 nơtron
Những nguyên tử là các đồng vị của cùng một nguyên tố là:
A. X, Y. B. X, Z. C. Y, Z. D. Không có nguyên tử nào.
44. Ba nguyên tử X, Y, Z có số proton và số nơtron như sau:
X: 20 proton và 20 nơtron; Y: 18 proton và 22 nơtron; Z: 20 proton và 22 nơtron
Những nguyên tử có cùng số khối là:
A. X, Y. B. X, Z. C. Y, Z. D. Không có nguyên tử nào.
45.Điều nhận định nào sau đây không đúng
A. Nguyên tử có cấu tạo rỗng, hạt nhân mang điện tích dương có kích thước rất nhỏ so với kích thước của nguyên tử và nằm ở tâm của nguyên tử.
B. Khối lượng của nguyên tử tập trung hầu hết ở hạt nhân nguyên tử, khối lượng của electron không đáng kể so với khối lượng của nguyên tử.
C. Tổng trị số điện tích âm của các electron trong lớp vỏ nguyên tử bằng tổng trị số điện tích dương của các prôton trong hạt nhân nguyên tử.
D. Khối lượng tuyệt đối của nguyên tử bằng tổng khối lượng của prôton và nơtron..
46. Số prôtôn, nơtron và electron của  lần lượt là:
lần lượt là:
A. 19, 20, 39. B. 20, 19, 39 C. 19, 20, 19. D. 19,19,20.
47. Tổng số hạt (p, n, e) trong  là:
là:
A. 19. B. 28. C. 30. D. 32.
48. Tổng số hạt n, p, e trong  là:
là:
A. 52 B. 35 C. 53 D. 51
49. Tổng số hạt p, n, e trong  lần lượt là:
lần lượt là:
A. 24,28,24. B. 24,28,21. C. 24,30,21. D. 24,28,27.
50. Nguyên tử X có tổng số hạt là 60. Trong đó số hạt n bằng số hạt p. X là:
51. Đồng vị  và
và  kết hợp tạo phân tử SO2. Tổng số hạt trong p.tử SO2 là
kết hợp tạo phân tử SO2. Tổng số hạt trong p.tử SO2 là
A. 83 B. 66 C. 98 D. 32.
52. Nguyên tử có kí hiệu là:  Vậy nguyên tử đó thuộc nguyên tố.
Vậy nguyên tử đó thuộc nguyên tố.
A. Bari B. Nhôm C. Na D. Kali.
53. Nguyên tử nào sau đây có sự khác biệt về cấu tạo nguyên tử so với các nguyên tử còn lại. .
.
54. Tổng số hạt prôtôn, nơtron và electron trong nguyên tử A là 40. Số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt. Vậy A là:
A. Cu B. Ag C. Fe D. Al.
55. Dãy gồm các phân lớp electron đã bão hòa là
A. s2; p6; d5; f14. B. s2; p6; d10; f14. C. s1; p5; d5; f7. D. s2; p6; d10; f7.
56. Cho 5 nguyên tử  . Cặp nguyên tử nào là đồng vị.
. Cặp nguyên tử nào là đồng vị.
A. (C, D) B. ( C, E) C. ( A,B) D. (B,C).
57. Nguyên tử nào sau đây có 3 electron thuộc lớp ngoài cùng:
A. Na B. N C. Al D. C
58. Ion nào sau đây không có cấu hình của khí hiếm:
A. Ca2+ B. Cl- D. K+ D. Fe2+.
59. Nguyên tử Ca có cấu hình electron đúng như sau:
A. 1s22s22p63s23p64s2 B. 1s22s22p63s23p63d2 C. 1s22s22p53s23p64s2. D. 1s22p63s23p63d24s2.
60. Cấu hình e của 4 nguyên tố: (X: 1s22s22p5 ); ( Y : 1s22s22p63s1 ); ( Z: 1s22s22p63s23p1 ); ( T: 1s22s22p4).
Ion của 4 nguyên tố trên là:
A. X+, Y+, Z+, T2+. B. X-, Y2+, Z3+, T+ C. X-, Y+, Z3+, T2-. D. X+, Y2+, Z3+, T-.
61. Xét ba nguyên tố X ( Z =2); Y ( Z =16), T ( Z =19).
A. X và T là kim loại, Y là phi kim. C. X là khí hiếm, Y là phi kim, T là kim loại.
B. X, Y là khí hiếm, T là kim loại. D. Tất cả đều sai.
62. Nguyên tử oxi có 8 electron, 8 proton, 8 nơtron. Khối lượng của nguyên tử oxi (u) là
. A. 16,0404 u. B. 16,4400 u. C. 16,4040 u. D. 16,0044 u.
63. Cấu hình electron của Fe3+ nào sau đây là đúng:
A. 1s22s22p63s23p63d5. B. 1s22s22p63s23p63d34s2 C.1s22s22p63s23p6 D. 1s22s22p53s23p63d34s2
64. Ion A2+ có tổng số hạt là 34. Trong đó số hạt không mang điện là 12. Vậy số khối của A là:
A. 46 B. 23 C. 24 D. 2
65. Cấu hình electron nào sau đây là đúng:
A. 1s22s22d63s2 B. 1s22s22p63p63d44s2 C. 1s22s22p63s23p63d104s1 D. 1s22s22p63s23d54s1
66. Dãy gồm các lớp electron đã bão hòa là
A.Lớp K: 2e, lớp L: 6e, lớp M: 18e, lớp N: 32e. B. Lớp K: 2e, lớp L: 8e, lớp M: 18e, lớp N: 32e.
C. Lớp K: 2e, lớp L: 6e, lớp M: 8e, lớp N: 18e. D. Lớp K: 2e, lớp L: 6e, lớp M: 8e, lớp N: 32e.
67. Nguyên tử của nguyên tố nào sau đây chứa đồng thời 20n, 19e, 19p.
68. Clo có 2 đồng vị bền 35Cl và 37Cl. Có bao nhiêu công thức phân tử Clo (Cl2) khác nhau?
A. 5. B. 2. C. 3. D. 4.
69. Một nguyên tử X có tổng số electron ở các phân lớp p là 11. Vậy X thuộc loại:
A. nguyên tố s. B. nguyên tố p. C. nguyên tố d. D. nguyên tố f.
70.Nguyên tử của nguyên tố có tổng số hạt là 40 trong đó số hạt mang điện nhiều hơn số hat không mang điện là 12. vậy số khối của nguyên tử đó là:
A. 27 B. 26 C.28 D. Kết quả khác.
71. Ion M3+ có số electron ở lớp vỏ ngoài cùng là 13. Nguyên tố M là:
A. Al B. Fe C. Na D. Cr
72. Nguyên tử A có cấu hình electron là 1s22s22p63s23p3. Ion A3- có cấu hình electron là:
A. 1s22s22p63s23p64s2 C. 1s22s22p63s23p5
B. 1s22s22p63s23p6 D. 1s22s22p63s23p1
73. Cho các nguyên tố có cấu hình electron nguyên tử của các nguyên tố như sau :
X ( 1s22s22p63s2); Y ( 1s22s22p63s23p63d54s2); Z ( 1s22s22p63s23p5); T( 1s22s22p6).
Các nguyên tố là kim loại nằm ở tập hợp nào sau đây:
A. X, Y, T. B. X, Y C. Z, T D. Y, Z, T.
74. Cấu hình electron của các nguyên tử có số hiệu Z=3, Z=11 và Z=19 có đặc điểm chung là:
A. có 1 electron lớp ngoài cùng. B. có 2 electron lớp ngoài cùng.
C. có 3 electron lớp ngoài cùng. D. đáp án khác.
75. Cấu hình electron của Fe2+ :
A. 1s22s22p63s23p63d6 C. 1s22s22p63s23p63d54s2
B. 1s22s22p63s23p64s2 D. 1s22s22p63s23p63d5.
76. Oxi có 3 đồng vị khác nhau, Cacbon có hai đồng vị khác nhau: có bao nhiêu phân tử CO2 được tạo thành :
A. 11 B.12 C.13 D.14
77. Cấu hình electron của Cu ở trạng thái cơ bản:
- 1s22s22p63s23p63d94s2 C. 1s22s22p63s23p64s23d9
B. 1s22s22p63s23p63d104s1 D. 1s22s22p63s23p64s13d10.
78. A+ và B- đều có cấu hình electron giống nhau là 1s22s22p6.
A. A là Cl , B là K B. A là K, B là Clo
C. A là Na, B là F D. A là F, B là Na
79. Số hiệu nguyên tử nào sau không đúng với nguyên tố hóa học.
A. ( Na : Z =11). B. ( Cr : Z =24 ). C. ( Ti : Z = 23) D. (Cl : Z =17)
80. Hiđrô có 3 đồng vị  , Cacbon có 2 đồng vị.
, Cacbon có 2 đồng vị.  và
và  . Hỏi có bao nhiêu phân tử C2H2 được tạo nên từ các loại đồng vị đó:
. Hỏi có bao nhiêu phân tử C2H2 được tạo nên từ các loại đồng vị đó:
A. 6 B. 12 C. 9 D. 18.
81. Tổng số hạt prôtôn, nơtron và electron trong nguyên tử A là 82. Số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt. Vậy A là:
A. Cu B. Ag C. Fe D. Al.
82. Tổng số hạt prôtôn, nơtron và electron trong nguyên tử A là 93. Số hạt mang điện nhiều hơn số hạt không mang điện là 23 hạt. Vậy A là:
A. Cu B. Ag C. Fe D. Al.
83. Tổng số hạy proton,nơtron và electron trong nguyên tử của một nguyên tố là 40. Biết số hạt nơtron nhiều hơn số hạt proton là 1. Cho biết nguyên tố trên thuộc loại nguyên tố nào?
A. Nguyên tố s. B. Nguyên tố p. C Nguyên tố d. D. Nguyên tố f.
84. Nguyên tử khối của Brôm là 79,91. Brôm có hai đồng vị  và
và  .
.
(1). Tính % của mỗi loại đồng vị trong tự nhiên lần lượt là: ……………………………………
(2). % khối lượng của mỗi loại đồng vị trong tự nhiên lần lượt là: ……………………………………………
85. Một nguyên tử X có tổng số hạt electron ở các phân lớp s là 6 và tổng số electron lớp ngoài cùng là 6. Cho biết X thuộc về nguyên tố hóa học nào?
A. oxi(Z=8) B. Lưu huỳnh(Z=16) C. Flo(Z=9) D. Clo(Z=17)
86. A+ và B- đều có cấu hình electron giống nhau là 1s22s22p63s23p6.
A. A là Cl , B là K B. A là K, B là Clo
C. A là Na, B là F D. A là F, B là Na
87. Nguyên tử là phần tử nhỏ nhất của chất
A. không mang điện. C. mang điện tích dương.
B. mang điện tích âm. D. Có thể mang điện hoặc không mang điện.
88. Số đơn vị điện tích hạt nhân của clo là 17. Trong nguyên tử clo số electron ở phân mức năng lượng cao nhất là
A. 1. B. 2. C. 3. D. 4.
89. Số electron tối đa trên phân lớp s, p, d, f lần lượt là
A. 2, 10, 6, 14. B. 2, 6, 14, 10. C. 2, 6, 10, 14. D. 6, 2, 10, 14.
90. Cho 2 đồng vị 1H và 2H, có bao nhiêu công thức phân tử hidro khác nhau?
A. 1. B. 2. C. 3. D. 4.
91. Cấu hình electron nào sau đây có tính kim loại ?
A. 1s2 B. 1s22s22p63s23p63d54s2 C. 1s22s22p63s23p3 D. 1s22s22p5.
92. Tổng số hạt cơ bản (proton, nơtron, electron) của một nguyên tử X là 26. Số hạt mang điện nhiều hơn số hạt không mang điện là 6. nguyên tử X là:
93. Khi nói về số khối, điều khẳng định nào sau đây luôn đúng.
A. Trong nguyên tử, số khối bằng tổng khối lượng các hạt proton và nơtron.
B. Trong nguyên tử, số khối bằng tổng số lượng các hạt proton và nơtron.
C. Trong nguyên tử, số khối bằng nguyên tử khối.
D. Trong nguyên tử, số khối bằng các hạt proton, nơtron, và electron.
94. Khi nói về mức năng lượng của các electron trong nguyên tử, điều nào sau đây là sai?
A. Các electron ở lớp K có mức năng lượng thấp nhất.
B. Các electron ở lớp ngoài cùng có mức năng lượng trung bình cao nhất.
C. Các electron ở lớp K có mức năng lượng cao nhất.
D. Các electron trong cùng lớp K có mức năng lượng bằng nhau.
95. Fe (Z = 26) thuộc loại nguyên tố
A. s. B. p. C. d. D. f.
96. Cho biết cấu hình electron của nguyên tố A là 1s22s22p63s23p4 và cấu hình electron của nguyên tố B là 1s22s22p63s1. Phát biểu đúng là
A. Nguyên tố A là phi kim, nguyên tố B là kim loại.
B. Nguyên tố A là kim loại, nguyên tố B là phi kim.
C. Nguyên tố A, nguyên tố B đều là phi kim.
D. Nguyên tố A, nguyên tố B đều là kim loại.
97. Nguyên tử natri có 11 proton, 11 electron, 12 nơtron. Khối lượng của nguyên tử natri (u) là
A. 23,00605 u. B. 23,00506 u. C. 23, 00065 u. D. 23,00056 u.
98. Ion  có tổng số hạt cơ bản là 53, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 17. Số electron phân lớp s là: A. 2 B. 6 C. 4 D. 5
có tổng số hạt cơ bản là 53, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 17. Số electron phân lớp s là: A. 2 B. 6 C. 4 D. 5
99. Trong các câu sau đây câu nào sai?
A. Số electron ở phần vỏ bằng số proton ở hạt nhân.
B. Hạt nhân có kích thước rất nhỏ bé so với nguyên tử.
C. Số khối A = Z + N.
D. Nguyên tử khối bằng số nơtron trong hạt nhân.
100. Một nguyên tử X có 15 electron trong lớp vỏ. Vậy cấu hình electron của X có bao nhiêu lớp?
A. 2 B. 3 C. 4 D. 5
Chương II
1. Các nguyên tố được sắp xếp trong bảng tuần hoàn theo nguyên tắc:
A. Các nguyên tố được sắp xếp theo chiều tăng dần của nguyên tử khối trung bình các nguyên tử.
B. Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một cột.
C. Các nguyên tố có electron hoá trị trong nguyên tử như nhau được xếp thành một hàng.
D. Các nguyên tố được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
2. Số nguyên tố trong chu kì 3 và 4 bằng:
A. 8, 32 B. 8, 18 C. 8, 16. D. 2, 8.
3. Các nguyên tố ở chu kì 3 và 5 có số lớp electron trong nguyên tử là:
A. 3, 6. B. 3, 7. C. 4, 8. D. 3, 5.
4. Các nguyên tố Li, Na, K, Be được sắp xếp theo chiều tính kim loại yếu dần là
A. Be> K>Na>Li; B. K>Na>Li>Be C. Be>Na>Li>K; D. Li>Be>Na>K
(Cho Z của Be =4, Li =3, Na =11,K =19)
5. Kết luận nào sau đây luôn đúng ?
A. Nguyên tử của nguyên tố Y có phân mức năng lượng cao nhất là 3d7, vậy Y ở nhóm VIIB.
B. Nguyên tử của nguyên tố Z có 3 electron lớp ngoài cùng nên Z ở nhóm IIIA.
C. Nguyên tử của nguyên tố T có 1 electron lớp ngoài cùng nên T là kim loại.
D. Nguyên tử của nguyên tố X có lớp electron ngoài cùng là 4s2, vậy điện tích hạt nhân của X là 20.
6. Trong cùng 1 chu kì, theo chiều tăng của điện tích hạt nhân
A. tính kim loại tăng. B. tính axit của các oxit và hiđroxit tăng.
C. tính phi kim giảm dần. D. tính axit của các oxit và hiđroxit giảm.
7. Nguyên tử của một nguyên tố có bốn lớp electron, theo thứ tự từ gần hạt nhân ra ngoài: K, L, M, N. Electron thuộc lớp nào sau đây có mức năng lượng trung bình cao nhất là?
A. Lớp K. B. Lớp M. C. Lớp L. D. Lớp N.
8. Các nguyên tử và ion Ca2+, Cl-, Ar có đặc điểm chung là
A. cùng một chu kì. B. cùng một nhóm.
C. cùng số electron. D. cùng số proton.
9. Nguyên tử của nguyên tố nào trong các nguyên tố sau luôn nhường 2 electron trong các phản ứng hóa học
A. Na (Z = 11). B. Mg (Z = 12). C. Al (Z = 13). D. Si ( Z = 14).
10. Các nguyên tử trong cùng một nhóm A thì có cùng
A. số electron ngoài cùng. B. số lớp electron.
C. số electron. D. số proton.
11. Dãy nguyên tố sắp xếp theo chiều giảm dần tính kim loại và tăng dần tính phi kim là
A. Al, Mg, Br, Cl. B. Na, Mg, Si, Cl.
C. Mg, K, S, Br. D. N, O, Cl, Ne.
12. Trong nguyên tử , ở trạng thái cơ bản, mỗi electron có
A. một mức năng lượng nhất định. B. một mức năng lượng thay đổi.
C. nhiều mức năng lượng nhất định. D. nhiều mức năng lượng thay đổi.
13. Nguyên tử của nguyên tố X có cấu hình electron của phân lớp ngoài cùng là 3p3. Vị trí của X trong bảng tuần hoàn là
A. chu kì 3, nhóm IIIA. B. chu kì 3, nhóm IVA. C. chu kì 3, nhóm VA. D. chu kì 6, nhóm IIIA.
14. Nguyên tử của hai nguyên tố X và Y đứng kế nhau trong một chu kỳ có tổng số hạt proton là 25. X và Y thuộc chu kỳ và các nhóm nào sau đây ?
A. Chu kỳ 2, nhóm IIIA, IVA. B. Chu kỳ 2, nhóm IIA, IIIA C. Chu kỳ 3, nhóm IIA, IIIA D. Chu kỳ 3, nhóm IA, IIA.
15. Theo chiều tăng của điện tích hạt nhân, tính chất bazơ của hiđroxit tương ứng với nguyên tố trong nhóm VIA
A. tăng. B. giảm. C. không đổi. D. giảm rồi tăng.
16. Số hiệu nguyên tử của các nguyên tố trong bảng tuần hoàn cho biết
A. số electron hóa trị. B. số proton trong hạt nhân.
C. số nơtron trong hạt nhân. D. số khối của hạt nhân.
17. Trong 20 nguyên tố đầu của bảng tuần hoàn, số nguyên tố có 2 electron hóa trị ở trạng thái cơ bản là
A. 1. B. 3. C. 2. D. 4.
18. Hoà tan hoàn toàn 2,4 gam hỗn hợp hai kim loại X, Y thuộc nhóm II A và thuộc hai chu kì liên tiếp bằng dung dịch HCl thu được 4,48 lít H2 (đktc). Hai kim loại X, Y là :
A. Ca (M = 40) và Sr (M = 88) B. Sr (M = 88) và Ba (M = 137)
C. Be (M = 9) và Mg (M = 24) D. Mg (M = 24) và Ca (M = 40)
19. Hoà tan 2,4 g kim loại Mg trong dung dịch HCl dư, khối lượng muối MgCl2 thu được là
A. 9,5 g. B. 5,9 g. C. 9,4 g. D. 4,9 g.
20. Biết cấu hình electron của các nguyên tố A, B, C, D, E như sau: A: 1s22s22p63s23p64s1; B: 1s22s22p63s1; C: 1s22s22p63s23p4; D: 1s22s22p4; E: 1s22s22p5.Thứ tự tăng dần tính phi kim của các nguyên tố là:
A. A, B, C, D, E B. A, B, E, C, D C. B, A, C, D, E. D. Kết quả khác.
21. Trong một nhóm A, bán kính nguyên tử các nguyên tố
A. tăng theo chiều tăng của điện tích hạt nhân.
B. giảm theo chiều tăng của điện tích hạt nhân.
C. giảm theo chiều giảm của tính kim loại.
D. cả A và C đều đúng.
22. Một nguyên tố R có công thức oxit cao nhất dạng RO2. Công thức hợp chất khí với H của R có dạng
A. RH4. B. RH3. C. RH2. D. RH.
23. Nguyên tử của nguyên tố X có cấu hình electron: 1s22s22p63s23p64s1. Hãy chọn phát biểu đúng:
A. X ở ô thứ 19, chu kì 4, nhóm VIIA.
B. X ở ô thứ 20, chu kì 3, nhóm IA.
C. X ở ô thứ 19, chu kì 4, nhóm IA.
D. X ở ô thứ 20, chu kì 4, nhóm VIIA.
24. Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần độ âm điện của nguyên tử?
A. Li, F, N, Na, C. B. N, F, Li, C, Na.
C. F, Li, Na, C, N. D. Na, Li, C, N, F.
(Cho Z của Li=3, C=6, N=7, F=9, Na=11)
25. Trong một nhóm A, theo chiều tăng của điện tích hạt nhân nguyên tử:
A. Tính kim loại của các nguyên tố giảm dần, tính phi kim của các nguyên tố tăng dần, độ âm điện tăng dần.
B. Tính kim loại của các nguyên tố tăng dần, tính phi kim của các nguyên tố giảm dần, độ âm điện tăng dần.
C. Tính kim loại của các nguyên tố tăng dần, tính phi kim của các nguyên tố giảm dần, độ âm điện giảm dần.
D. Tính kim loại và tính phi kim của các nguyên tố không thay đổi, độ âm điện giảm dần.
26. Ngyên tử các nguyên tố kim loại có tính đặc trưng là:
A. Nhường electron tạo thành ion âm.
B. Nhận electron tạo thành ion dương.
C. Nhận electron tạo thành ion âm.
D. Nhường electron tạo thành ion dương.
27. Nhóm nguyên tố nào mà hợp chất oxit cao nhất ứng với công thức chung là X2O3?
A. Nhóm IA. B. Nhóm IIA . C. Nhóm IIIA. D. Nhóm VIA.
28. Trong một chu kì, theo chiều tăng của điện tích hạt nhân nguyên tử
A. Tính kim loại của các nguyên tố giảm dần, tính phi kim của các nguyên tố tăng dần, độ âm điện tăng dần.
B. Tính kim loại của các nguyên tố tăng dần, tính phi kim của các nguyên tố giảm dần, độ âm điện tăng dần.
C. Tính kim loại của các nguyên tố tăng dần, tính phi kim của các nguyên tố giảm dần, độ âm điện giảm dần.
D. Tính kim loại và tính phi kim của các nguyên tố không thay đổi, độ âm điện giảm dần.
29. Độ âm điện đặc trưng cho khả năng
A. hút electron của nguyên tử trong phân tử.
B. nhường electron của nguyên tử cho nguyên tử khác.
C. tham gia phản ứng mạnh hay yếu.
D. nhường proton của nguyên tử cho nguyên tử khác.
30. Theo quy luật biến đổi tính chất các nguyên tố trong bảng tuần hoàn thì:
A. phi kim mạnh nhất là Iot. B. kim loại mạnh nhất là Liti.
C. phi kim yếu nhất là Flo. D. kim loại yếu nhất là Xesi.
31. Các nguyên tố xếp ở chu kỳ 6 có số lớp electron trong nguyên tử là:
A. 3. B. 5. C. 6. D. 7.
32. Số chu kỳ nhỏ và số chu kỳ lớn trong bảng hệ thống tuần hoàn là
A. 3 và 3. B. 3 và 4. C. 4 và 4. D. 4 và 3.
33. Số nguyên tố trong chu kỳ 3 và 5 là:
A. 8 và 18. B. 18 và 8. C. 8 và 8. D. 18 và 18.
34. Các nguyên tố thuộc cùng một nhóm A có tính chất hóa học tương tự nhau, vì vỏ nguyên tử các nguyên tố nhóm A có:
A. số electron như nhau. B. số lớp electron như nhau.
C. số electron thuộc lớp ngoài cùng như nhau. D. cùng số electron s hay p.
35. Sự biến thiên tính chất của các nguyên tố thuộc chu kỳ sau được lặp lại tương tự như chu kỳ trước là do:
A. Sự lặp lại tính chất kim loại của các nguyên tố ở chu kỳ sau so với chu kỳ trước.
B. Sự lặp lại tính chất phi kim của các nguyên tố ở chu kỳ sau so với chu kỳ trước.
C. Sư lặp lại cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố ở chu kỳ sau so với chu kỳ trước (ở ba chu kỳ đầu).
D. Sự lặp lại tính chất hóa học của các nguyên tố ở chu kỳ sau so với chu kỳ trước.
36. Trong một chu kỳ, bán kính nguyên tử các nguyên tố
A. tăng theo chiều tăng dần của điện tích hạt nhân.
B. giảm theo chiều tăng dần của điện tích hạt nhân.
C. giảm theo chiều tăng của tính phi kim. D. B và C đều đúng.
37. Các nguyên tố halogen được sắp xếp theo chiều bán kính nguyên tử giảm dần (từ trái sang phải) như sau:
A. I, Br, Cl, F. B. F, Cl, Br, I. C. I, Br, F, Cl. D. Br, I, Cl, F.
38. Các nguyên tố ở chu kỳ 2 được sắp xếp theo chiều giá trị độ âm điện giảm dần (từ trái qua phải) như sau:
A. F, O, N, C, B, Be, Li. B. Li, B, Be, N, C, F, O.
C. Be, Li, C, B, O, N, F. D. N, O, F, Li, Be, B, C.
39. Oxit cao nhất của một nguyên tố R ứng với công thức RO2. Nguyên tố R đó là:
A. Magie. B. Nitơ. C. Cacbon. D. Photpho.
40. Theo quy luật biến đổi tính chất đơn chất của các nguyên tố trong bảng tuần hoàn thì:
A. phi kim mạnh nhất là iot. B. kim loại mạnh nhất là liti.
C. phi kim mạnh nhất là flo. D. kim loại yếu nhât là xexi.
41. Số hiệu nguyên tử Z của các nguyên tố X, A, M, Q lần lượt là 6, 7, 20, 19. Nhận xét nào sau đây đúng ?
A. X thuộc nhóm VA. B. A, M thuộc nhóm IIA.
C. M thuộc nhóm IIB. D. Q thuộc nhóm IA.
42. Số hiệu nguyên tử Z của các nguyên tố X, A, M, Q lần lượt là 6, 7, 20, 19. Nhận xét nào sau đây đúng ?
A. Cả 4 nguyên tố trên thuộc 1 chu kỳ. B. M, Q thuộc chu kỳ 4.
C. A, M thuộc chu kỳ III. D. Q thuộc chu kỳ III.
43. Trong bảng tuần hoàn, nguyên tố X có số thứ tự 16, nguyên tố X thuộc
A. Chu kỳ 3, nhóm IVA. B. Chu kỳ 4, nhóm VIA.
C. Chu kỳ 3, nhóm VIA. D. Chu kỳ 4, nhóm IIIA.
44. Tìm câu sai trong những câu dưới đây
A. Trong chu kỳ, các nguyên tố được sắp xếp theo chiều điện tích hạt nhân tăng dần.
B. Trong chu kỳ, các nguyên tố được sắp xếp theo chiều số hiệu nguyên tử tăng dần.
C. Nguyên tử của các nguyên tố trong cùng một chu kỳ có số electron bằng nhau.
D. Chu kỳ thường được bắt đầu là một kim loại kiềm, kết thúc là một khí hiếm (trừ chu kì 1 và chu kỳ 7 chưa hoàn thành).
45. Các nguyên tố Na, Mg, Al, Si, P, S, Cl, Ar thuộc chu kỳ 3. Lớp electron ngoài cùng có số electron tối đa là:
A. 3. B. 10. C. 8. D. 20.
46. Nguyên tố X có số thứ tự Z = 9. Hãy chon câu phát biểu đúng.
a. Nguyên tử của nguyên tố X có cấu hình electron là:
A. 1s22s22p3. B. 1s22s22p4. C. 1s22s22p5. D. 1s22s22p6.
b. Nguyên tố X thuộc chu kỳ: A. 1. B. 2. C. 3. D. 4.
c. Nguyên tố X thuộc nhóm: A. VIIA. B. VA. C. VIIIA. D. VIA.
47. Nguyên tố X thuộc chu kỳ 3, nhóm IIA. Nguyên tử của nguyên tố X có cấu hình electron là:
A. 1s22s22p33s1. B. 1s22s22p6. C. 1s22s22p53p4. D. 1s22s22p63s2.
48. Dãy nguyên tố nào sắp xếp theo chiều tăng dần của bán kính nguyên tử?
A. Be, F, O, C, Mg. B. Mg, Be, C, O, F. C. F, O, C, Be, Mg. D. F, Be, C, Mg, O.
49. Trong các nguyên tố sau đây, nguyên tử của nguyên tố nào có bán kính lớn nhất?
A. Al. B. P. C. S. D. K. E. Na.
50. Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần độ âm điện của nguyên tử?
A. Li, F, N, Na, C. B. F, Li, Na, C, N. C. Na, Li, C, N, F. D. N, F, Li, C, Na.
51. Trong bảng tuần hoàn các nguyên tố, nhóm gồm những nguyên tố phi kim điển hình là nhóm:
A. IA. B. IIA. C. VIIA. D. VA.
52. Trong bảng tuần hoàn các nguyên tố, nhóm gồm những nguyên tố kim loại điển hình là nhóm:
A. IA. B. IIA. C. VIIA. D. VA.
53. Cho các nguyên tố: Ca, C, F, O, Be.
a. Dãy nguyên tố nào sau đây được sắp xếp theo chiều tăng dần độ âm điện của nguyên tử?
A. C, F, Ca, O, Be. B. Ca, Be, C, O, F. C. F, O, C, Be, Ca. D. O, C, F, Ca, Be.
b. Dãy nguyên tố nào sau đây được sắp xếp theo chiều tăng dần bán kính của nguyên tử?
A. C, F, O, Be, Ca. B. Ca, Be, C, O, F. C. F, C, O, Ca, Be. D. F, O, C, Be, Ca.
54. Hợp chất của một nguyên tố có công thức RH2. Oxit cao nhất của R chiếm 40% khối lượng R. R là:
A. S. B. Se. C. N. D. Ca. E. KQ khác.
55. B là nguyên tố có hóa trị cao nhất đối với oxi bằng hóa trị trong hợp chất khí với hiđro. Oxit cao nhất của B chứa 53,33% khối lượng oxi. B là :
A. Si. B. C. C. Al. D. N. E. KQ khác.
56. Hai nguyên tố X, Y ở hai nhóm A liên tiếp trong bảng tuần hoàn, X thuộc nhóm V. Ở trạng thái đơn chất X và Y không phản ứng với nhau. Tổng số p trong hạt nhân X và Y bằng 23. X, Y lần lượt là
A. Mg, Na. B. Na, Mg. C. Mg, Al. D. Al, Mg.
57. Khi cho 0,6g một kim loại thuộc nhóm IIA tác dụng với nước thì được 0,336 lít H2 (đkct). Tên kim loại là:
A. canxi. B. beri. C. magie. D. bari.
58. Hòa tan m g kim loại Mg trong dung dịch HCl rồi cô cạn thì thu được 9,5 g MgCl2. Giá trị m là:
A.2,4. B. 4,2. C. đồng. D. 2,5. E. 5,2.
59. 0,5 mol hỗn hợp 2 kim loại liên tiếp ở nhóm IIA có khối lượng là 18g. Xác định hai kim loại.
A. Mg, Ca. B. Be, Mg. C. Ca, Sr. D. Sr, Ba.
60. Hòa tan hoàn toàn 1,08g hỗn hợp 2 kim loại kiềm ở hai chu kỳ liên tiếp vào nước, thu được 0,448lit H2 (đktc).
a. 2 kim loại trên là:
A. Na, K. B. Li, Na. C. K, Rb. D. Cs, Rb.
b. Phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp là:
A. 63,9; 36,1. B. 60, 40. C. 50, 50. D. 40, 60.
61. Cấu hình electron của nguyên tố  là 1s22s22p63s23p64s1. Vậy nguyên tố
là 1s22s22p63s23p64s1. Vậy nguyên tố  có đặc điểm:
có đặc điểm:
A. Nguyên tố thuộc chu kỳ 4, nhóm IA. B. Số nơtron trong nhân nguyên tử X là 20.
C. X là nguyên tố kim loại có tính khử mạnh. D. Là nguyên tố mở đầu chu kỳ 4.
E. Cả 4 câu trên đều đúng.
62. Cho các nguyên tố X1, X2, X3, X4, X5, X6 lần lượt có cấu hình electron như sau:
X1 : 1s22s22p63s2; X2: 1s22s22p63s23p64s1; X3: 1s22s22p63s23p64s2;
X4: 1s22s22p63s23p5. X5: 1s22s22p63s23p63d64s2. X6: 1s22s22p63s23p1.
Các nguyên tố nào thuộc cùng một chu kỳ:
A. X1, X4, X6. B. X2, X3, X5. C. X3, X4.
D. X1, X2, X6. E. Cả A, B đều đúng.
63. Cho các nguyên tố X1, X2, X3, X4 lần lượt có cấu hình electron như sau:
X1 : 1s22s22p63s2; X2: 1s22s22p63s23p64s1; X3: 1s22s22p63s23p64s2; X4: 1s22s22p63s23p5.
Các nguyên tố kim loại là:
A. X1, X2, X3. B. X1, X2, X4. C. X2, X3, X4. D. Tất cả các nguyên tố đã cho.
64. A, B là hai nguyên tố đứng kế tiếp nhau trong cùng một chu kì của bảng HTTH. Tổng số hạt proton trong hạt nhân hai nguyên tử A, B là 17. X, Y lần lượt là
A. Al, Si. B. Si, Al. C. Na, C. D. C, Na.
65. Ion X2+ có cấu hình electron: 1s22s22p6. Hãy cho biết X ở chu kỳ mấy? nhóm mấy?
A. Chu kỳ 3, nhóm IIA. B. Chu kỳ 2, nhóm VIA. C. Chu kỳ 2, nhóm VIIA. D. Chu kỳ 4, nhóm IIA.
66. Ion Y- có cấu hình electron: 1s22s22p63s23p6. Hãy cho biết Y ở chu kỳ nào? nhóm nào?
A. Chu kỳ 3, nhóm VIIA. B. Chu kỳ 3, nhóm VIA. C. Chu kỳ 4, nhóm IA. D. Chu kỳ 4, nhóm IIA.
67. Một nguyên tố R có cấu hình electron: 1s22s22p3, công thức hợp chất với hiđro và công thức oxit cao nhất là:
A. RH2, RO. B. RH3, R2O5. C. RH4, RO2. D. RH5, R2O5.
68. Nguyên tố Z thuộc chu kỳ 3, nhóm VIIA, cấu hình electron của Z là:
A. 1s22s22p63s23p5. B. 1s22s22p63s23p5. C. 1s22s22p63s23p64s24p5. D. 1s22s22p63s23p63d104s24p5.
69. Thứ tự giảm dần của bán kính nguyên tử của các nguyên tử là
A. Na>Mg> Al. B. Al>Mg>Na. C. Mg>Na> Al. D. Na>Al>Mg.
70. Thứ tự tăng dần của bán kính nguyên tử của các nguyên tử là
A. Na<Mg<Al. B. Al<Mg<Na. C. Mg<Na< Al. D. Na<Al<Mg.
71. Khảo sát các nguyên tố trong cùng một chu kỳ, ta có kết luận nào sau đây không luôn luôn đúng?
A. Đi từ trái qua phải các nguyên tố được sắp xếp theo chiều số điện tích hạt nhân tăng dần.
B. Tất cả các nguyên tử có số lớp electron bằng nhau và số hiệu nguyên tử tăng dần.
C. Mở đầu chu kỳ bao giờ cũng là một kim loại kiềm và kết thúc chu kỳ là một khí hiếm.
D. Đi từ trái qua phải, tính kim loại tăng dần.
72. Hai nguyên tố X, Y cùng một nhóm và ở hai chu kì liên tiếp nhau trong bảng HTTH. Tổng số đơn vị điện tích hạt nhân của chúng bằng 24. X, Y lần lượt là
A. O, S. B. S, O. C. N, P. D. P, N.
73. Phát biểu nào sau đây sai: Trong một chu kỳ, khi đi từ trái sang phải, có các qui luật biến thiên tuần hoàn:
A. Hóa trị cao nhất đối với oxi tăng dần từ 1 ® 8.
B. Hóa trị đối với hiđro của phi kim giảm dần từ 7 ®1.
C. Tính kim loại giảm dần, tính phi kim tăng dần.
D. Oxit và hiđroxit có tính bazơ giảm dần, tính axit tăng dần.
74. Giá trị độ âm điện tăng theo
A. Chiều tăng số lớp electron. B. Chiều tăng tính kim loại.
C. Chiều tăng tính phi kim. D. Chiều tăng khối lượng nguyên tử.
75. So sánh tính kim loại: Li :1; Na :2 ; K:3
A. 1>2>3 B. 2>1>3 C. 3>1>2 D. 3>2>1
76. Nguyên tố X có Z = 20. Vị trí của X trong hệ thống hoàn:
A. chu kì 4, nhóm IIA. B. chu kì 3, nhóm IA C. chu kì 4, nhóm IIIA. D.Tất cả đều sai.
77. Nguyên tố R có công thức hợp chất với hiđro là RH thì công thức hợp chất oxit cao nhất là:
A. R2O B. R2O7 C. R2O hoặc R2O7 D. R2O hoặc R2O5
78. Hai nguyên tố X, Y thuộc cùng một phân nhóm và ở hai chu kì liên tiếp trong bảng HTTH, có tổng số proton trong hạt nhân nguyên tử hai nguyên tố là 30. X, Y lần lượt là
A. Na, K. B. K, Na. C. Mg, Ca. D. Ca, Mg.
79. Trong các nguyên tố sau, nguyên tố nào có cùng hóa trị trong oxit cao nhất?
A: F, Cl, Br, I B: N, V, As C: Na, K, Cu, Ag D: Cr, Fe, S
80. Từ F®I:
A. Chiều giảm độ âm điện. B. Chiều giảm tính phi kim.
C. Chiều tăng bán kính nguyên tử. D. A, B, C đều đúng.
81. X ở chu kỳ 3, nhóm VA. X có cấu hình electron là
A. 1s22s22p63s23p1 B. 1s22s22p1 C. 1s22s22p63s23p3 D. Kết quả khác.
82. Cho 8,8g hỗn hợp hai kim loại ở hai chu kỳ liên tiếp và đều thuộc nhóm II trong HTTH tác dụng với dung dịch HCl dư thu được 6,72lit khí ở điều kiện chuẩn. 2 kim loại đó là:
A. Li, Fe B. Ca, Ba C. Mg, Ca D. Mg, Zn.
83.Yếu tố nào sau đây ảnh hưởng đến tính chất hóa học của nguyên tố:
A. Số nơtron trong nguyên tử. B. Số proton trong nguyên tử. C. Số khối của nguyên tử. D. Tất cả đều đúng.
84. Những tính chất sau không biến đổi tuần hoàn là:
A. Hóa trị cao nhất đối với oxi. B. KLNT.
C. Thành phần oxit, hiđroxit. D. Số electron lớp ngoài cùng.
85. Cấu hình electron của R: 1s22s22p4 . Công thức hợp chất với hiđro và công thức oxit cao nhất là:
A. RH2, RO. B. RH3, R2O3 C. RH2, RO3 D. RH5, R2O5.
86. Oxit cao nhất của một nguyên tố là R2O5. Hợp chất với hiđro của R chiếm 43,66 % về khối lượng. Khối lượng và tên của R là:
A. 39, K B. 31, P C.28, N D. Kết quả khác.
87. Thứ tự tăng dần bán kính nguyên tử:
A. Cl<F<P<Na< Al B. F< Cl<P<Na< Al C. Cl<F<P<Na< Al D. F< Cl<P< Al <Na
88. Nguyên tố X thuộc chu kỳ 3, nhóm IIIA. Cấu hình electron của X là:
A. 1s22s22p63s23p3. B. 1s22s22p63s3. C. 1s22s22p63s23p1. D. 1s22s22p3.
89. Những nguyên tố nào sau đây có cùng hóa trị với nhau trong hợp chất với hiđro:
A. N, P, As B. Cl, F, Br C. Te, O, S D. Tất cả đều đúng.
90. B là nguyên tố có hóa trị cao nhất đối với oxi bằng hóa trị trong hợp chất khí với hiđro. Oxit cao nhất của B chứa 53,33% khối lượng oxi. B là : A. Si. B. C. C. Al. D. KQ khác.
91. Oxit cao nhất của một nguyên tố R có công thức là R2O5. trong hợp chất với hiđro, R chiếm 82,35% về khối lượng. Vậy R là: A. 14N B. 122 Sb C. 31P. D. 75As.
92. Xét 3 nguyên tố có cấu hình lần lượt là: (X) 1s22s22p63s1; (Y) 1s22s22p63s2 ;(Z)1s22s22p63s23p1. Hyđroxit của X, Y, Z xếp theo thứ tự tính bazơ tăng dần là :
A. XOH < Y(OH)2 < Z(OH)3 B. Y(OH)2 < Z(OH)3 < X(OH) C. Z(OH)3 < Y(OH)2 < XOH D. Kết quả khác.
93. Xét 3 nguyên tố có cấu hình lần lượt là: (X) 1s22s22p63s1; (Y) 1s22s22p63s2 ; (Z)1s22s22p63s23p1. Hyđroxit của X, Y, Z xếp theo thứ tự tính bazơ giảm dần là :
A. XOH > Y(OH)2 > Z(OH)3 B. Y(OH)2 >Z(OH)3 > X(OH) C. Z(OH)3 > Y(OH)2 > XOH D. Kết quả khác.
94. Nguyên tố thuộc phân nhóm chính nếu:
A. Thuộc chu kỳ 1,2,3. B. Thuộc chu kỳ 4,5,6,7.
C. Electron có mức năng lượng cao nhất thuộc orbital s hoặc p.
D. A, C đúng.
95. Nguyên tử nguyên tố X có tổng số hạt là 40, thuộc nhóm IIIA. X là:
A. Al. B. B. C. Fe. D. Cr.
96. Nguyên tố X có Z = 26. Vị trí của X trong bảng HTTH là:
A. Chu kì 4, nhóm IIIA. B. Chu kì 4, nhóm IIIB.
C. Chu kì 4, nhóm VIA. D. Chu kì 4, nhóm VIIIB.
97. Oxit cao nhất của một nguyên tố là R2O5. Hợp chất với hiđro của R chiếm 8,82% về khối lượng. Nguyên tử khối và tên của R là
A. 39, K B. 31, P C.28, N D. Kết quả khác.
98. Nguyên tố A có cấu hình electron lớp ngoài cùng : …3d54s1. Phát biểu đúng là
A. A ở nhóm VI. B. A có 6 electron hóa trị. C. Oxit cao nhất AO3.D. Tất cả đều đúng.
99. Bán kính nguyên tử các nguyên tố Cl, S, Mg, Si giảm dần theo thứ tự sau:
A. Cl>S>Mg>Si. B. Cl> S> Si>Mg. C. S>Mg> Si>Cl. D. Mg>Si >S>Cl.
100. Bán kính nguyên tử các nguyên tố Cl, S, Mg, Al giảm dần theo thứ tự sau:
A. Mg>Al>S>Cl. B. Cl> S> Al>Mg. C. S>Mg> Al>Cl. D. Mg>Cl>S>Al.
CHƯƠNG 3
1. Liên kết ion là liên kết được tạo thành
A. bởi cặp electron chung giữa hai nguyên tử phi kim.
B. bởi cặp electron chung giữa hai nguyên tử kim loại.
C. bởi cặp electron giữa một nguyên tử kim loại điển hình và một nguyên tử phi kim điển hình.
D. do lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
2. Liên kết cộng hóa trị là liên kết được hình thành giữa hai nguyên tử
A. bằng một hay nhiều cặp electron chung.
B. bằng cặp electron chung giữa hai nguyên tử kim loại.
C. bằng cặp electron chung giữa một nguyên tử kim loại điển hình và một nguyên tử phi kim điển hình.
D. do lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
3. Bản chất của liên kết ion là
A. cho electron. B. cho và nhận electron. C. nhận electron. D. chung cặp electron.
4. Bản chất của liên kết cộng hóa trị không cực là
A. đôi electron chung lệch về nguyên tử bên trái.
B. đôi electron chung lệch về nguyên tử bên phải.
C. đôi electron chung cho một nguyên tử.
D. đôi electron chung không lệch về nguyên tử nào.
5. Bản chất của liên kết cộng hóa trị có cực là
A. đôi electron chung lệch về nguyên tử nào có độ âm điện nhỏ hơn.
B. đôi electron chung lệch về nguyên tử nào có độ âm điện lớn hơn.
C. đôi electron chung không lệch về nguyên tử nào.
D. đôi electron lệch về phía nguyên tử có tính phi kim yếu.
6. Trong các hợp chất sau, hợp chất có liên kết cộng hóa trị là
A. LiCl B. NaF C. KBr D. CCl4
7. Trong các hợp chất sau, hợp chất ion là
A. HCl B. H2O C. NH3 D. CsF
8. Cộng hóa trị của Cl trong hợp chất nào sau đây lớn nhất:
A. HClO B. Cl2O7 C. HClO3 D. AlCl3
9. Nguyên tố A là kim loại kiềm (nhóm IA). Nguyên tử của nguyên tố B có 7 electron lớp ngoài cùng. Công thức của hợp chất tạo bởi A và B là
A. A7B B. AB7 C. AB D. A7B2
10. Nguyên tử của nguyên tố X có tổng số hạt p, n, e là 18. Liên kết hóa học trong oxit của X là:
A. liên kết ion B. liên kết cộng hóa trị phân cực. C. liên kết cộng hóa trị không phân cực. D. liên kết cho nhận.
11. Ion X- có cấu hình electron là 1s22s22p6, nguyên tử Y có số electron ở các phân lớp s là 5. Liên kết giữa X và Y thuộc loại liên kết nào sau đây:
A. cộng hóa trị phân cực. B. cho nhận. C. ion. D. cộng hóa trị.
12. Những nguyên tố nào sau đây có cùng hóa trị cao nhất đối với oxi: 16A, 15B, 24D, 8E?
A. A, B B. A, D. C. A, E. D. B, E.
13. Nguyên tử phi kim có khuynh hướng đặc trưng là.....và tạo thành.....
A. nhận e – ion dương B. nhường e – ion âm. C. nhường e – ion dương. D. nhận e – ion âm.
14. Nguyên tử R có cấu hình electron là 1s22s22p63s23p1. Ion mà R có thể tạo thành là:
A. R- B. R3- C. R+ D. R3+
15. Công thức electron của HCl là:
A. H: Cl B. H : Cl C. H :Cl D. H::Cl.
16. Liên kết hóa học trong phân tử flo, clo, brom, iot, oxi đều là:
A. Liên kết ion. B. Liên kết cộng hóa trị có cực. C. Liên kết cộng hóa trị không cực. D. Liên kết đôi.
17. Liên kết trong phân tử HCl, HBr, HI, H2O đều là
A. liên kết ion. B. liên kết cộng hóa trị có cực. C. liên kết cộng hóa trị không cực. D. liên kết đôi.
18. Hạt nhân của nguyên tử X có 19 prroton, của nguyên tử Y có 17 proton,liên kết hóa học giữa X và Y là:
A. liên kết cộng hóa trị không cực B. liên kết cộng hóa trị có cực. C. liên kết ion.D. liên kết cho nhận.
19. Liên kết hóa học trong KCl được hình thành do
A. hai hạt nhân nguyên tử hút electron rất mạnh. B. mỗi nguyên tử K và Cl góp chung một electron.
C. nguyên tử clo nhường electron, nguyên tử K nhận electron tạo nên hai ion ngược dấu, hút nhau tạo nên phân tử KCl
D. nguyên tử K nhường electron, nguyên tử Cl nhận electron tạo nên hai ion ngược dấu, hút nhau tạo nên phân tử KCl.
20. Liên kết cộng hóa trị là liên kết:
A. hình thành do sự góp chung một electron. B. hình thành do sự góp chung 2 electron
C. hình thành do sự góp chung 3 electron. D. hình thành do sự góp chung 1 hay nhiều cặp electron.
21. Độ âm điện của một nguyên tử đặc trưng cho
A. Khả năng hút electron của nguyên tử đó khi hình thành liên kết hóa học.
B. Khả năng nhường electron của nguyên tử đó cho nguyên tử khác.
C. Khả năng tham gia phản ứng mạnh hay yếu của nguyên tử đó.
D. Khả năng nhường proton của nguyên tử đó cho nguyên tử khác.
22. Trong các hợp chất sau đây, hợp chất nào có liên kết cộng hóa trị?
A. LiCl. B. NaF. C. CaF2. D. CCl4.
23. Trong các hợp chất sau đây, hợp chất nào có liên kết ion?
A. HCl. B. H2O. C. NH3. D. NaCl.
24. Khi các nguyên tử liên kết với nhau để tạo thành phân tử thì dù liên kết theo loại nào vẫn phải tuân theo quy tắc:
A. Sau khi liên kết mỗi nguyên tử đều có lớp vỏ ngoài cùng chứa 8 electron.
B. Sau khi liên kết thành phân tử, mỗi nguyên tử phải đạt được cấu hình electron giống như cấu hình electron của nguyên tử khí hiếm gần nó nhất trong bảng hệ thống tuần hoàn.
C. Khi liên kết phải có một nguyên tố nhường electron và một nguyên tố nhận electron.
D. Sau khi liên kết thành phân tử, mỗi nguyên tử phải đạt được cấu hình electron giống nhau và giống với cấu hình electron của nguyên tử khí trơ gần nó nhất trong bảng hệ thống tuần hoàn.
25. Điện hóa trị của các nguyên tố Cl, Br trong các hợp chất với các nguyên tố nhóm IA là:
A. 2- B. 2+ C. 1- D. 1+.
26. Trong hợp chất Al2(SO4)3, điện hóa trị của Al là:
A. 3+ B. 2+ C. 1+ D. 3-.
27. Liên kết trong phân tử HI là liên kết
A. cộng hóa trị không phân cực. B. cộng hóa trị có cực C. cho – nhận D. ion.
28. Giá trị hiệu độ âm điện => 1,7 là liên kết
A. cộng hóa trị. B. cộng hóa trị có cực. C. cộng hóa trị không cực. D. ion.
29. Liên kết trong phân tử NaI là liên kết
A. cộng hóa trị không phân cực. B. cộng hóa trị có cực C. cho – nhận D. ion.
30. Nguyên tố A có 2 electron hóa trị và nguyên tố B có 5 electron hóa trị. Công thức hợp chất tạo bởi A và B là:
A. A2B3 B. A3B2 C. A2B5 D. A5B2
31. Nguyên tử của nguyên tố Y có phân lớp ngoài cùng là 4s. Y là:
A. kim loại. B. phi kim. C. khí hiếm. D. kim loại hoặc phi kim.
32. Phát biểu nào sau đây không đúng ?
A. Liên kết ion được tạo thành do sự dịch chuyển electron từ nguyên tử này sang nguyên tử kia.
B. Hiđro có thể tạo thành hợp chất ion H- với kim loại mạnh.
C. Phi kim có thể tạo thành cation. D. Kim loại có thể tạo thành cation.
33. Hợp chất tạo giữa silic (14Si ) và hydrô (1H )có công thức phân tử là :
A. Si4H. B. SiH2. C. SiH D. SiH4
34. Khí hydroclorua tan tốt trong nước vì
A. Nó là hợp chất. B. Nó là hợp chất của halogen. C. Phân tử phân cực. D. Cl có số oxyhóa âm.
35. Chọn phát biểu sai trong các câu sau
A. Liên kết cộng hoá trị được tạo thành giữa những nguyên tố có tính chất gần giống nhau.
B. Liên kết cộng hoá trị được tạo thành giữa những nguyên tử phi kim .
C. Liên kết ion được tạo thành giữa hai nguyên tố có tính chất hoá học trái ngược nhau.
D. Liên kết cộng hoá trị được tạo thành giữa nguyên tố kim loại điển hình và phi kim điển hình.
36. Nguyên tử X có 20 proton, nguyên tử Y có 9 proton. Công thức hợp chất hình thành từ hai nguyên tử này là:
A. X2Y với liên kết ion. B. X2Y với liên kết cộng hoá trị. C. XY2 với liên kết cộng hoá trị.D. XY2 với liên kết ion.
37. Phân tử được tạo thành giữa kim loại điển hình và phi kim điển hình, liên kết hoá học giữa chúng là:
A. Liên kết ion. B. Liên kết cộng hoá trị có phân cực. C. Liên kết cộng hoá trị không phân cực. D. Liên kết kim loại.
38. Trong phân tử NaCl, cấu hình electron của các ion là
A. Na+ 1s22s22p6; Cl- 1s22s22p63s23p6.
B. Na+ 1s22s22p63s23p6; Cl- 1s22s22p6.
C. Na+ 1s22s22p63s23p6; Cl- 1s22s22p63s23p6.
D. Na+ 1s22s22p6; Cl- 1s22s22p6.
39. Khi hình thành phân tử NaCl từ natri và clo:
A.Nguyên tử natri nhường một eletron cho nguyên tử clo để tạo thành các ion dương và âm tương ứng, các ion này hút nhau tạo thành phân tử.
B.Hai nguyên tử góp chung một electron với nhau tạo thành phân tử.
C.Nguyên tử clo nhường một eletron cho nguyên tử natri để tạo thành các ion dương và âm tương ứng, các ion này hút nhau tạo thành phân tử.
D.Mỗi nguyên tử (natri và clo) góp chung một electron để tạo thành cặp electron chung giữa hai nguyên tử đó.
40. Liên kết ion là liên kết được tạo thành
A. bởi cặp electron chung giữa hai nguyên tử phi kim.
B. bởi cặp electron chung giữa hai nguyên tử kim loại.
C. bởi cặp electron chung giữa một nguyên tử kim loại điển hình và một phi kim điển hình.
D. do lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
41. Nguyên tử X có 19 proton, nguyên tử Y có 17 proton. Công thức hợp chất hình thành từ hai nguyên tử này là:
A. X2Y với liên kết ion. B. X2Y với liên kết cộng hoá trị. C. XY2 với liên kết cộng hoá trị. D. XY2 với liên kết ion.
42. Trong phân tử hai nguyên tử của một nguyên tố, liên kết hoá học giữa hai nguyên tử phải là:
A. Liên kết ion. B. Liên kết cộng hoá trị có phân cực. C. Liên kết cộng hoá trị không phân cực. D. Liên kết kim loại.
43. Trong các phân tử sau, phân tử có liên kết đôi giữa hai nguyên tử là:
A. Khí nitơ. B. Khí flo. C. Khí cacbonic. D. Khí hyđrô.
44. Cho độ âm điện của F, S, Cu, Ba lần lượt bằng 3,98 ; 2,58; 1,90; 0,89. Trong các hợp chất CuF2, CuS, BaF2, BaS, hợp chất nào là hợp chất ion?
A. CuF2, BaF2. B. CuS. C. CuF2, BaF2, BaS. D. Cả 4 chất trên.
45. Hợp chất ion AB biết số e của cation bằng số electron của anion và tổng số electron của AB là 20.
A. Chỉ NaF. B. Chỉ MgO. C. NaF và MgO. D. KCl.
46. Cho biết các giá trị độ âm điện Na (0,93) ; Li (0,98) Mg (1,31) ; Al (1,61) ; P(2,19) ; S (2,58) ; Br (2,96) ; N (3,04), Cl (3,16). Liên kết ion có trong phân tử:
A. AlCl3. B. LiBr. C. MgS. D. Na3P.
47. Liên kết trong phân tử nào dưới đây không phải là liên kết cộng hóa trị ?
A. Na2O. B. Br2O7. C. Cl2O5. D. As2O3.
48. Liên kết trong phân tử nào dưới đây là liên kết ion?
A. Na2O. B. Br2O7. C. Cl2O5. D. As2O3.
49. Khuynh hướng nào dưới đây không xảy ra trong quá trình hình thành liên kết hóa học ?
A. Chia tách electron. B. Cho nhận electron. C. Dùng chung electron. D. Dùng chung electron tự do.
50. Hợp chất có liên kết cộng hóa trị có cực được gọi là
A. hợp chất phức tạp. B. hợp chất cộng hóa trị. C. hợp chất không điện li. D. hợp chất trung hòa điện.
50. Hợp chất có liên kết ion được gọi là
A. hợp chất ion. B. hợp chất cộng hóa trị. C. hợp chất không điện li. D. hợp chất trung hòa điện.
51. Liên kết hóa học giữa các ion được gọi là
A. liên kết anion – cation. B. liên kết ion hóa. C. liên kết tĩnh điện. D. liên kết ion.
52. Chất có mạng lưới tinh thể ion là
A. kim cương. B. iot. C. nước đá. D. natriclorua.
53. Trong một phân tử giá trị hiệu độ âm điện > =1,7 là liên kết
A. cộng hóa trị. B. cộng hóa trị có cực. C. cộng hóa trị không cực. D. ion.
54. Chất có mạng lưới tinh thể ion có đặc tính
A. nhiệt độ nóng chảy cao. B. tan kém. C. dễ bay hơi. D. dễ thăng hoa.
55. Liên kết hóa học trong phân tử Hiđrosunfua là liên kết
A. ion. B. cộng hóa trị. C. hiđro. D. cho – nhận.
56. Dãy các chất chỉ chứa liên kết cộng hóa trị là
A. BaCl2 ; CdCl2 ; LiF. B. H2O ; SiO2 ; CH3COOH. C. NaCl ; CuSO4 ; Fe(OH)3.D. N2 ; HNO3 ; NaNO3.
57. Dãy các chất có độ phân cực liên kết tăng dần là
A. NaBr; NaCl; KCl; LiF. B. CO2 ; SiO2; ZnO; CaO. C. CaCl2; ZnSO4; CuCl2; Na2O. D. FeCl2; CoCl2; NiCl2; MnCl2.
58. Trong phân tử nitơ, các nguyên tử liên kết với nhau bằng liên kết
A. cộng hóa trị không cực. B. Ion yếu. C. ion mạnh. D. Cộng hóa trị phân cực.
59. Trong một phân tử giá trị hiệu độ âm điện (0 : < 0,4) là liên kết
A. cộng hóa trị. B. cộng hóa trị có cực. C. cộng hóa trị không cực. D. ion.
60. Trong một phân tử giá trị hiệu độ âm điện (0,4 : < 1,7) là liên kết
A. cộng hóa trị. B. cộng hóa trị có cực. C. cộng hóa trị không cực. D. ion.
61. Số oxi hóa của photpho trong các hợp chất sau: PH3, P2O3, H3PO4 lần lượt là
A. -3, +3, +3. B. -3, +3, +5. C. -3, +5, +3. D. +3, +3, +5.
62. Cọng hóa trị của lưu huỳnh trong các hợp chất sau: H2S, SO2, SO3 lần lượt là
A. 2, 4, 6. B. 2, 6, 4. C. 6, 2, 6. D. 2, 3, 6.
63. Anion X- có cấu hình electron phân lớp ngoài cùng là 3p6. Bản chất liên kết giữa X với hiđro là
A. cộng hóa trị không phân cực. B. cộng hóa trị phân cực. C. ion. D. cho – nhận.
64. Số oxi hóa của nitơ trong các chất: N2, NH3, N2H4, NH4Cl tương ứng là
A. 0, -3, -2, -3. B. 0, 3, 3, 4. C. 2, 3, 0, 4. D. 3, 3, 3, 4.
65. Trong các phân tử sau, phân tử có liên kết ba giữa hai nguyên tử là:
A. Khí nitơ. B. Khí flo. C. Khí cacbonic. D. Khí hyđrô.
66. Điện hóa trị của các ion đơn nguyên tử là
A. điện tích của ion. B. số e nhường. C. số e nhận. D. cả số e nhường và nhận.
67. Phân tử khí cacbon đioxit là phân tử
A. không phân cực. B. phân cực. C. không xác định đuợc. D. có liên kết cộng hóa trị không phân cực.
68. Cation X+ có cấu hình electron phân lớp ngoài cùng là 2p6. Bản chất liên kết giữa X với clo là
A. cộng hóa trị không phân cực. B. cộng hóa trị phân cực. C. ion. D. cho – nhận.
69. Trong hợp chất AlCl3 điện hóa trị của Al, Cl lần lượt là
A. 3+, 1+. B. 2+, 1-. C. 1+, 2-. D. 3+, 1-.
70. Điện hóa trị của các nguyên tố nhóm IA trong tất cả các hợp chất là
A. 2- B. 2+ C. 1- D. 1+.
71. Nguyên tử của nguyên tố Y có 8 e ở lớp ngoài cùng. Y là
A. kim loại. B. phi kim. C. khí hiếm. D. kim loại hoặc phi kim.
72. Nguyên tử R có cấu hình electron là 1s22s22p63s1. Ion mà R có thể tạo thành là:
A. R- B. R3- C. R+ D. R3+
73. Nguyên tử R có cấu hình electron là 1s22s22p63s23p4. Ion mà R có thể tạo thành là:
A. R- B. R2- C. R+ D. R3+
74. Nguyên tử R có cấu hình electron là 1s22s22p63s23p5. Ion mà R có thể tạo thành là:
A. R- B. R2- C. R+ D. R3+
75. Ion X- có cấu hình electron là 1s22s22p63s23p6, nguyên tử Y có số electron ở phân lớp s là 1. Liên kết giữa X và Y thuộc loại liên kết nào sau đây:
A. cộng hóa trị phân cực. B. cho nhận. C. ion. D. cộng hóa trị.
76. Ion X- có cấu hình electron là 1s22s22p6 3s23p6 .Liên kết giữa phân tử X thuộc loại liên kết nào sau đây:
A. cộng hóa trị phân cực. B. cho nhận. C. ion. D. cộng hóa trị không cực.
77. Ion X- có cấu hình electron là 1s22s22p3 .Liên kết giữa phân tử X thuộc loại liên kết nào sau đây:
A. cộng hóa trị phân cực. B. cho nhận. C. ion. D. cộng hóa trị không cực.
78. Nguyên tử của nguyên tố Y có 3 e ở các phân lớp s. Y là
A. kim loại. B. phi kim. C. khí hiếm. D. kim loại hoặc phi kim.
79. Điện hóa trị của các nguyên tố Cl, I trong các hợp chất với các nguyên tố nhóm IA là:
A. 2- B. 2+ C. 1- D. 1+.
80. Điện hóa trị của các nguyên tố Na, K trong mọi hợp chất là
A. 2- B. 2+ C. 1- D. 1+.
81. Cộng hóa trị của nitơ và hiđrô trong phân tử NH3 lần lượt là
A. 0, 1. B. 3, 1. C. 1, 3. D. 1, 0.
82. Điện hóa trị của magiê, clo trong phân tử MgCl2 lần lượt là
A. 2+, 1-. B. 1-, 2+. C. 1+, 2-. D. 2-, 1+.
83. Số oxi hóa của lưu huỳnh trong các phân tử và ion sau: H2S, SO2, SO3, SO32- lần lượt là
A. -2, +4, +6, +6. B. -2, +4, +6, +4. C. A. -2, +4, +4, +6. D. +4, +4, +6, +6.
84. Số oxi hóa của lưu huỳnh trong các phân tử và ion sau: SO42-, H2SO4, H2SO3. lần lượt là
A. -2, +4, +6. B. +6, +4, +6. C. +6, +6, +4. D. +4, +6, +6.
85. Số oxi hóa của mangan trong các phân tử sau: MnO2, MnO, KMnO4, K2MnO4 lần lượt là
A. +4, +3, +6, +7. B. +4, +2, +7, +6. C. +2, +4, +6, +7. D. +4, +6, +7, +2.
86. Cộng hóa trị và số oxi hóa của cacbon trong các hợp chất sau: CH4, C2H6, C2H4, HCHO lần lượt là
A. 4 , 4, 4, 4. B.1, 2, 3, 4. C. 4, 3, 2, 1. D. 2, 4, 2, 4.
87. Số oxi hóa của cacbon trong các hợp chất sau: CH4, C2H6, C2H4, HCHO lần lượt là
A. -4, -2, -2, -4. B. -4, -3, -2, 0. C. -4, -2, 0, -4. D. -4, 0, -2, -4.
88. Cộng hóa trị của C và H trong phân tử CH4 lần lượt là
A. 1, 4. B. 4, 4. C. 4, 1. D. 1, 1.
89. Cộng hóa trị của nitơ trong các hợp chất sau NH3, HNO3 lần lượt là
A. 3, 4. B. 4, 3. C. 3, 3. D. 4, 4.
90. Số oxi hóa của clo trong các phân tử sau: HCl, Cl2, HClO, HClO2, HClO3, HClO4 lần lượt là
A. -1, 0, +1, +3, +5, +7. B. -1, 0, +3, +1, +5, +7. C. -1, 0, +1, +3, +5, +7. D. -1, 0, +1, +7, +5, +3.
91.Trong phản ứng oxi hóa – khử
A. chất bị oxi hóa nhận điện tử và chất bị khử cho điện tử.
B. quá trình oxi hóa và khử xảy ra đồng thời.
C. chất chứa nguyên tố số oxi hóa cực đại luôn là chất khử.
D. quá trình nhận điện tử gọi là quá trình oxi hóa.
92. Chất khử là chất
A. cho điện tử, chứa nguyên tố có số oxi hóa tăng sau phản ứng.
B. cho điện tử, chứa nguyên tố có số oxi hóa giảm sau phản ứng.
C. nhận điện tử, chứa nguyên tố có số oxi hóa tăng sau phản ứng.
D. nhận điện tử, chứa nguyên tố có số oxi hóa giảm sau phản ứng.
93.Chất oxi hoá là chất
A. cho điện tử, chứa nguyên tố có số oxi hóa tăng sau phản ứng.
B. cho điện tử, chứa nguyên tố có số oxi hóa giảm sau phản ứng.
C. nhận điện tử, chứa nguyên tố có số oxi hóa tăng sau phản ứng.
D. nhận điện tử, chứa nguyên tố có số oxi hóa giảm sau phản ứng.
94. Chọn phát biểu không hoàn toàn đúng.
A. Sự oxi hóa là quá trình chất khử cho điện tử.
B. Trong các hợp chất số oxi hóa H luôn là +1.
C. Cacbon có nhiều mức oxi hóa (âm hoặc dương) khác nhau.
D. Chất oxi hóa gặp chất khử chưa chắc đã xảy ra phản ứng.
95. Phản ứng oxi hóa – khử xảy ra theo chiều tạo thành
A. chất oxi hóa yếu hơn so với ban đầu. B. chất khử yếu hơn so với chất đầu.
C. chất oxi hóa (hoặc khử) mới yếu hơn. D. chất oxi hóa (mới) và chất khử (mới) yếu hơn.
96. Phát biểu nào dưới đây không đúng?
A. Phản ứng oxi hoá - khử là phản ứng luôn xảy ra đồng thời sự oxi hoá và sự khử.
B. Phản ứng oxi hoá - khử là phản ứng trong đó có sự thay đổi số oxi hoá của tất cả các nguyên tố.
C. Phản ứng oxi hoá - khử là phản ứng trong đó xảy ra sự trao đổi electron giữa các chất.
D. Phản ứng oxi hoá - khử là phản ứng trong đó có sự thay đổi số oxi hoá của một số nguyên tố
97. Phản ứng giữa các loại chất nào sau đây luôn luôn là phản ứng oxi hóa – khử ?
A. oxit phi kim và bazơ. B. oxit kim loại và axit.
C. kim loại và phi kim. D. oxit kim loại và oxit phi kim.
98.Cho các hợp chất: NH , NO2, N2O, NO
, NO2, N2O, NO , N2. Thứ tự giảm dần số oxi hóa của N là
, N2. Thứ tự giảm dần số oxi hóa của N là
A. N2 > NO > NO2 > N2O > NH
> NO2 > N2O > NH . B. NO
. B. NO > N2O > NO2 > N2 > NH
> N2O > NO2 > N2 > NH .
.
C. NO > NO2 > N2O > N2 > NH
> NO2 > N2O > N2 > NH . D. NO
. D. NO > NO2 > NH
> NO2 > NH > N2 > N2O.
> N2 > N2O.
99. Số oxi hóa của oxi trong các hợp chất HNO3, H2O2, F2O, KO2 theo thứ tự là
A. -2, -1, -2, -0,5. B. -2, -1, +2, -0,5. C. -2, +1, +2, +0,5. D. -2, +1, -2, +0,5.
100. Cho các hợp chất: NH , NO2, N2O, NO
, NO2, N2O, NO , N2. Thứ tự tăng dần số oxi hóa của N là
, N2. Thứ tự tăng dần số oxi hóa của N là
A. N2 < NO < NO2 < N2O < NH
< NO2 < N2O < NH . B. NH
. B. NH < N2 < N2O < NO2 <NO
< N2 < N2O < NO2 <NO
C. NO < NO2 < N2O < N2 < NH
< NO2 < N2O < N2 < NH . D. NO
. D. NO < NO2 < NH
< NO2 < NH < N2 < N2O.
< N2 < N2O.
II. TỰ LUẬN
CHƯƠNG 1
Câu 1. Hãy cho biết số đơn vị điện tích hạt nhân, số proton, số nơtron, số electron và số khối của các nguyên tử sau  .
.
Câu 2. Nguyên tử nguyên tố A, B, C, D, có số hiệu nguyên tử lần lượt là 16, 9, 17, 7.
a. Xác định số hiệu nguyên tử, số proton, số e, số đơn vị điện tích hạt nhân của các nguyên tố A, B, C, D?
b. Hãy viết cấu hình elctron của các nguyên tố đó.
c. Lớp electron ngoài cùng của nguyên tử các nguyên tố đó có bao nhiêu electron, những nguyên tử đó thuộc loại nguyên tố gì (nguyên tố s, p, d hay f)?
d. Đó là nguyên tử của nguyên tố kim loại hay phi kim?
Câu 3. Trong một nguyên tử X, tổng số các hạt: proton, nơtron và electron là 28. Biết rằng số nơtron bằng số proton cộng thêm một.
a. Hãy cho biết số proton có trong nguyên tử và xác định X.
b. Hãy cho biết số khối của hạt nhân.
c. Viết cấu hình electron của nguyên tử và ion X-
d. Hãy cho biết đó là nguyên tử của nguyên tố nào?
Câu 4. Tổng số hạt cơ bản (p, n, e) trong nguyên tử một nguyên tố A là 52. Biết số hạt không mang điện bằng một nửa số hạt mang điện cộng thêm 1. Xác định A và vị trí của nó (số thứ tự, chu kì, nhóm) trong bảng tuần hoàn?
Câu 5. Tính nguyên tử khối trung bình ( ) của các nguyên tố sau (xem nguyên tử khối trùng với số khối). Cho biết:
) của các nguyên tố sau (xem nguyên tử khối trùng với số khối). Cho biết:
a. Nguyên tố brom là hỗn hợp hai đồng vị  hàm lượng 50,7%;
hàm lượng 50,7%;  hàm lượng 49,3% (so với tổng khối lượng của brom tự nhiên).
hàm lượng 49,3% (so với tổng khối lượng của brom tự nhiên).
b. Nguyên tố clo là hỗn hợp 2 đồng vị:  có nguyên tử khối là 34,97; 37Cl có nguyên tử khối là 36,97. Biết rằng đồng vị
có nguyên tử khối là 34,97; 37Cl có nguyên tử khối là 36,97. Biết rằng đồng vị  chiếm 75,77%.
chiếm 75,77%.
c. Trong tự nhiên Brom có 2 đồng vị  ( 54,5%) và
( 54,5%) và  ( 45,5%).
( 45,5%).
Câu 6. Tính thành phần phần trăm mỗi đồng vị tồn tại trong tự nhiên ở các trường hợp:
a. Liti tự nhiên có hai đồng vị:  và
và  . Biết rằng nguyên tử khối trung bình của Li tự nhiên là 6,94 đvC. (Xem nguyên tử khối trùng với số khối)
. Biết rằng nguyên tử khối trung bình của Li tự nhiên là 6,94 đvC. (Xem nguyên tử khối trùng với số khối)
b. Đồng có hai đồng vị là  , khối lượng nguyên tử trung bình của đồng 63,54 đvC.
, khối lượng nguyên tử trung bình của đồng 63,54 đvC.
c. Clo có hai đồng vị là  , khối lượng nguyên tử trung bình của clo là 35,5 đvC.
, khối lượng nguyên tử trung bình của clo là 35,5 đvC.
CHƯƠNG 2 VÀ CHƯƠNG 3
Câu 1. Hai nguyên tố X, Y cùng một nhóm và ở hai chu kì liên tiếp nhau trong bảng HTTH. Tổng số đơn vị điện tích hạt nhân của chúng bằng 32.
a) Xác định vị trí của X, Y (số thứ tự, chu kì, nhóm) và X, Y?
b) So sánh độ âm điện, bán kính nguyên tử và tính chất hóa học của X và Y?
Câu 2. Hai nguyên tố X, Y cùng một nhóm và ở hai chu kì liên tiếp nhau trong bảng HTTH. Tổng số đơn vị điện tích hạt nhân của chúng bằng 24.
a) Xác định vị trí của X, Y (số thứ tự, chu kì, nhóm) và X, Y?
b) So sánh độ âm điện, bán kính nguyên tử và tính chất hóa học của X và Y?
Câu 3. Hai nguyên tố A và B đứng kế tiếp nhau trong cùng một nhóm A, có tổng số đơn vị điện tích hạt nhân là 26. Biết rằng A và B chỉ nằm ở chu kì nhỏ.
a) Xác định vị trí của A, B (số thứ tự, chu kì, nhóm) ?
b) So sánh độ âm điện, bán kính nguyên tử và tính chất hóa học của A và B ?
Câu 4. A, B là hai nguyên tố đứng kế tiếp nhau trong cùng một chu kì của bảng HTTH. Tổng số hạt proton trong hạt nhân hai nguyên tử A, B là 17.
a) Viết cấu hình e nguyên tử của A, B để suy ra vị trí của A, B?
b) Xác định nguyên tố A, B.
c) So sánh độ âm điện, bán kính nguyên tử và tính chất hóa học của A và B ?
Câu 5. Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kì của bảng tuần hoàn có tổng số đơn vị điện tích hạt nhân là 25.
a) Viết cấu hình e để xác định vị trí của hai nguyên tố A, B trong BTH ?
b) So sánh độ âm điện, bán kính nguyên tử và tính chất hóa học của chúng ?
Câu 6. X, Y, Z là 3 nguyên tố đứng kế tiếp nhau trong cùng một chu kì ( 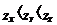 ) của bảng tuần hoàn, có tổng số hiệu nguyên tử là 36.
) của bảng tuần hoàn, có tổng số hiệu nguyên tử là 36.
a) Hãy xác định X, Y, Z và vị trí của nó trong BHTTH?
b) So sánh độ âm điện, bán kính nguyên tử của các nguyên tố X, Y, Z ?
c) Nêu tính chất hóa học của X? Vận dụng hoàn thành các phương trình phản ứng sau:
Câu 7. Ba nguyên tố X, Y, Z đứng kế tiếp trong cùng một chu kì có tổng số hiệu nguyên tử là 39.
a) Hãy xác định vị trí các nguyên tố đó trong BHTTH ?
b) Viết cấu hình electron nguyên tử và gọi tên ba nguyên tố đó?
c) So sánh độ âm điện, bán kính nguyên tử và tính chất hóa học cơ bản của các nguyên tố X, Y, Z?
d) Xác định hóa trị cao nhất của các nguyên tố trên trong hợp chất với oxi? Từ đó viết công thức oxit tương ứng của các hợp chất đó.
Câu 8. Một nguyên tố X có hợp chất với hidro có CTPT dạng XH3. Trong hợp chất oxit, có hóa trị cao nhất thì % khối lượng của X là 25,926%.
a. Xác định tên nguyên tố này?
b. Viết công thức oxit và hidroxit của X, từ đó cho biết oxit và hidroxit này mang tính chất gì (axit hay bazơ hay lưỡng tính)?
Câu 9. Oxit của một nguyên tố RO3 trong hợp chất của nó với hidro có 5,88% hidro về khối lượng.
a. Xác định tên nguyên tố này?
b. Viết công thức oxit và hidroxit của X, từ đó cho biết oxit và hidroxit này mang tính chất gì (axit hay bazơ hay lưỡng tính)?
Câu 10. Hợp chất khí với hidro của một nguyên tố là RH4. Oxit cao nhất của nó chứa 53,3 % oxi về khối lượng. Tìm nguyên tố đó.
a. Xác định tên nguyên tố này?
b. Viết công thức oxit và hidroxit của X, từ đó cho biết oxit và hidroxit này mang tính chất gì (axit hay bazơ hay lưỡng tính)?
Câu 11. Hòa tan hết a g Na trong nước, dung dịch thu được chiếm thể tích 500ml có nồng độ 0,1M. Viết phương trình phản ứng và xác định a?
Câu 12. Cho 3,9 g kim loại K tác dụng với lượng nước dư. Viết phương trình phản ứng xảy ra và tính thể tích khí H2 thoát ra ở điều kiện tiêu chuẩn?
Câu 13. Cho a g Na vào nước thu được 5,6 lít H2 (đktc). Viết phương trình phản ứng xảy ra và tính a?
Câu 14. Hòa tan hết a g K trong nước, dung dịch thu được chiếm thể tích 500ml có nồng độ 0,5M. Viết phương trình phản ứng xảy ra và xác định a?
Câu 15. Hòa tan hoàn toàn 1,08g hỗn hợp 2 kim loại kiềm ở hai chu kỳ liên tiếp vào nước, thu được 0,448lit H2 (đkc). Xác định hai kim loại và viết các phương trình phản ứng xảy ra?
Câu 16. Trong số các chất sau đây: H2, HCl, H2O, Cl2, Br2, I2, NH3, H2S, PH3, CaO, F2, N2 CsF, NaCl, KBr, CH4 chất nào có liên kết ion, chất nào có liên kết cộng hóa trị? Viết công thức electron và công thức cấu tạo của các hợp chất cộng hoá trị trên?
Câu 17. Hãy cho biết số oxi hóa của clo trong các hợp chất sau:
a. HCl, Cl2, Cl2O, Cl2O3, Cl2O5, Cl2O7.
b. HClO3, HClO2, HClO
Hãy cho biết số oxi hóa của Mn trong các hợp chất: Mn, MnO, MnCl4, KMnO4.
Hãy cho biết số oxi hóa của S trong các hợp chất: H2S, SO2, H2SO4,  ,
, 
CHƯƠNG 4
Câu 1. Cân bằng các phản ứng oxi hóa khử sau (theo phuơng pháp thăng bằng electron) và chỉ rõ chất khử, chất oxi, quá trình khử, quá trình oxi hóa:
a. Fe + H2SO4 đặc nóng → Fe2(SO4)3 + SO2 + H2O
b. KMnO4 → K2MnO4 + MnO2 + O2 c. KClO3 → KCl + O2
e. MnO2 + HCl → MnCl2 + Cl2 + H2O f. Cl2 + KOH → KCl + KClO3 + H2O
i. H2SO4 đặc nóng + HBr → Br2 + SO2 + H2O l. Zn + H2SO4 đặc nóng → ZnSO4 + H2S + H2O
m. C + H2SO4đặc nóng → SO2 + CO2 + H2O o. Cu + H2SO4 đặc nóng → CuSO4+ SO2 + H2O
p. Cl2 + NaBr → NaCl + Br2 d. Al + Fe3O4 → Al2O3 + Fe
r. Cl2 + NaI → NaCl + I2
Câu 2. Hòa tan hoàn toàn 2,4g kim loại Mg vào dung dịch HNO3 loãng, giả sử chỉ thu được V lít khí N2 duy nhất (đktc). Tính giá trị của V?
Câu 3. 1,84g hỗn hợp Cu và Fe hòa tan hết trong dung dịch HNO3 tạo thành 0,01 mol NO và 0,04 mol NO2. Tính thành phần phần trăm khối lượng của Fe và Cu?
Câu 4. Cho m gam Cu vào dung dịch HNO3 (loãng) dư thu được Cu(NO3)2 , H2O và 448 ml khí NO (đktc).
a) Viết phương trình phản ứng xảy ra và cân bằng theo phuơng pháp thăng bằng electron?
b) Hãy cho biết giá trị m là bao nhiêu?
Câu 5. Cho 18,4 gam hỗn hợp Mg, Fe với dung dịch HNO3 đủ được 5,824 lít hỗn hợp khí NO, N2 (đktc). Khối lượng hỗn hợp khí là 7,68 gam. Hãy tính thành phần phần trăm khối lượng Fe và Mg trong hỗn hợp ban đầu.
HẾT!
CHÚC CÁC EM HỌC TỐT!


































 Trang Trước
Trang Trước



No comments: