Hóa Học 10 Nâng Cao
Së GD §T Kiªn Giang Trêng THPT Chuyªn Huúnh MÉn §¹t --------------- | Kú thi: KiÓm Tra Hãa 10 N©ng cao M«n thi: Hãa 10 N©ng cao (Thêi gian lµm bµi: 45 phót) |
§Ò sè: 138 |
Hä tªn thÝ sinh:..............................................................SBD:...............................................
C©u 1: Trong các cấu hình electron sau, cấu hình nào viết sai?
C©u 2: Cho nguyên tố X có Z = 17. Nguyên tử X có số electron độc thân ở trạng thái cơ bản là:
A. 1 B. 2 C. 3 D. 5
C©u 3: Các obitan trong một phân lớp electron:
A. có cùng sự định hướng trong không gian.
B. có cùng mức năng lượng.
C. khác nhau về mức năng lượng.
D. có hình dạng không phụ thuộc vào đặc điểm mỗi phân lớp.
C©u 4: Nguyên tử của nguyên tố R có tổng số hạt p,n,e bằng 46, số khối nhỏ hơn 32.Vậy số electron độc thân của nguyên tử R là:
A. 1 B. 2 C. 4 D. 3
C©u 5: Kí hiệu nguyên tử  cho biết
cho biết
A. Tổng số hạt của nguyên tử X là 155
B. số notron của nguyên tử X là 47
C. Tổng số hạt mang điện của nguyên tử X là 108
D. Trong hạt nhân nguyên tử X, số hạt không mang điện nhiều hơn số hạt mang điện là 33 hạt.
C©u 6: Nguyên tử khối trung bình của đồng là 63,54. Trong tự nhiên, đồng tồn tại 2 loại đồng vị là  và
và  . Nếu có 118 nguyên tử của
. Nếu có 118 nguyên tử của  thì có bao nhiêu nguyên tử
thì có bao nhiêu nguyên tử  ?
?
A. 336 B. 319 C. 320 D. 324
C©u 7: Chọn câu sai:
A. Số hiệu nguyên tử của một nguyên tố bằng số đơn vị điện tích hạt nhân nguyên tử của nguyên tố đó
B. Trong hạt nhân nguyên tử, số hạt mang điện bằng số hạt không mang điện
C. Những nguyên tử có cùng điện tích hạt nhân có tính chất hoá học giống nhau.
D. Số khối của hạt nhân bằng tổng số proton và số notron
C©u 8: Một nguyên tố R có 2 đồng vị X và Y, tỉ lệ số nguyên tử X: Y là 45 : 455. Tổng số hạt trong X là 32, Y nhiều hơn X 2 nơtron. Nguyên tử khối trung bình của R là:
A. 23,82 B. 24, 01 C. 22,18 D. 28,02
C©u 9: Chọn câu phát biểu đúng. Theo quan điểm hiện đại, sự chuyển động của electron trong nguyên tử:
A. theo một quỹ đạo tròn hay bầu dục xác định quanh hạt nhân.
B. trên các obitan hình tròn hay hình bầu dục.
C. rất nhanh xung quanh hạt nhân, không theo một quỹ đạo xác định nào.
D. tạo thành đám mây mang điện tích dương.
C©u 10: Nguyên tố Argon có 3 loại đồng vị có số khối lần lượt là 36; 38 và A . Phần trăm số nguyên tử của 3 đồng vị trên lần lượt là: 0,34%, 0,06% và 99,6%. Khối lượng của 125 nguyên tử Argon là 4997,5 (u). Giá trị của A là:
A. 39 B. 40 C. 41 D. 42
C©u 11: Cho hai nguyên tố M và N có số hiệu nguyên tử lần lượt là 11 và 13. Cấu hình electron của M và N lần lượt là:
A. 1s22s22p63s1 và 1s22s22p63s2 B. 1s22s22p63s1 và 1s22s22p63s3
C. 1s22s22p63s1 và 1s22s22p63s23p1 D. 1s22s22p7 và 1s22s22p63s23p1
C©u 12: Một kim loại M có số khối A= 54. Tổng số các hạt cơ bản trong nguyên tử M là 80. Cho biết M là kim loại nào trong số các kim loại sau:
C©u 13: Thí nghiệm tìm ra hạt nhân nguyên tử là:
A. Phóng điện cao thế 15 kV trong chân không
B. Dùng chùm hạt α bắn phá một lá vàng mỏng và dùng màn huỳnh quang theo dõi
C. Bắn phá hạt nhân nguyên tử nitơ bằng hạt α
D. Dùng hạt α bắn phá hạt nhân nguyên tử beri
C©u 14: Electron thuộc lớp nào sau đây liên kết với hạt nhân bền chặt nhất?
A. Lớp K B. Lớp L C. Lớp M D. Lớp N
C©u 15: Cho cấu hình electron của X là: 1s22s22p63s23p3 và cấu hình electron của Y là: 1s22s22p63s23p64s1.
Nhận xét nào sau đây đúng:
A. X và Y đều là kim loại. B. X và Y đều là phi kim.
C. X và Y đều là các khí hiếm. D. X là phi kim, Y là kim loại.
C©u 16: Chọn cặp nguyên tử là đồng vị của cùng một nguyên tố hóa học là:
C©u 17: Phân bố electron trong nguyên tử không tuân theo nguyên lý và quy tắc nào sau đây?
A. Cho nhận electron B. Nguyên lý Pauli C. Nguyên lý vững bền D. Quy tắc Hun
C©u 18: Nguyên tử của các nguyên tố có cấu hình e lớp ngoài cùng như sau: 3s2 3p2 ; 3s2 3p3; 3s2;
3s2 3p5 . Số hiệu nguyên tử của các nguyên tố này lần lượt là:
A. 13,14,20,15 B. 12,14,20,17 C. 14,15,12,17 D. 13,15,20,17
C©u 19: Giả sử trong tự nhiên Mg có hai đồng vị bền là 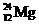 và
và  . Nguyên tử khối trung bình của Mg là 24,31. Phần trăm về khối lượng của
. Nguyên tử khối trung bình của Mg là 24,31. Phần trăm về khối lượng của 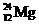 trong Mg(NO3)2 là:
trong Mg(NO3)2 là:
A. 11,16% B. 69% C. 31% D. 11,19%
C©u 20: Một nguyên tử X có tổng số hạt cơ bản là 58, số khối nhỏ hơn 40. Số hiệu của nguyên tử X là:
A. 17 B. 18 C. 19 D. 16
C©u 21: Một mol nguyên tử Ca ( z = 20)có khối lượng là 40 gam. Khối lượng proton trong 1 gam nguyên tử Ca là:(mp = 1,67.10-24 g)
A. 0,503 gam B. 0,2gam C. 4,02 gam D. 0,25 gam
C©u 22: Hai nguyên tố X, Y có cấu hình e lớp ngoài cùng là 3s2 , 4s1. Chọn phát biểu đúng
A. X, Y đều là kim loại B. X, Y có cùng số phân lớp electron
C. X, Y có cùng số lớp electron D. X, Y đều là phi kim
C©u 23: Một nguyên tử có tổng số hạt là 46. Trong đó tỉ số hạt mang điện đối với hạt không mang điện là 1,875. Khối lượng tuyệt đối của nguyên tử đó là:
(Cho biết me = 9,109.10-31 kg ; mp = 1,6726.10-27 kg; mn = 1,6748.10-27 kg).
A. 5,1673.10-26kg B. 5,1899.10-26 kg. C. 5,2131.10-26 kg D. 5,252.10-27kg.
C©u 24: Cho các nguyên tử sau: N, O, Cl, P, Al, Mg, Ne.Các nguyên tử có số e ở lớp ngoài cùng giống nhau là:
A. P, Al, N B. O, Cl, Ne C. Al, Mg D. N, P
C©u 25: Chọn câu sai trong số các câu sau.
A. Nguyên tử khối là khối lượng tuyệt đối của nguyên tử.
B. Một cách gần đúng có thể coi nguyên tử khối xấp xỉ số khối của hạt nhân.
C. Nguyên tử khối trung bình của hỗn hợp các đồng vị là có tính đến tỉ lệ phần trăm số nguyên tử của mỗi đồng vị.
D. Nguyên tử khối của clo 35,5 chính là nguyên tử khối trung bình của clo.
C©u 26: Nguyên tử của nguyên tố R có 3 electron cuối cùng thuộc phân lớp 3d. Cấu hình electron đầy đủ của nguyên tử R theo lớp và phân lớp là:
A. 1s22s22p63s23p64s23d3 B. 1s22s22p63s23p63d34s2
C. 1s22s22p63s23p3 D. 1s22s22p63s23p63d3
C©u 27: Nguyên tử Y có tổng số hạt cơ bản là 58 trong đó số hạt mang điện gấp 1,9 lần số hạt không mang điện . Số khối và tính chất cơ bản của Y là:
A. 39, kim loại B. 18, phi kim C. 20, kim loại D. 39,phi kim
C©u 28: Một nguyên tử R có tổng số e trong các phân lớp p là 8.Số e độc thân của nguyên tử R là:
A. 3 B. 4 C. 1 D. 2
C©u 29: Nguyên tử X có 14e, lớp electron ngoài cùng có số e là:
A. 3 B. 4 C. 8 D. 7
C©u 30: Thí nghiệm tìm ra hạt proton là:
A. Sự phóng điện cao thế trong chân không B. Dùng chùm hạt α bắn phá một lá vàng mỏng
C. Bắn phá hạt nhân nguyên tử nitơ bằng hạt α D. Dùng hạt α bắn phá hạt nhân nguyên tử beri
Cho Mg =12; O = 16; N =14
----------------- HÕt 138 -----------------
Tags: Huỳnh Mẫn Đạt

















 Trang Trước
Trang Trước



No comments: