Đề kiểm tra môn hóa lớp 10 chuyên 16/10/2012
Së GD §T Kiªn Giang Trêng THPT Chuyªn Huúnh MÉn §¹t --------------- | Kú thi: KiÓm Tra Hãa 10 Chuyªn M«n thi: Hãa 10 Chuyªn (Thêi gian lµm bµi: 45 phót) |
§Ò sè: 178 |
Hä tªn thÝ sinh:..............................................................SBD:..........................
Cho độ âm điên của các nguyên tố: Na ( 0,93); K ( 0,82); Rb (0,82); Al (1,61); Mg (1,31); H (2,2);
C (2,55); O (3,44);F (3,98); Cl (3,16); Br (2,96); I (2,66); S (2,58); N ( 3,04); P (2,19); Si (1,9)
Cho Li = 7, Na = 23, K = 39, Rb = 85, Cs = 133; S = 32, O = 16, H = 1, Se = 79, Te = 128; Cl = 35,5; F =19; Mg = 24; Cu =64; Ca =40; Sr = 88; Ba = 137; Si = 28; C =12;
C©u 1: Nguyên tố X có tổng hạt các loại trong nguyên tử là 52. Hợp chất chỉ chứa X và Oxi có liên kết:
A. Ion B. Cộng hóa trị không phân cực
C. Cộng hóa trị có cực D. Ion và Cộng hóa trị
C©u 2: Phân tử IF5 có dạng hình học là:
A. chữ T B. tháp vuông C. tam giác D. bát diện đều
C©u 3: Nguyên tử trung tâm trong phân tử SCl4 có trạng thái lai hóa là:
A. sp B. sp3d C. sp2 D. sp3
C©u 4: Hợp chất X gồm hai nguyên tố là A có Z = 7 và B có Z = 8. Trong phân tử X , A chiếm 25,926% . X có các loại liên kết:
A. Cộng hóa trị và liên kết cho nhận B. Cộng hóa trị có cực
C. Cộng hóa trị không cực D. Liên kết ion và cộng hóa trị có cực
C©u 5: Cho cấu hình elctron của nguyên tử nguyên tố R là 1s2 2s2 2p6 3s2 3p6 3dx 4s2 . Để R ở chu kỳ 4, nhóm IIB thì giá trị của x là:
A. 10 B. 0 C. 8 D. 6
C©u 6: Cho 41,9 (gam) muối cacbonat của 2 kim loại X và Y ở nhóm II A thuộc 2 chu kỳ liên tiếp vào dung dịch HCl dư. Sau phản ứng thu được một khí có V= 5,6 (l) (ở đkc). Tên của X và Y là:
A. Mg, Ca B. Ca, Ba C. Ba, Sr D. Ca, Cu
C©u 7: Nguyên tố R ở nhóm IVA . X là hợp chất khí của R với hidro trong đó hidro chiếm 25% về khối lượng. Công thức hợp chất X là:
A. H2Se B. CH4 C. SiH4 D. H2S
C©u 8: Cho biết tổng số electron trong ion 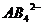 là 50. Trong các hạt nhân A cũng như B, số proton bằng số electron.Tổng số hạt mang điện trong 1 nguyên tử A gấp đôi tổng số hạt mang điện trong 1 nguyên tử B . Số khối ; tên nguyên tố của A và B lần lượt là:
là 50. Trong các hạt nhân A cũng như B, số proton bằng số electron.Tổng số hạt mang điện trong 1 nguyên tử A gấp đôi tổng số hạt mang điện trong 1 nguyên tử B . Số khối ; tên nguyên tố của A và B lần lượt là:
A. 28; Silic và 16; oxi B. 32; lưu huỳnh và 16; oxi
C. 12; cacbon và 16; oxi D. 14; nitơ và 16; oxi
C©u 9: Dãy gồm các phân tử có cùng một kiểu liên kết
A. MgO, Na2SO4 , Na3PO4 , AlCl3 B. Na2O, KCl, HCl , Al2O3
C. Cl2 , Br2 , I2 , HCl D. HCl , H2S , H2O , AlCl3
C©u 10: Cho các nguyên tố: Na, Mg, Li, K, Al, Si, N, S, Rb. Các nguyên tố thuộc cùng một chu kì là:
A. Na, Mg, Al, Si, S B. Mg, Al, Si, N, S C. Na, Li, K, Rb D. Na, Al,Si, N, S
C©u 11: Cấu hình electron lớp ngoài cùng của ion A+ là: 3s2 3p6. Vị trí của A trong bảng tuần hoàn là:
A. Ô 16, chu kỳ 3, nhóm IA B. Ô 20, chu kỳ 4, nhóm IIA
C. Ô 18, chu kỳ 3, nhóm VIIIA D. Ô 19, chu kỳ 4, nhóm IA
C©u 12: Chiều tăng độ âm điện của các nguyên tố được sắp xếp như sau:
A. O, N, C, Si, Al B. Al, Si, C, N, O C. Al, N, Si, O, C D. Al, Si, N, C, O
C©u 13: Dãy các tính chất biến đổi tuần hoàn theo chiều tăng dần của điện tích hạt nhân nguyên tử là :
A. Độ âm điện, khối lượng nguyên tử.
B. Tính kim loại, số proton trong hạt nhân.
C. Hóa trị của nguyên tố, số electron ở lớp vỏ.
D. Bán kính nguyên tử, cấu hình electron lớp ngoài cùng.
C©u 14: Cho 5,98 gam một kim loại M thuộc nhóm IA tác dụng với nước thu được 2,912 lít khí H2 (đktc). M là:
A. Na B. Li C. K D. Rb
C©u 15: Hình dạng các phân tử H2O, CH4, CO2 tương ứng là:
A. Gấp khúc, tứ diện, thẳng. B. Tam giác, thẳng, gấp khúc.
C. Tam giác, tứ diện, thẳng. D. Tứ diện, thẳng, tam giác
C©u 16: Để hòa tan hoàn toàn 15,2 gam hỗn hợp A gồm Fe và 1 kim loại M hóa trị 2 thuộc nhóm A cần 0,6 mol HCl. Nếu cho 12 gam M vào dung dịch axit HCl dư thì khí thoát ra (đktc) nhỏ hơn 7 lít. M là:
A. Be B. Mg C. Ca. D. Sr
C©u 17: Chọn phát biểu đúng:
A. Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron
B. Chu kì 3 gồm có 18 nguyên tố bắt đầu là nguyên tố Natri kết thúc là nguyên tố Agon
C. Nguyên tố d là những nguyên tố mà nguyên tử có electron cuối cùng được điền vào phân lớp p
D. Các nhóm B bao gồm nguyên tố p và nguyên tố d
C©u 18: Trong oxit cao nhất của nguyên tố X thuộc nhóm V A, tỉ lệ khối lượng của X và oxi bằng 15: 8. Nguyên tố X có nguyên tử khối bằng:
A. 14 B. 31 C. 75 D. 93
C©u 19: Chọn phát biểu sai:
A. Trong cùng chu kì, theo chiều tăng của Z, độ âm điện của các nguyên tố thường tăng dần
B. Trong một nhóm A, theo chiều tăng của Z, tính kim loại của các nguyên tố giảm dần
C. Độ âm điện đặc trưng cho khả năng hút e của nguyên tử trong phân tử
D. Trong một nhóm A, theo chiều tăng của Z, tính bazơ của các oxit và hiđroxit tương ứng của các nguyên tố tăng dần.
C©u 20: Số oxi hóa của cacbon, brom, lưu huỳnh, nitơ trong CaC2, HBrO4, Na2SO3, AlN lần lượt là:
A. -1, +7, +4, -3 B. -2, +7, -3, +4 C. +1, +3, -3, -2 D. +1, +3, -3, +4
C©u 21: Cho 10 gam hỗn hợp muối cacbonat của kim loại IA và IIA tác dụng với lượng dư dung dịch HCl, thu được 2,24 lít khí (đktc). Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là:
A. 11,1 B. 12,1 C. 9,1 D. 13,1
C©u 22: Hợp chất X gồm 3 nguyên tử của 2 nguyên tố Flo và oxi. Trong X , Flo chiếm 70,37% về khối lượng. Loại liên kết trong phân tử X là:
A. Ion B. Cộng hóa trị không cực
C. Cộng hóa trị có cực D. Cộng hóa trị có cực và cho nhận
C©u 23: Các nguyên tố dưới đây đều tạo clorua. Dãy các nguyên tố chỉ tạo hợp chất ion với clo:
A. Magie, photpho, lưu huỳnh B. Photpho, lưu huỳnh, cacbon
C. Canxi , natri, kali. D. Kali, photpho, cacbon
C©u 24: Dựa vào hiệu độ âm điện của các nguyên tố, chọn dãy gồm các chất được sắp xếp theo chiều tăng dần sự phân cực liên kết trong phân tử:
A. F2, NaF, HF, F2O B. F2O, NaF, F2 , HF C. F2, HF, F2O, NaF D. F2, F2O, HF , NaF
C©u 25: Số oxi hóa của Cr trong K2CrO4 là:
A. +6 B. -6 C. +1 D. +7
C©u 26: Cộng hóa trị của N trong phân tử HNO3 là:
A. 5 B. 4 C. +4 D. +5
C©u 27: Điều khẳng định sau về mạng tinh thể phân tử là đúng:
A. Lực hút trong mạng tinh thể phân tử là lực hút yếu giữa các phân tử.
B. Nút mạng tinh thể là các ion dương.
C. Chất có cấu tạo mạng tinh thể phân tử có nhiệt độ nóng chảy cao.
D. Chất có cấu tạo mạng tinh thể phân tử có độ cứng lớn.
C©u 28: Cho các phân tử sau: P2O5, PCl3, H3PO4 và CO. Theo qui tắc bát tử, số phân tử có liên kết cho nhận là:
A. 3 B. 1 C. 2 D. 4
C©u 29: Dãy các chất xếp theo chiều tính axit tăng dần:
A. HClO4, H2SO4, H3PO4, H2SiO3 B. H2SiO3, H2SO4, HClO4, H3PO4
C. H2SiO3, H3PO4, H2SO4, HClO4 D. H2SiO3, H3PO4, HClO4, H2SO4
C©u 30: Nhóm A gồm những khối nguyên tố nào?
A. s, d B. s, p C. s, f D. d , f
----------------- HÕt 178 -----------------
Tags: Huỳnh Mẫn Đạt

 Trang Trước
Trang Trước



No comments: